
为了响应《“健康中国2030”规划纲要》,实现我国全民消化肿瘤早诊早治,《肿瘤界》设立“齐力荟聚-消化肿瘤频道”,聚焦消化肿瘤患者的诊断治疗。旨在报道国内前瞻性、创新性和高学术水平的关于消化道肿瘤防治的临床应用和基础研究,把握学术发展动向,促进学术交流,整体提高国内消化肿瘤防治的临床与研究水平,结合国内研究特色,以及国内临床规范制度,推动消化肿瘤防治的进步,普及推广临床规范化诊疗。
一 专家访谈
专家简介

Q1 相比其它癌症,结直肠癌的发展速度相对缓慢,在发病早期,很容易与其它非肿瘤性疾病混淆。请您谈谈结直肠癌流行病学、危险因素及早期表现。
肠癌一般指大肠癌,是指位于升结肠、横结肠、降结肠、乙状结肠和直肠的恶性肿瘤。在中国,结直肠癌的发病率仅次于肺癌和胃癌,是非常常见的恶性肿瘤。结直肠癌的发病年龄多在40岁以上,80~84岁达到高峰。30岁以下者约占15%。男性较多见,男女之比为2~3:1,肠癌应以积极预防为主。
尽管目前对大肠癌确切的病因仍不清楚,但临床发现以下因素能大大增加大肠癌发生的危险性,包括:年龄、家族史、结肠炎性疾病史、大肠息肉史、基因背景等。
早期信号表现为:(1)突然体重减轻;(2)原因不明的贫血;(3)腹胀、腹痛、消化不良、食欲减退;(4)腹部有肿块;(5)大便带血(或出现黑便)及有下坠感;(6)大便内有脓血或粘液血丝;(7)大便习惯改变,便频或腹泻便秘交替;(8)经久不愈的肛门溃疡、持续性的肛门疼痛;(9)大便形状改变、变细、变扁或带槽沟;(10)发现有结肠多发息肉或乳头状腺瘤。
Q2 针对于结直肠癌提倡早诊断、早治疗,结直肠癌早期筛查是早期发现癌前病变或肿瘤,尽快进行根治性治疗的有效手段。请您谈谈结直肠癌早诊早筛的意义和方法?
结直肠癌早期筛查是早期发现癌前病变或肿瘤,尽快进行根治性治疗的有效手段。目前对于健康人群,推荐40岁以上一般人群接受结直肠癌风险评估。结直肠癌的筛查方法包括粪便隐血试验、直肠指检、肠镜、抽血化验等,最重要的是肠镜检查,以上检查相互结合,可早期发现肿瘤及一些癌前病变,有效减少肿瘤发生,从而提高肿瘤治愈率,降低死亡率,延长患者生存时间。
(一)结直肠癌早期筛查方法
肠癌早期筛查的方法包括:大便常规加隐血、肿瘤标志物检查、电子结肠镜检查、影像学检查等多种筛查方法。对于一些高度怀疑为肠癌的患者,需要检查癌胚抗原及糖类抗原CA19-9;电子结肠镜检查作为一种最直观发现肿瘤的方法,在临床上较为常用,它不仅可以帮助直观发现肠腔内的占位性病变或肿瘤,同时方便医生进行肿瘤组织的取材来进行病理诊断,这也是判断肠癌的金标准;而影像学检查目的是为了发现肿瘤的部位,肿瘤的大小,对周围器官的侵犯以及是否存在其他器官的远处转移。
【结肠镜检查】
结肠镜可以通过电视屏幕观察到结肠和大肠的内部情况,用来检查大肠的内部病变。还可以钳取小块病变组织进行病理检查,有助于明确诊断和判断病情的严重程度,进而指导治疗。随着内镜技术的日臻成熟,内镜黏膜切除术(EMR)、内镜黏膜下剥离术(ESD)不断进步,可以在结肠镜下辅助切除结直肠息肉,也可在结肠镜下止血等。
目前结肠镜作为不可替代的诊断方法。但结肠镜检查依然存在缺陷,如侵入性肠道准备繁琐、有创伤风险,人群筛查依从性较低,禁忌证人群无法进行此项检测。所以,肠癌早筛在人群中的渗透仍需非侵入性检测手段的支持。
【粪便隐血试验】
非侵入性检测手段如粪便隐血检测包括gFOBT(粪便隐血试验)和FIT技术(粪便免疫化学试验)。
正常人消化道胃肠黏膜上皮更新过程中每天约要丢失0.5~1.5 ml血液,但如果消化道的失血量每日大于2 ml时,说明消化道有病变出血,属于是病理性出血。大便肉眼观察不到大便内有血液、只有通过化学试验才能检出血液,称为大便隐性出血(FOB),简称大便隐血。该方法存在饮食限制、采样次数多、敏感性低的缺陷。
【基于粪便DNA(sDNA)或血液DNA筛查技术】
相比于传统肠癌筛查技术,基于DNA的肠癌筛查技术同时具备非侵入性和高敏感性的优点。该技术基本原理是:检测粪便中脱落的发生癌前病变肠黏膜细胞中的异常DNA。在粪便样品收集并运输到检测中心后,检测人员通过采用DNA提取和分离技术提取所需DNA,通过DNA检测技术筛查出早期肠癌。但基于粪便DNA检测的劣势在于假阳率比FIT还要高,价格也比较高。
以上几种主要的筛查方法各有优缺点,因此,需要根据自身情况来选择最符合自己的筛查方式。
(二)结直肠癌早诊早筛进展
随着时代的发展和数据的完善,精准治疗被越来越多地应用于临床。对于取出的病理组织,可以进行基因检测,根据结果有针对性地设计个体化治疗方案。
在肠镜检查中发现息肉的患者,要注意进一步检查。假性息肉(炎性息肉)可直接镜下电烧切除。而对于真性息肉(肠管状腺瘤),镜下电烧切除术后,一定要做病理学检查。对于有高危因素的管状腺瘤需要进一步做肠癌基因检测,能够准确预测该腺瘤的发生发展。
肠癌基因检查种类较多,肠癌的发生与基因突变有较大关系,所以基因检查对于判断或早期发现有无大肠癌较重要。临床上有较多检查方法,常用方法为粪便DNA检测,因为粪便检测取样简单、无创伤,且技术较先进、可靠性较强,应用较广泛,对于临床指导意义较大。
血液DNA检查,通过血液可查到变异基因,包括原癌基因、抑癌基因、易感基因,对肿瘤、大肠癌的诊断有指导意义,可通过检测DNA来指导大肠癌术后是否需靶向治疗或其它化疗方法。
Q3 近年来,转移性结直肠癌治疗取得了长足的进步,迈入靶向免疫时代。在结直肠癌领域,基因检测逐渐改变治疗策略,抗EGFR单抗历久弥新丰富精准内涵,经历了怎样的历程?
近年来,mCRC治疗取得了长足的进步。从早期的单药化疗到两药化疗,多个靶向治疗药物问世,更是进一步提高了有效率和延长了生存时间。现在免疫治疗和一些新的靶向治疗也进入了mCRC领域,治疗格局发生了重大改变。今天的mCRC治疗,不能像过去一样眉毛胡子一把抓,而是应该有选择、有策略地进行。
随着检测技术的发展和相关临床数据的充实,基因检测指导下的精准治疗在mCRC领域已经进入实战状态。很多临床研究都揭示了在不同基因突变状态下应该如何选择药物,比如 RAS/BRAF 野生型的结直肠癌患者,可以选用西妥昔单抗;HER2阳性患者,可以在后线选择抗HER2相关药物;高度微卫星不稳定(MSI-H)型患者,可以选择免疫治疗。
临床上药物可及,基因检测更准确,使得治疗的精准度和有效率大幅提高,同时也避免了一些不必要的治疗。目前,直接应用到临床的mCRC基因检测已经有10种左右,临床医生要关注患者的基因突变及分型,给患者提供最准确的治疗,使患者得到最佳获益。
客观来讲,在 RAS/BRAF 野生型左半mCRC患者中使用西妥昔单抗相比贝伐珠单抗更有优势。在双药化疗联合抗EGFR单抗研究中,已经证明西妥昔单抗有效率更高,部分缓解(PR)时间更长,总生存(OS)也更长。
此外,一些研究表明三药联合化疗可以进一步提高有效率和转化率。所以对于RAS/BRAF 突变的预后差的,身体各方面状态都比较好、年轻的患者,可以选用三药化疗联合抗VEGF单抗,使患者有更好的缩瘤率和更高的转化率。
同时,由于ct-DNA检测的临床应用更成熟,我们发现一些原来是 RAS/BRAF 野生的患者,经过治疗后变成RAS/BRAF 突变的,那么治疗也要及时调整。这是一个很新鲜的概念,也有待更多的数据去证实。mCRC的治疗仍需要更多的研究去挖掘基因突变的规律,以及对临床治疗的指导意义,让患者获得合适的治疗。
Q4 今年4月CACA-RC指南根据一系列研究进展,将曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗这一联合方案推荐为晚期不可切除直肠癌一线治疗方案。请您结合相关研究,谈谈曲氟尿苷替匹嘧啶片(TAS-102)作为晚期不可切除结直肠癌的一线用药具有怎样的优势?
曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗方案因其高效、低毒的特点,为不适合强烈治疗的 mCRC 患者及老年患者带来了新的希望,其疗效与生存获益令人期待。
2022年 CACA-RC 指南基于 TASCO-1 研究的结果,推荐拒绝静脉化疗或不能耐受强烈治疗、易敏的晚期结直肠癌患者姑息一线选择曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗方案。TASCO-1 研究是一项旨在随机比较曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗和卡培他滨+贝伐珠单抗在一线治疗不可接受高强度治疗的不可切除转移性结直肠癌的II期研究。研究结果显示:曲氟尿苷替匹嘧啶片(TAS-102)组延长患者 mPFS 时间1.41个月(9.23个月 vs 7.82个月);延长患者 mOS 时间4.64个月(22.31个月 vs 17.67个月)。安全性分析也提示曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗治疗具有良好的耐受性,它最常发生的3/4级不良事件是中性粒细胞减少。严重的发热性中性粒细胞减少症率约为4%。
既往晚期转移性结直肠癌的一线标准化疗方案在国内外指南中均是以奥沙利铂或伊立替康为基础的,即 FOLFOX、CapOX 或 FOLFIRI 方案,在此基础上,可以根据患者基因型和原发灶部位联合西妥昔单抗或者贝伐珠单抗。但是,依旧有部分患者身体状况无法耐受这种强度化疗,少数患者因为高敏可能出现药物过敏,针对这一类患者,治疗方案的选择非常有限且预后情况并不理想。推荐曲氟尿苷替匹嘧啶片(TAS-102)+贝伐珠单抗方案应用于拒绝静脉化疗或不能耐受高强度治疗、易敏的晚期结直肠癌患者姑息一线治疗,为晚期转移性结直肠癌的治疗开启新的篇章。
二 病例分享
01 基本情况
基本信息:陈XX,65岁。
主诉:患者于2017.10.11 因便血行肠镜检查示:回盲部新生物。
既往史、个人史:高血压病史。
家族史:无特殊。
02 初诊病史
患者于2017.10.11 因便血行肠镜检查示:回盲部新生物。
03 治疗方案
2017年10月诊断:右半结肠癌。
2017.10.11 在我院外科行“腹腔镜下右半结肠癌根治术+回肠造口术”。
术后病理:
肉眼所见:1. (右半结肠)结肠27cm*3.5cm,回肠12.5cm*2cm,回盲部阑尾开口处腹膜覆盖区见6.5cm*3.4cm隆起溃疡型肿块,切面灰白,穿透基层;2. 粘膜组织2.2cm*1.5cm一块。
镜下所见:(右半结肠)中分化腺癌,癌组织穿透肠壁固有肌层至浆膜下脂肪组织(pT3),癌组织累及周围淋巴结(1枚),伴结肠系膜淋巴结(3/16枚)癌转移;阑尾、结肠及回肠侧手术切缘、环周切缘阴性。
免疫组化染色示肿瘤细胞:MSH6(+), MSH2(+), MLH1(+),PMS2(+)。RAS,BRAF 野生型。
术后诊断: 右半结肠癌术后(pT3N1bM0),pMMR。
2017.11.7 至2018.4.12 行7周期FOLFOX4方案化疗。
2018.6.26 行造口还纳术,后定期复查。
2019年3月胸部CT:右肺上叶近水平裂胸膜处有一枚结节,大小约6mm*5mm,考虑肿瘤转移;腹部MRI:肝右叶S8段新发结节,弥散受限,约16mm*12mm,考虑转移瘤可能性大。
2019年3月肿瘤标记物:CEA 22.8ng/ml, CA19-9, CA125正常。
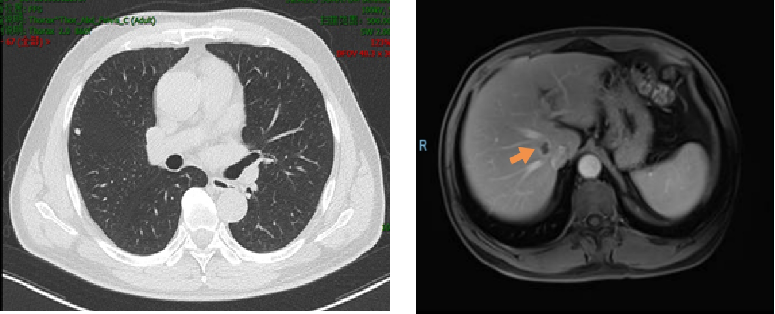
诊断:1. 右半结肠癌术后(pT3N1bM0)化疗后进展(肝,肺?),(RAS、BRAF 野生型,pMMR);2. 高血压病。
MDT讨论结果
目前诊断为右半结肠腺癌术后肝肺转移;
患者为异时性复发;
目前为寡转移:肝脏病灶一个,肺部病灶一个;
治疗目标:NED;
肝脏病灶位于S8段,上下骑跨动脉,难以手术切除,考虑射频消融治疗;
肺部病灶可能为转移灶,小于1cm,可密切观察。积极处理的话,考虑手术为首选。
如不能达NED,再予以全身化疗或加靶向治疗。
2019.4.10于介入科行肝S8段转移瘤射频消融术。
患者拒绝肺部病灶手术治疗,选择观察等待。
2019.4.24 行FOLFIRI方案化疗1周期,期间出现II度血小板减少,后患者拒绝继续化疗。
因肝脏转移瘤靠近血管,射频消融术后复查CT认为肿瘤边缘存在强化,2019.5.27 行肝S8段转移瘤放疗,DT 40GY/5F。
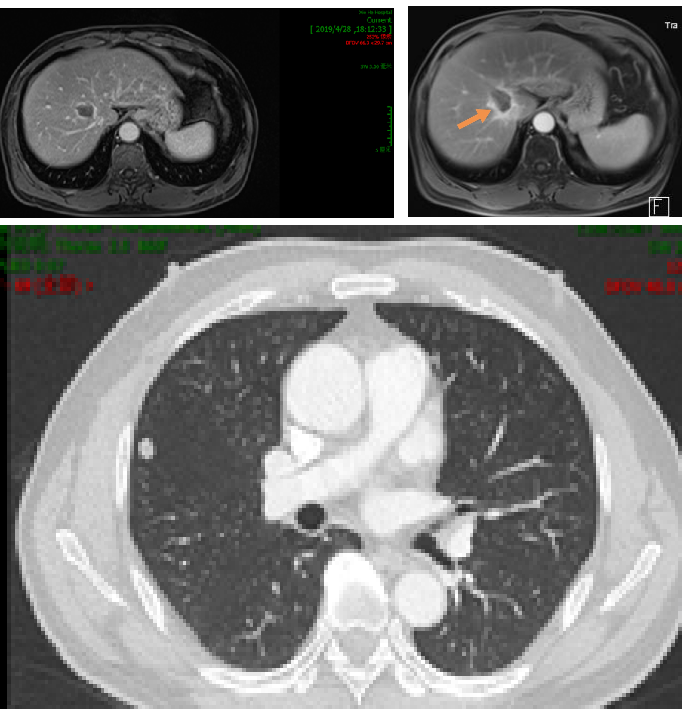
2019年9月复查,右肺结节略增大,由6mm变成9mm,肺部单个转移灶建议患者手术,病人拒绝,继续选择观察。
2019年10月患者出现头晕严重,不能下床独立行走,伴额头及右侧肢体麻木。
2019.10.18 当地医院头部MRI示:脑干区异常信号,约11mm*15mm,考虑转移瘤合并脑卒中。
体检:神情,言语不流利,口角左侧歪斜,右侧上下肢肌力2级。
化验:血常规、肝肾功能正常,CEA正常。
脑部蛋氨酸PET示:脑桥结节,蛋氨酸代谢异常增高,SUVmax 4.51,考虑转移性恶性肿瘤。
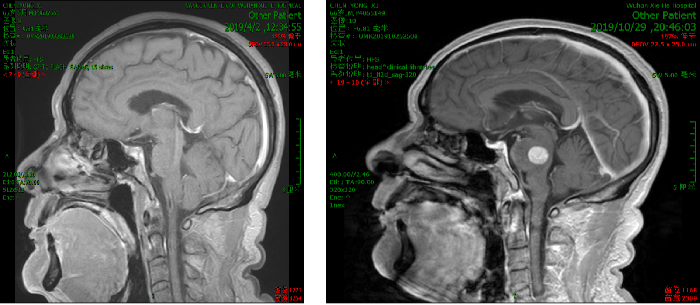
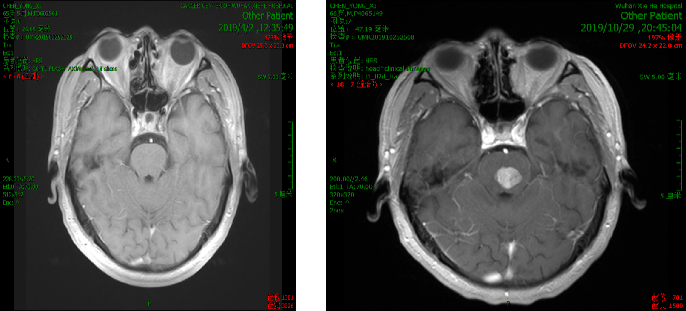
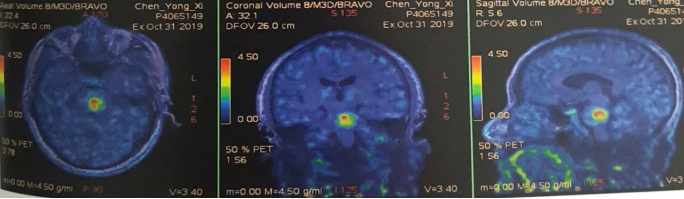
影像科、神经内科会诊,考虑脑部病灶为肠癌转移病灶。
MDT讨论结果
患者为晚期结肠癌合并肝、肺、脑干转移,但是每个器官为单发病灶,肝转移灶经过治疗后稳定,右肺单个病灶稍有增大。但脑干转移灶严重影响患者生活质量及生存,建议先行脑干病灶局部放疗,再行化疗+靶向治疗。靶向治疗考虑选用抗VEGF单抗。
治疗目标:控制局部症状,提高生活质量,延长患者生命。
脑干转移病变,合并瘤卒中,周边水肿。
处理:2019.11.5至2019.11.10行射波刀放疗,DT 20GY/4F,同步替莫唑胺化疗。
10天后复查脑部CT提示病灶变化不明显,出血量无增加,水肿无增加。
处理:再次射波刀追加剂量,DT 20GY/4F,贝伐珠单抗200mg治疗一次。
效果:患者脸部麻木及右侧肢体麻木症状改善明显,肌力IV级,可独自行走。
2019.12.10行伊立替康+贝伐珠单抗300mg化疗1周期
2019.12.27、2020.1.17行FOLFIRI+贝伐珠单抗化疗2周期,期间出现Ⅱ~Ⅲ度血小板减少,患者拒绝继续治疗
2020.5.28 复查示肝脏及脑干病灶稳定,肺部结节略增大。
2020.5.30至2021.5.25 行卡培他滨+贝伐珠单抗治疗,期间疗效评价SD。
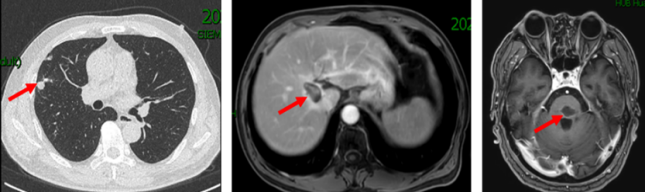
2021.7.27 复查CT示右肺上叶近水平裂实性结节,较前稍增大;右肺前段沿肺纹理分布的多发结节,较前新发,疗效评价为PD。
MDT讨论结果
患者目前诊断为结肠癌综合治疗后(肝、脑、肺),不可手术切除,但病程为缓慢进展。右上肺增大病灶可行局部放疗。全身治疗上考虑患者化疗耐受性差,治疗期间持续存在Ⅱ~Ⅲ度血小板减少,建议更改呋喹替尼靶向治疗,同时考虑抗血管靶向联合免疫治疗在部分晚期肿瘤中取得一定效果,可联合免疫治疗。
治疗目的:控制病灶,提高生活质量,延长生存时间。
04 疗效评估
2021.8.16 始行右肺上叶病灶射波刀放疗,DT 54Gy/6F,同时口服呋喹替尼。
2021.9.22 开始:呋喹替尼 3mg/d+信迪利单抗治疗。
2021.11.25 复查疗效评价为SD。
患者症状明显改善:右侧肌力IV级。
2022.3.29 复查:
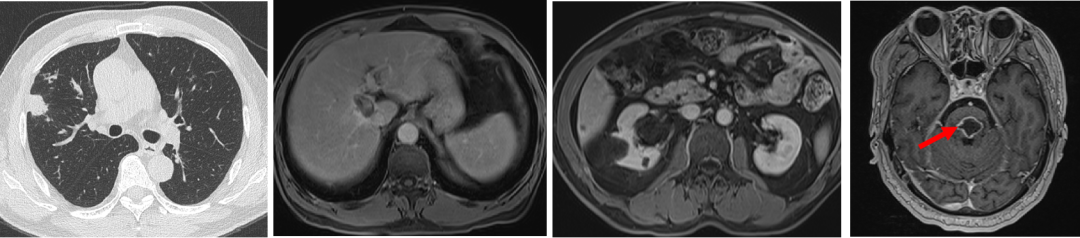
1. 右肺上叶近水平裂实性结节,较前增大;
2. 右肺多发结节,部分较前略增大;
3. 肝右叶S8段异常强化灶,考虑转移性肿瘤,较前相仿;
4. 肝SVI段新发结节,考虑转移瘤;
5. 脑干转移瘤并周围水肿,较前增大。
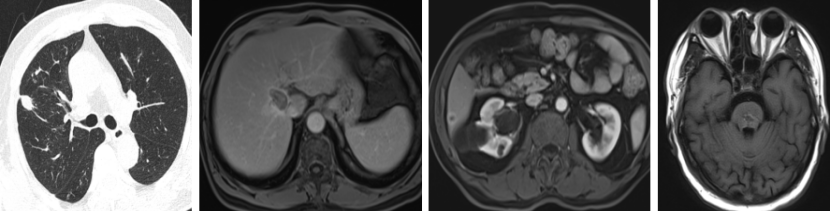
2022.4.2 始行TAS-102+贝伐珠单抗(双周方案)治疗8个周期,6周期时复查,疗效评价为缩小的SD。
05 病例体会
MDT讨论以及局部治疗在寡转移瘤中的重要性;
立体定向放射外科(SRS)在脑干转移瘤中的治疗价值;
卡培他滨+贝伐珠单抗对于不适合进行高强度治疗的患者的应用;
抗血管靶向联合免疫治疗在部分晚期肠癌中的疗效;
TAS-102联合贝伐珠单抗在晚期肠癌中的疗效及应用。
*本文仅代表专家观点,并经专家审校。