前言
2024年欧洲肿瘤内科学会亚洲年会(ESMO ASIA 2024)于当地时间12月6日-8日在新加坡召开,ESMO ASIA是亚太地区讨论肿瘤学领域重磅突破的领先平台,多项全球及亚太地区的最新科研和临床进展在会上公布。
研究背景
在全球III期CheckMate 77T研究中,对于可切除的II–IIIB期非小细胞肺癌(NSCLC),围术期应用纳武利尤单抗相比新辅助化疗加术后辅助安慰剂,显著改善了患者的无事件生存期(EFS)。研究者在本次大会上报告CheckMate 77T研究中国患者的临床结果。
研究方法
研究纳入未接受治疗的可切除IIA期(>4 cm)至IIIB期(N2)NSCLC患者,这些患者无EGFR突变或已知的ALK重排,且体能状态评分(ECOG)≤1。患者以1:1比例随机分组,接受纳武利尤单抗(360 mg)的纳武利尤单抗联合铂类双药化疗或安慰剂联合铂类双药化疗,每3周1次(Q3W),共4个周期,随后进行手术和术后辅助纳武利尤单抗(480 mg)或安慰剂治疗,每4周1次(Q4W),共13个周期。CheckMate 77T研究共纳入了68例中国患者。研究的主要终点为盲法独立中央评审(BICR)根据RECIST v1.1评估的EFS,次要终点包括BIPR评估的病理完全缓解率(pCR)、主要病理缓解率(MPR)和安全性。探索性终点为BIPR评估的客观缓解率(ORR)。
研究结果
基线特征在两组间总体平衡(纳武利尤单抗组n=37;PBO组n=31)。中位随访29.1个月,纳武利尤单抗组患者的中位EFS尚未达到(22.6个月-NE),安慰剂组的为12.6个月(3.5-NE),风险比(HR)为0.40(95% CI:0.17–0.92)。此外,两组患者的1年EFS率分别为77.2%和51.1%。与安慰剂组组相比,纳武利尤单抗组的pCR率(35.1% vs 3.2%)、MPR率(51.4% vs 6.5%)和ORR(78.4% vs 32.3%)均有所提高(见下表)。最终手术完成率分别为81%和61%。
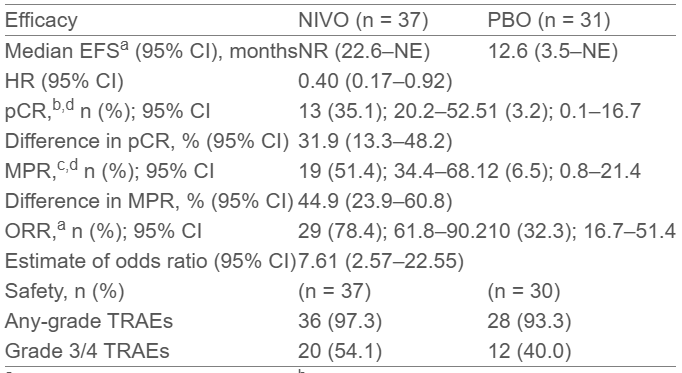
a 根据 RECIST v1.1 标准由 BICR 评估;b 原发肿瘤和淋巴结中残留的可存活肿瘤细胞为 0%;c 手术后原发肿瘤和淋巴结中可存活肿瘤细胞 ≤10%;d 根据 BIPR 评估,NR 表示未达到(Not Reached)。
安全性方面,3/4级治疗相关不良事件(TRAEs)发生率分别为54%和40%。
研究结论
在可切除的IIA–IIIB期NSCLC的中国患者中,与安慰剂治疗相比,纳武利尤单抗在EFS、pCR和MPR方面显示出临床意义上的改善,且未观察到新的安全性信号。值得注意是,由于样本量有限,解读结果时需谨慎。
参考文献:
Lin Wu, et al. Perioperative nivolumab (NIVO) in patients (pts) with resectable stage II–IIIB NSCLC: CheckMate 77T Chinese population analysis. 2024 ESMO Asia Abstract 594P.
编辑:黄鸿飞