KRAS突变素有肿瘤领域“不可成药”靶点之称,其中KRAS G12D是实体瘤中最常见的突变亚型,在胰腺癌、非小细胞肺癌、结直肠癌等高发肿瘤中频发,临床上长期缺乏针对性治疗药物,存在巨大未被满足的医疗需求。
近日,浙江省肿瘤医院宋正波教授作为主要通讯作者,博士后谢玲作为第一作者,联合中国科学院杭州医学研究所等多家单位完成的研究成果“Preclinical Characterization and Clinical Activity of RNK08954, a Highly Selective and Orally Bioavailable KRASG12D Inhibitor”,在线发表于肿瘤学期刊Cancer Discovery(IF=33.3)。
该研究首次全面报道了新一代高选择性、口服生物可利用的KRAS-G12D抑制剂RNK08954的临床前研究数据和Ia期临床初步结果,为KRAS G12D突变实体瘤患者解锁了全新治疗方向。

01. 攻坚克难,全新高选择性KRAS-G12D靶向抑制剂
KRAS基因是调控细胞增殖、存活和分化的关键癌基因,其突变会导致下游MAPK、PI3K/AKT等信号通路持续激活,成为驱动肿瘤发生、发展的核心因素。其中KRAS G12D突变因缺乏可结合的活性位点,成药难度远超其他KRAS突变亚型,长期以来是靶向治疗领域的一大难题。
RNK08954是一款新型非共价KRAS-G12D选择性抑制剂。该药物通过与KRAS-G12D蛋白形成盐桥,实现对靶点的高亲和力结合,其对野生型KRAS及G12C、G12V等其他突变亚型则表现出高度选择性,选择性倍数最高达339倍。临床前研究证实,RNK08954的抑制活性显著优于同类抑制剂MRTX1133,以浓度、时间依赖性抑制KRAS下游p-ERK1/2、p-AKT等信号通路,诱导肿瘤细胞G0-G1期周期阻滞并引发细胞死亡,在KRAS G12D突变肿瘤细胞中IC50值低至2.6 nmol/L。
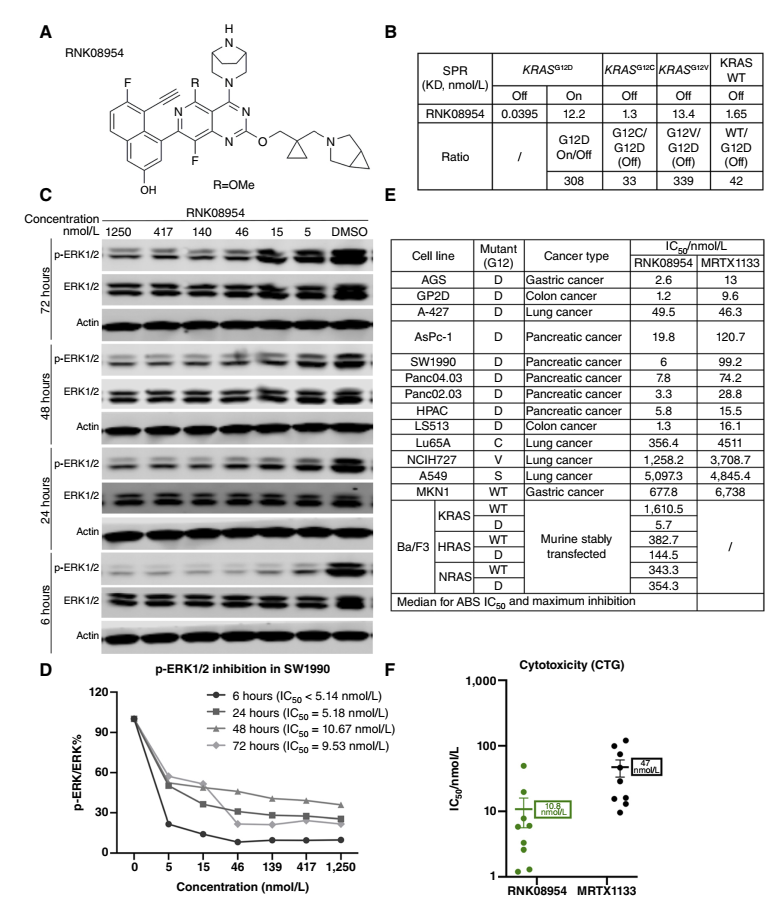
同时,RNK08954展现出独特的药代动力学特征:口服生物利用度良好,消除半衰期长达7.86小时,且能优先在肿瘤组织中富集,在动物模型中肿瘤组织与血浆的暴露比最高可达223倍,这种靶向性分布大幅提升了抗肿瘤效果,降低了全身毒性。
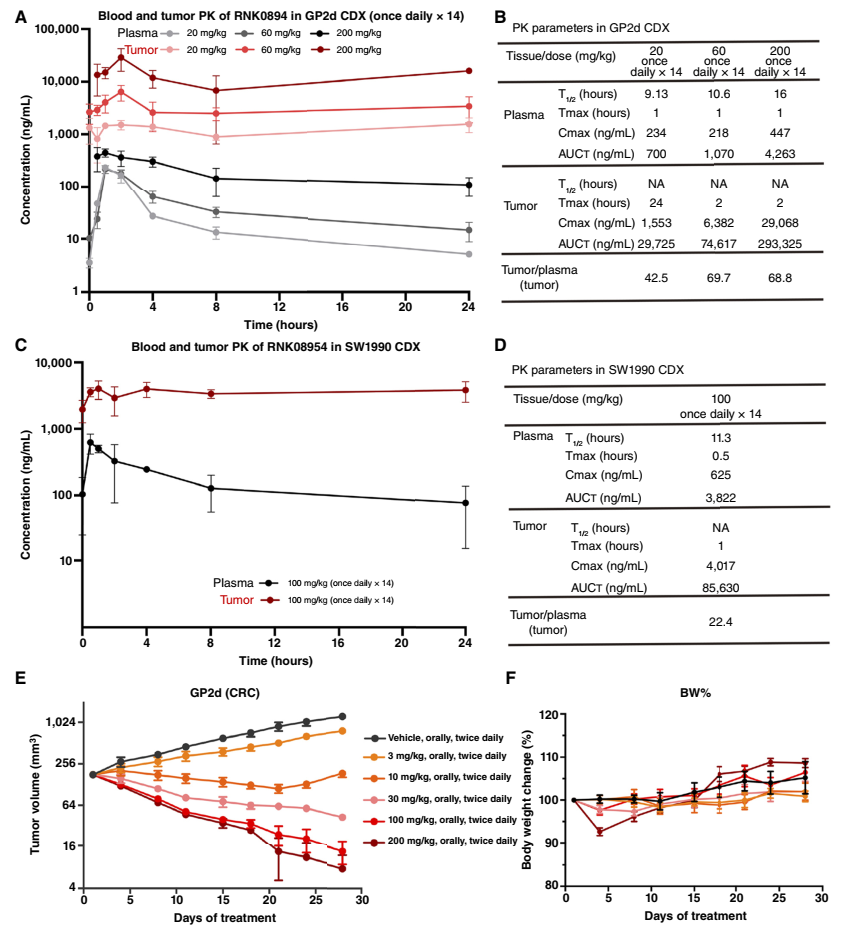
在多种KRAS G12D突变肿瘤的细胞系异种移植模型(CDX)、患者来源异种移植模型(PDX)及原位模型中,RNK08954均能显著抑制肿瘤生长,甚至在Panc 04.03模型中实现100%肿瘤消退,且安全性良好,无明显体重下降等毒性反应。
此外,研究还发现RNK08954可有效调节肿瘤免疫微环境,显著增加肿瘤组织中CD8+T细胞浸润,与PD-1抑制剂联用可产生显著的协同抗肿瘤效果,为后续联合免疫治疗奠定了坚实的理论基础。
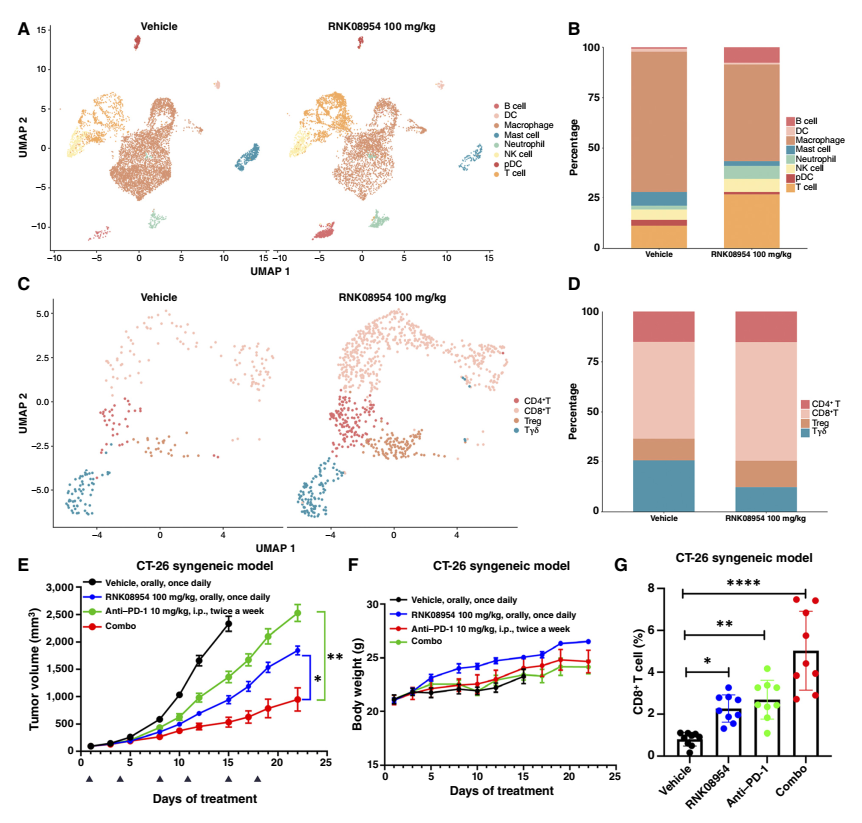
02. 初露锋芒,Ia期临床研究成果彰显优异疗效与安全性
基于优异的临床前数据,团队牵头启动了RNK08954的首次人体I期临床试验(NCT06667544),宋正波教授作为主要研究者牵头开展了该研究的Ia期剂量递增阶段,研究共纳入42例KRAS突变晚期实体瘤患者,涵盖胰腺癌、非小细胞肺癌、结直肠癌等主要瘤种。截至2025年10月数据截止时,36例可评估患者的中位随访时间为4.85个月,研究结果展现出出色的安全性和令人鼓舞的抗肿瘤活性,核心亮点如下:
1)安全性优异,耐受性良好:研究中无剂量限制性毒性发生,所有治疗相关不良事件以胃肠道反应(腹泻、呕吐、恶心)为主,且多为1-2级,3级及以上不良事件发生率仅23.8%,仅少数患者因不良事件进行剂量调整,药物整体耐受性优异;
2)非小细胞肺癌队列疗效突出:12例可评估的非小细胞肺癌患者,其中7例患者达到部分缓解(PR);客观缓解率(ORR)为58.33%,5例达到疾病稳定(SD),疾病控制率(DCR)为100%。83%的患者既往接受过铂类化疗,92%接受过免疫治疗,提示该药物在经多线治疗的难治性患者中仍能发挥显著疗效;
3)胰腺癌队列实现突破性进展:在1000-1200mg高剂量队列中,两名患者达到PR,ORR为33.33%,四名患者达到SD,DCR为100%,中位治疗时间延长至6.43个月,RNK08954为这一难治性肿瘤带来了全新治疗希望;
4)药代动力学特征契合临床需求:药物吸收迅速,在400-1200mg剂量范围内暴露量与剂量呈正相关,1000mg和1200mg被确定为扩展研究的推荐剂量。
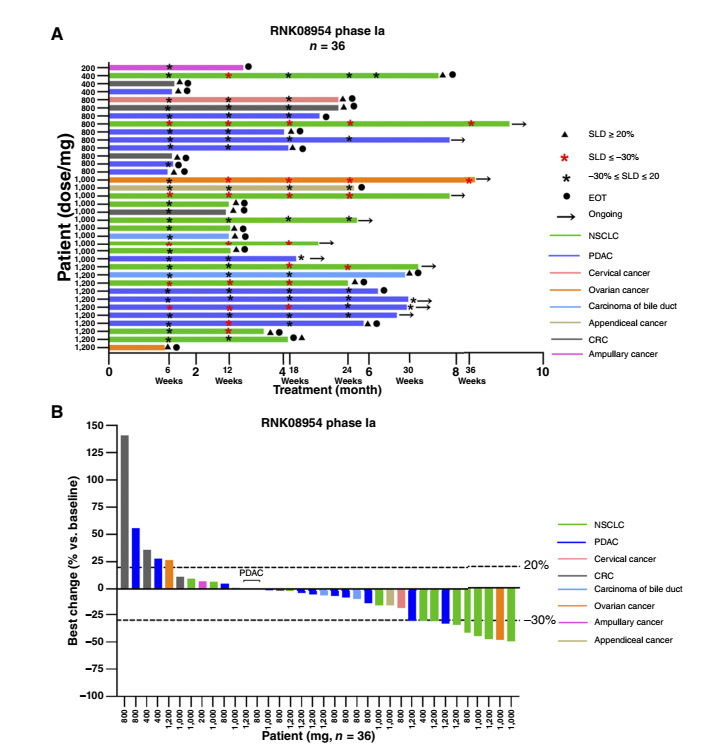
03. 意义深远,填补临床空白,开启KRAS靶向治疗新征程
本研究的发表,标志着我国在KRAS-G12D靶向药物研发领域取得了重要突破,RNK08954作为潜在的首个口服生物可利用的KRAS-G12D抑制剂,其独特的药代动力学特征、强效的抗肿瘤活性和良好的安全性,有望填补KRAS G12D突变实体瘤靶向治疗的临床空白,为胰腺癌、非小细胞肺癌等缺乏有效治疗手段的肿瘤患者提供全新的治疗选择。
同时,研究证实了RNK08954与免疫检查点抑制剂联用的协同潜力,为后续开展联合治疗研究、进一步提升疗效奠定了基础。目前,RNK08954的Ib期剂量优化研究正在顺利开展,未来将进入II期扩展研究,有望加速推进临床转化,早日为更多KRAS G12D突变肿瘤患者带来福音。
据悉,本研究的I期研究部分已经被2026年ASCO会议遴选为口头报告,作为本研究的牵头人,宋正波教授将代表项目组在国际上展示该研究的最新学术成果。
此次研究成果的发表,是浙江省肿瘤医院在肿瘤创新药物临床研究领域的一项重要突破,彰显了该院在肿瘤精准治疗临床转化方面的领先地位,也体现了产学研医协同创新在攻克肿瘤“不可成药”靶点中的核心作用。未来,该院将继续聚焦临床需求,推动更多新型抗肿瘤药物的研发和临床转化,为广大肿瘤患者提供更优质、更精准的治疗方案,助力健康中国建设!
通讯作者简介

来源:浙肿发布