本文刊登于《肿瘤药学》2026, 16(1): 1-10. DOI: 10.3969/j.issn.2095-1264.2026.01.01.
【引用本文】徐恒戈,王先火,张会来. 新型CAR-T细胞疗法研究进展[J]. 肿瘤药学, 2026, 16(1): 1-10.
DOI:10.3969/j.issn.2095-1264.2026.01.01.
作者:徐恒戈,王先火,张会来
通信作者:张会来,天津医科大学肿瘤医院淋巴瘤内科/国家恶性肿瘤临床医学研究中心/药物成药性评价与系统转化全国重点实验室,博士,主任医师。
嵌合抗原受体T细胞(chimeric antigen receptor T cell, CAR-T)治疗是近年来肿瘤免疫治疗领域最具代表性的突破之一。靶向CD19或B细胞成熟抗原(B cell maturation antigen, BCMA)的CAR-T产品已在多种复发/难治性血液肿瘤中展现出显著疗效,多种产品临床获批,为患者带来了深度且持久的抗肿瘤效应[1]。然而,该疗法的广泛应用仍面临诸多限制,如自体CAR-T制备流程复杂、周期长且成本高昂,导致部分患者因疾病进展或细胞质量不佳而错失治疗机会;同时,细胞因子释放综合征(cytokine release syndrome, CRS)与免疫效应细胞相关神经毒性综合征(immune effector cell-associated neurotoxicity syndrome, ICANS)等严重不良反应也对临床管理和医疗资源配置提出了较高要求[2]。因此,当前CAR-T领域的研究重点正逐渐转向提高治疗的可及性、安全性与可控性,这不仅涉及CAR结构和功能的优化,也包括对制备流程、递送方式及治疗全程管理的系统性革新[3]。
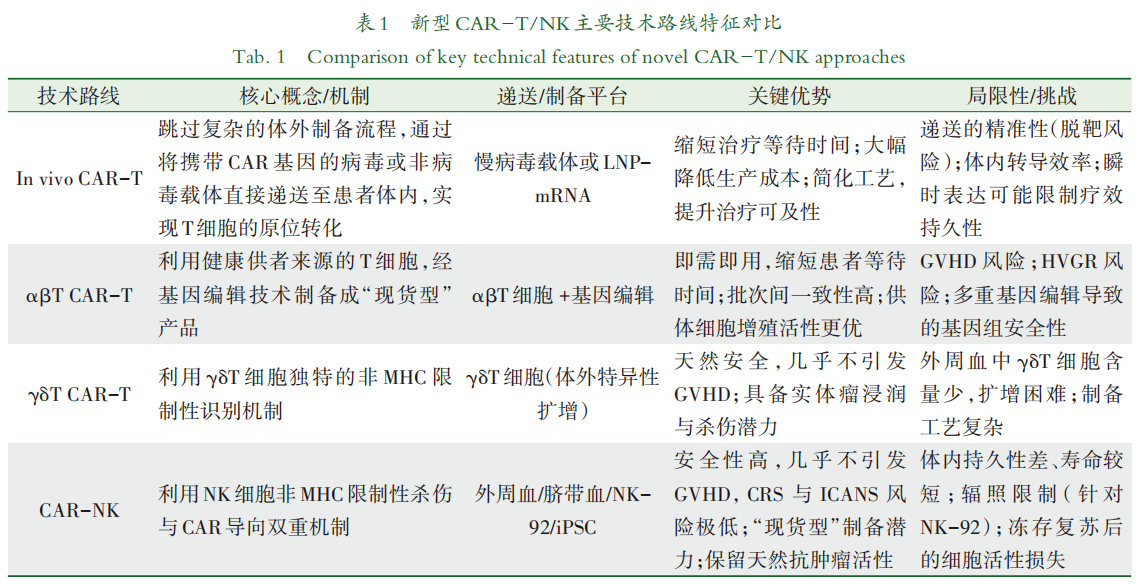
围绕提升治疗可及性与可控性的目标,CAR-T研究近年来形成了多条技术路线。首先,体内CAR-T(in vivo CAR-T)旨在通过病毒载体或非病毒纳米递送系统将CAR基因直接导入患者体内的T细胞,使CAR-T细胞在体内生成,从而有望缩短治疗等待时间并减少对复杂体外制备流程的依赖。其次,通用型(异体)CAR-T(universal CAR-T)利用基因编辑等技术降低移植物抗宿主病(graft versus host disease, GVHD)和宿主免疫排斥风险,致力于开发可提前制备、随时可用的“现货型”产品。此外,NK细胞来源的CAR(CAR-NK)凭借其较低的GVHD风险、较小的细胞毒性及丰富的细胞来源,成为兼顾安全性与规模化生产可行性的另一重要研究方向。
本文拟在简要介绍CAR-T的基本结构、作用机制及相关不良事件的基础上,重点综述in vivo CAR-T、通用型CAR-T(包括γδT CAR-T)及CAR-NK的关键技术路线、代表性研究进展与临床转化现状,进而讨论其在制备、疗效、安全性及临床管理等方面面临的挑战,以期为后续研究设计和临床策略优化提供参考。
1 CAR-T的基本概念、作用机制与临床管理
1.1 CAR的基本结构与功能
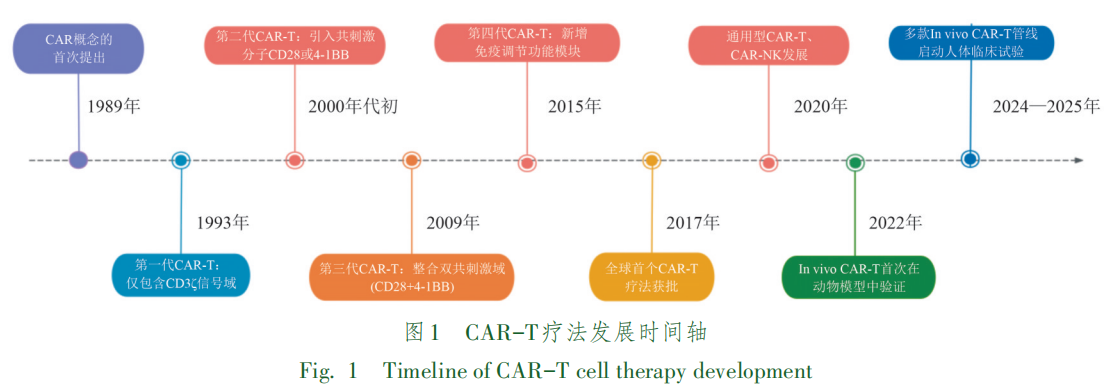
CAR是一种人工构建的跨膜受体,其典型结构包括胞外域、跨膜域及胞内域3个核心组件,这一结构使T细胞能够不依赖于主要组织相容性复合体(major histocompatibility complex, MHC)呈递,直接识别肿瘤细胞表面抗原并实现特异性杀伤[4]。
胞外域主要由单链可变片段(single-chain variable fragment, scFv)和铰链区(hinge region)构成,其中scFv负责识别并结合肿瘤相关抗原(tumor-associated antigen, TAA),铰链区则在连接和调节空间构型方面发挥作用。跨膜域除起到物理连接作用外,对受体稳定性和免疫突触形成具有重要影响[5]。胞内域整合了T细胞激活信号域(如CD3ζ)和共刺激信号域(如CD28和4-1BB)。共刺激分子的选择差异会影响CAR-T细胞的扩增动力学、持久性及功能表型,一般认为CD28信号倾向于驱动快速扩增,而4-1BB信号更有利于维持细胞长期存活,但上述差异受到制备工艺、细胞来源与疾病环境等多因素影响[6]。
1.2 CAR-T抗肿瘤作用机制与相关毒性
CAR-T细胞的抗肿瘤效应依赖于其对靶抗原的特异性识别及免疫突触的形成。抗原结合后,胞内信号域被激活,启动下游信号通路,进而诱导T细胞活化、增殖并释放效应分子。其主要杀伤机制包括穿孔素-颗粒酶介导的细胞毒作用、死亡受体相关通路及细胞因子介导的间接抗肿瘤效应[4, 7]。临床获益不仅取决于CAR结构设计,还与CAR-T细胞在体内的药代动力学及其对肿瘤微环境的适应能力密切相关。
CAR-T治疗相关毒性与其免疫激活机制密切相关。CAR-T细胞在体内大量扩增并释放炎症细胞因子,进而激活其他免疫细胞,引发系统性炎症反应。临床上最常见且具有代表性的毒性事件包括CRS和ICANS。CRS一般表现为发热、低血压和低氧血症,其严重程度与肿瘤负荷、CAR-T细胞扩增峰值及炎症细胞因子水平有关[8]。ICANS主要累及中枢神经系统,其发病机制尚未完全明确,可能与血脑屏障通透性增加及神经炎症反应有关[9]。此外,CAR-T治疗还可能引起B细胞缺乏、感染风险加剧及其他器官相关毒性,提示疗效增强往往伴随着安全性挑战。
1.3 与诊疗相关的关键评估指标
CAR-T相关毒性的发生受多种因素影响,包括肿瘤负荷、CAR-T细胞体内扩增特征、预处理方案及患者基础炎症状态等,因此,构建围治疗期的全程风险管理体系是保障治疗安全的关键。在当前临床实践中,托珠单抗、糖皮质激素及对症支持治疗是CAR-T相关毒性干预的核心手段[10]。
为实现精准化治疗和安全性优化,需对靶抗原表达水平、肿瘤负荷、免疫微环境特征、CAR-T细胞扩增情况及细胞因子变化等进行动态监测。治疗后结合微小残留病(minimal residual disease, MRD)、循环肿瘤DNA(circulating tumor DNA, ctDNA)及影像学评估,有助于早期判断疗效和复发风险[11]。将上述指标与不同CAR设计和工程化策略相结合,有助于更精准地把握疗效与毒性之间的关系,从而为后续治疗决策提供数据支持。
2 新型CAR-T的研究进展
2.1 in vivo CAR-T
2.1.1 概念与作用机制
in vivo CAR-T是一种新兴的免疫治疗策略,其核心理念在于绕过传统CAR-T治疗复杂的体外基因改造与扩增流程,通过直接向患者体内递送编码CAR的基因载体,从而在体内原位实现T细胞的CAR修饰并发挥抗肿瘤作用。相较于传统体外CAR-T(ex vivo CAR-T),该模式显著简化了治疗流程,避免了细胞分离、体外扩增及质检等环节,因而有望大幅降低生产成本,显著提升治疗的可及性与时效性[12-13]。
in vivo CAR-T的实现首先依赖于病毒载体或纳米递送系统将CAR基因精准递送至患者体内T细胞。载体成功进入T细胞后,外源基因经转录与翻译,在细胞表面稳定表达CAR蛋白。该蛋白的胞外结构域可特异性识别肿瘤相关抗原(如CD19、BCMA),随后激活胞内信号域,启动下游效应程序并释放穿孔素与颗粒酶,最终诱导靶细胞发生免疫介导的凋亡[12,14]。
2.1.2 递送平台
当前的in vivo CAR-T技术路线主要分为两条:一是以慢病毒(lentivirus, LV)为代表的整合型病毒载体路线,二是以脂质纳米颗粒(lipid nanoparticle, LNP)递送信使RNA(messenger RNA, mRNA)为核心的非病毒载体路线。
整合型病毒载体路线通常需先将载体靶向递送至T细胞,经膜融合后,病毒颗粒转运至细胞质或内溶酶体区室,最终实现CAR转基因的基因组整合。该路线的优势在于单次给药即可实现CAR的持久表达,但也面临病毒载体半随机整合带来的插入突变与克隆性扩增隐患,以及系统给药时非目标细胞(如B细胞或髓系细胞)的脱靶转导及异常表达等问题。因此,基于慢病毒的平台旨在通过多种方式提升靶向性和安全性。如EsoBiotec开发的ENaBL平台通过改造慢病毒衣壳蛋白上的VSVG突变体、在病毒表面展示抗T细胞受体(T cell receptor, TCR)纳米抗体,以实现T细胞特异性靶向,并过表达CD47抵抗巨噬细胞的吞噬清除,从而构建出“免疫屏蔽”的慢病毒载体[15]。Umoja Biopharma的VivoVec技术平台则在载体上融合了抗CD3的scFv,以增强T细胞识别,以及CD80共刺激分子,旨在提高转导效率和后续CAR-T细胞的活化与增殖能力[16]。这些工程化的慢病毒载体不仅提高了靶向精度,还通过引入T细胞特异性启动子等生物学元件,进一步限制了CAR在非目标细胞中的表达,从而增强了安全性。
非病毒载体路线以LNP-mRNA为代表,其介导的CAR表达具有瞬时性特征,理论上降低了长期毒性与基因组整合风险,且生产工艺相对简单,易于规模化生产。然而,由于CAR蛋白仅能表达数日至数周,往往需要依赖重复给药以维持疗效,但LNP重复给药可能诱导机体产生针对载体组分(尤其是聚乙二醇化脂质)的抗药物抗体,进而引发加速血液清除现象,导致疗效随给药次数衰减。此外,反复输注LNP还可能增加补体激活相关假性过敏反应(complement activation-related pseudoallergy, CARPA)等免疫原性风险。为克服上述局限,当前研究正积极探索新型低免疫原性脂质材料及给药策略的优化。另一方面,也有研究致力于在非病毒系统中实现基因的持久表达,如Lubelski团队开发的NCtx递送系统通过共转运DNA与mRNA,实现稳定表达CAR-T细胞的体内生成,为临床转化提供了新的技术支持[17]。
2.1.3 in vivo CAR-T的特点与临床研究进展
与传统ex vivo CAR-T相比,in vivo CAR-T在制备流程、临床应用及安全性特征上存在显著差异。
传统ex vivo CAR-T疗法需从患者体内采集外周血单个核细胞(peripheral blood mononuclear cell, PBMC),随后在实验室通过电穿孔或病毒载体介导将CAR基因导入T细胞,并经数周体外扩增培养后回输至患者体内。相比之下,in vivo CAR-T将基因修饰过程转移至体内,通过直接静脉输注载体实现T细胞的原位重编程,流程的简化及工业化生产潜力有望大幅降低成本并缩短治疗等待时间,从而实现更快速、更广泛的应用[13]。从机制上看,in vivo CAR-T可能因转导与扩增动力学差异而呈现出与传统ex vivo CAR-T不同的炎症反应谱。然而,现阶段临床样本量有限,且递送平台、剂量策略及适应证差异显著,其总体CRS与ICANS风险是否低于ex vivo CAR-T仍有待验证。此外,系统性递送方式还引入了载体整合突变风险、脱靶转导及重复给药相关免疫原性等新的安全性变量,需通过规范化检测与长期随访予以评估。
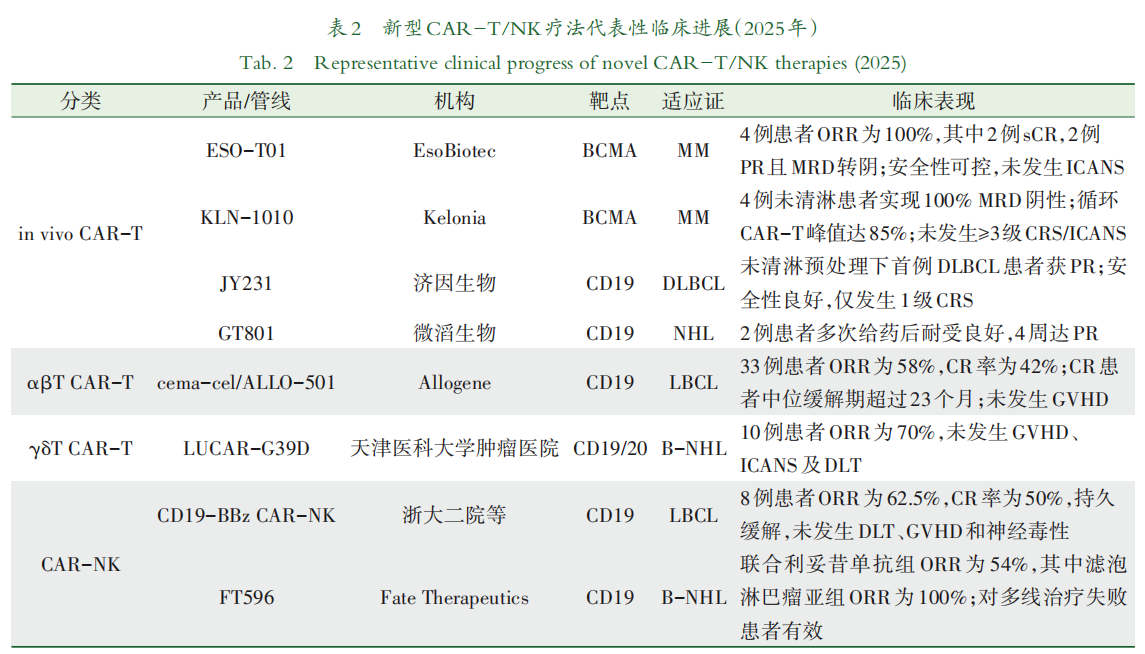
in vivo CAR-T在血液肿瘤领域已取得多项进展,多项试验数据初步证实了该策略的可行性与安全性。其中,EsoBiotec公司开发的基于慢病毒载体的ESO-T01疗法(靶向BCMA)在The Lancet上发表的研究数据引人注目。该研究是一项针对4例复发/难治性多发性骨髓瘤(multiple myeloma, MM)患者的开放标签、剂量递增Ⅰ期试验,患者接受单次静脉输注ESO-T01后,截至2025年4月1日的2~3个月随访期内,客观缓解率(objective response rate, ORR)达到100%,其中2例达到严格完全缓解(stringent complete remission, sCR),另2例达到部分缓解(partial response, PR)且MRD转阴。所有患者均观察到可控的急性炎症反应,尽管有3例患者发生了≥3级CRS,但均得到有效控制,且未观察到ICANS或其他严重的肝毒性反应。该研究有力地证明了慢病毒载体in vivo CAR-T在血液肿瘤中具有巨大的治疗潜力[18]。
Kelonia公司在2025年美国血液学会(American Society of Hematology, ASH)年会上汇报了in vivo BCMA CAR-T (KLN-1010)的Ⅰ期数据。4例患者在未接受清淋预处理的情况下均实现100% MRD阴性,循环CAR-T细胞峰值占比达85%,且在最长5个月的随访期内持续缓解,未见≥3级CRS或ICANS,初步证实了该方案的高效性与安全性[19]。
济因生物开发的靶向CD19的in vivo CAR-T疗法(JY231)也展现出令人振奋的初步成果。公开数据显示,1例复发/难治性弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma, DLBCL)患者在未进行传统淋巴细胞清除预处理的情况下,仅接受单次静脉输注后,于第35天达到PR,随访期间仅观察到1级CRS,未出现ICANS或感染,显示出良好的安全性[20]。这一案例首次提供了in vivo CAR-T在DLBCL中产生缓解的临床证据,其良好的安全性为后续更大规模的临床试验奠定了基础。
GT801是一款基于LNP-mRNA的抗CD19 CAR-T细胞治疗产品。在2025年ASH年会上,微滔生物汇报了其研究数据。临床前研究显示,GT801具有高度特异性。在人源化小鼠模型中,单次低剂量给药即可诱导>95%的B细胞清除及超过30倍的CAR-T体内扩增,表现出持久的CAR表达与强效抗肿瘤活性。此外,其安全性良好,支持重复给药[21]。目前,GT801相关临床试验正在进行中,截至2025年11月30日,2例非霍奇金淋巴瘤患者分别完成了3次(0.5 mg/次)及4次(1.5 mg/次)给药,受试者临床表现总体耐受性良好,并在给药4周后达到PR。
此外,多款创新管线已正式进入临床阶段。Interius BioTherapeutics的INT2104作为首个进入临床的CD20靶向in vivo CAR-T疗法,利用工程化慢病毒载体直接转导T细胞与NK细胞,已于2024年推进至Ⅰ期临床阶段,旨在评估其在B细胞恶性肿瘤中的安全性及药代动力学特征[22]。Umoja Biopharma启动了抗CD19的UB-VV111的Ⅰ期试验,该疗法基于VivoVec平台,整合了雷帕霉素激活细胞因子受体(rapamycin-activated cytokine receptor, RACR)系统,旨在通过口服雷帕霉素类似物实现体内CAR-T细胞的可控扩增与干性维持,从而解决体内原位生成细胞数量不足及持久性差的难题[23]。在自身免疫性疾病治疗领域,基于mRNA-LNP的in vivo CAR-T(HN2301)取得了全球首个体内试验的重大突破,验证了其在系统性红斑狼疮(systemic lupus erythematosus, SLE)患者中的安全性与初步有效性[24]。
in vivo CAR-T通过在体内原位递送遗传信息实现T细胞重编程,显著简化了传统CAR-T的复杂制备流程,有望降低生产成本并提升治疗可及性。当前主要技术路线以病毒载体和纳米递送平台为核心,已在血液肿瘤领域获得初步临床验证。尽管在递送精准性、表达可控性及长期安全性等方面仍面临挑战,但in vivo CAR-T正逐步走向临床落地,被认为是CAR-T领域最具潜力的发展方向之一。
2.2 通用型CAR-T
通用型CAR-T,又称同种异体CAR-T。其利用健康供者的T细胞,经基因编辑与标准化工程改造,制备成可大规模生产、质检并冻存的“现货”(off-the-shelf)产品,可实现解冻后直接输注使用,从而显著缩短治疗窗口期[34]。此外,工业化规模生产大幅降低了成本;源自健康供者的细胞通常具备更优的增殖活性与抗肿瘤潜能,且产品批次间一致性高,为自身T细胞耗竭或扩增失败的患者提供了可行的治疗选择[25, 27]。
2.2.1 核心免疫学挑战:GVHD与宿主排斥
异体CAR-T疗法的临床转化核心在于克服供受体间的双向免疫排斥:一方面,供体T细胞可通过内源性TCR攻击患者健康组织,引发GVHD,这是主要的致死性安全风险[26-27];另一方面,宿主残留的T细胞与NK细胞会识别并清除异体细胞[即宿主抗移植物反应(host versus graft reaction, HVGR)],导致通用型产品在体内的存续时间显著短于自体产品,从而削弱长期疗效[25, 28]。为解决上述免疫学挑战,目前的应对策略主要集中在基因编辑技术的应用上:(1)为预防GVHD,可通过锌指核酸酶(zinc finger nuclease, ZFN)、转录激活因子样效应物核酸酶(transcription activator-like effector nuclease, TALEN)或CRISPR/Cas9等基因编辑工具特异性敲除编码TCR α链或β链的基因[29-32]。TCR的缺失使供体T细胞无法识别人类白细胞抗原(human leukocyte antigen, HLA)分子,可有效预防GVHD的发生,早期临床试验已证实该策略的有效性[25]。(2)为逃避宿主排斥,需通过基因编辑改造HLA表达,如敲除β2-微球蛋白(β2-microglobulin, β2M)基因以阻止HLA-Ⅰ类分子在CAR-T细胞表面表达,从而躲避宿主CD8+ T细胞攻击。但HLA-Ⅰ类分子缺失会激活宿主NK细胞识别机制,导致CAR-T被NK细胞清除[28, 33]。因此,研究者提出,在敲除β2M的同时强制表达非经典抑制性HLA分子(如HLA-E或HLA-G),以实现对T细胞和NK细胞的双重免疫逃逸[36]。此外,敲除CIITA基因可阻止HLA-Ⅱ类分子表达,从而规避宿主CD4+ T细胞的攻击,进一步增强免疫豁免性[32]。(3)除改造常规αβT细胞外,研究人员也在探索其他天然具有低同种异体反应性的替代细胞来源,如γδT细胞、NK细胞、诱导多能干细胞(induced pluripotent stem cell, iPSC)来源的T/NK细胞。
2.2.2 αβT CAR-T
以健康供者的αβT细胞为起始材料,通过基因编辑实现通用化的CAR-T产品是该领域的重要技术路线之一。该路线的优势在于αβT细胞作为CAR载体的生物学基础最为明确,其信号放大能力和抗肿瘤效应已在自体CAR-T中得到充分验证[37]。然而,多重基因编辑显著增加了工艺复杂度,也对生产一致性、基因组安全性及长期毒性提出了更高要求。
目前,αβT CAR-T疗法已在全球范围内进入活跃的临床开发阶段,展现出令人振奋的前景。Cellectis公司开发的UCART19(靶向CD19)是首个进入临床试验的产品。早期研究证实了其在复发/难治性急性淋巴细胞白血病(acute lymphoblastic leukemia, ALL)患者中的可行性和初步疗效,且GVHD发生率极低[35]。2025年,ALPHA/ALPHA2研究报告了靶向CD19的αβT CAR-T(cema-cel/ALLO-501)治疗33例复发/难治性大B细胞淋巴瘤(large B-cell lymphoma, LBCL)患者的数据,结果显示ORR达58%,完全缓解(complete response, CR)率达42%,CR患者中位缓解期长达23.1个月;未发生GVHD、ICANS或≥3级CRS,证实了现货型CAR-T在联合ALLO-647清淋方案后,可实现持久且安全的临床获益[38]。
2.2.3 γδT CAR-T
与依赖MHC/HLA分子识别抗原的αβT细胞不同,γδT细胞主要通过其自身TCR及NKG2D等天然受体识别肿瘤细胞或受感染细胞表面因应激而上调的配体(如MICA/B、ULBPs)。这种MHC非限制性的识别模式使其在异体输注时几乎不产生GVHD风险,因而具备内在的安全性优势[39, 41]。尽管γδT细胞在外周血中含量稀少(占1%~5%),给大规模制备带来挑战,但研究已证实通过特定的体外扩增技术可有效富集并活化这些细胞,以满足临床需求[43]。临床前及早期临床研究数据表明,γδT CAR-T细胞不仅在血液肿瘤中展现出强大的杀伤活性,更因其独特的肿瘤浸润能力和对实体瘤微环境的适应性,在治疗胰腺癌、胶质母细胞瘤等实体瘤方面显示出巨大潜力,且通常伴随较低的CRS和神经毒性风险[42]。
LUCAR-G39D是全球首个靶向CD19/CD20双靶点的同种异体γδT CAR-T细胞疗法,用于治疗复发/难治性B细胞非霍奇金淋巴瘤(B-cell non-hodgkin lymphoma, B-NHL)。在2025年ASH年会上,天津医科大学肿瘤医院张会来教授团队口头报告了LUCAR-G39D Ⅰ期研究成果。数据显示,在10例可评估患者中,ORR达70%,预估6个月无进展生存(progression-free survival, PFS)率为75%,且多数患者体内检测到细胞扩增;安全性方面,未发生GVHD、ICANS及剂量限制性毒性(dose-limiting toxicity, DLT)。这一中国原创成果有力证实了双靶点异体γδT CAR-T的安全性与持久疗效,为临床患者提供了即时可用的新选择[40]。
此外,2025年欧洲肿瘤内科学会(European Society for Medical Oncology, ESMO)大会公布了一项抗CD38 γδT CAR-T细胞治疗MM的临床前突破。研究显示,该疗法利用γδT细胞低表达CD38的特性有效规避了自杀伤,且在冷冻复苏后及抗CD38药物(如达雷妥尤单抗)存在下仍保持强效活性,体内外实验均证实其能显著抑制肿瘤生长,展现了其作为“现货型”产品与标准抗体药物联合应用的广阔前景[44]。
通用型CAR-T细胞疗法通过基因编辑技术成功攻克了GVHD这一关键安全壁垒,为实现CAR-T细胞治疗的“现货化”和临床普及奠定了基础。目前,临床研究的核心挑战已转向如何延长通用型CAR-T细胞在体内的持久性,以实现与自体CAR-T相当的长期疗效。随着基因编辑策略的持续优化、新型清淋方案的应用及iPSC等创新细胞来源技术的发展,通用型CAR-T疗法有望在不久的将来彻底改变细胞免疫治疗的格局,为更多肿瘤患者带来希望[33]。
2.3 CAR-NK
CAR-NK疗法是通过基因工程将特异性识别肿瘤抗原的CAR分子表达于NK细胞表面,从而引导并增强其对肿瘤的靶向杀伤能力[47]。作为通用型细胞治疗的另一关键技术路线,CAR-NK凭借其独特的免疫生物学特性展现出差异化的临床优势。与CAR-T相比,NK细胞的杀伤活性不依赖MHC,在异体应用中几乎不引发GVHD。同时,由于其独特的细胞因子分泌谱(以IFN-γ等为主),显著降低了诱发严重CRS和ICANS的风险[45-46]。基于其良好的安全性,CAR-NK适合制备成“现货型”产品,可有效缩短患者等待时间并降低生产成本[48]。此外,CAR-NK细胞除通过表面CAR结构域特异性锚定肿瘤抗原(如CD19)外,还完整保留了其固有的非MHC限制性天然细胞毒性,从而为抗肿瘤治疗提供了双重作用机制[46,49]。
2.3.1 主要技术路线与细胞来源
根据细胞来源的差异,CAR-NK疗法主要分为外周血NK细胞(peripheral blood NK cell, PB-NK)、脐带血NK细胞(umbilical cord blood NK cell, UCB-NK)、NK细胞系(如NK-92)及诱导多能干细胞来源的NK细胞(iPSC-NK)4条技术路线。其中,PB-NK可从自体或异体供体外周血中分离,来源便捷,但受限于单次采集数量低、供体间异质性显著及体外扩增与基因修饰效率不稳定[48]。UCB-NK则利用脐带血这一丰富的同种异体来源,该来源的细胞状态更为“原始”,增殖能力和抗肿瘤活性更强。脐带血作为成熟的临床资源,其安全性已得到广泛验证,是当前临床研究中最常用的来源之一[48,50]。NK-92细胞系具备无限增殖能力且易于基因改造,可实现高度均质化、标准化生产,但因其为恶性来源,使用前必须进行辐照处理以防止成瘤风险,这在一定程度上限制了其在体内的存续时间与长期疗效[51-52]。iPSC-NK作为极具前景的新兴策略,不仅能通过单克隆扩增实现规模化生产,还支持在分化前进行多重基因编辑(如整合IL-15或敲除CISH),为开发功能一致且活性增强的下一代CAR-NK产品提供了理想平台[53]。
2.3.2 临床研究进展与展望
CAR-NK疗法已在临床研究中展现出显著成果,尤其是在安全性和初步疗效方面。CD19-BBz CAR-NK是一种来源于脐带血、具有4-1BB共刺激结构域的CD19特异性CAR-NK疗法,其临床前试验及治疗复发/难治性LBCL的Ⅰ期临床试验结果发表于2025年5月的Nature Cancer。该疗法在小鼠模型中具有持久的存续能力和显著的抗肿瘤活性,在Ⅰ期剂量递增试验中达到预设的安全性和可行性终点,且诱导了患者的持久缓解,8例患者的ORR为62.5%,其中4例患者(50%)达到CR。治疗过程中未观察到DLT、CRS、ICANS及GVHD,表明该疗法具有良好的安全性,为B细胞淋巴瘤患者提供了一种有潜力的通用型免疫治疗新选择[54]。
Fate Therapeutics公司是iPSC-NK领域的领导者,其开发的FT596是一款经过多重工程修饰、由iPSC衍生的CD19导向CAR-NK疗法。2025年公布的其在BCL中的Ⅰ期临床试验(NCT04245722)结果显示,86例经多线治疗(含38%的既往CAR-T治疗失败患者)的复发/难治性BCL患者中,FT596作为单药或与利妥昔单抗联合使用均表现出良好的安全性,未达到最大耐受剂量,未报道ICANS,CRS发生率低且均≤2级。联合治疗组CR率为37%,PR率为18%。在特定亚组中,如滤泡性淋巴瘤亚组ORR达100%[55]。该疗法在难治人群中诱导了深度且持久的缓解,有力验证了iPSC平台在克服传统细胞疗法制造与成本瓶颈、实现标准化现货供应方面的巨大潜力。此外,CAR-NK疗法在SLE治疗中也取得重大研究进展。
尽管前景广阔,CAR-NK疗法仍面临诸多挑战,其中最主要的问题在于如何提升其在体内的持久性。与能够长期存活的CAR-T细胞不同,CAR-NK细胞的寿命相对较短,这限制了其抗肿瘤作用的持续时间。目前,研究人员正通过共表达IL-15、优化淋巴细胞清除方案及探索多次输注等策略,以期延长其在体内的存活与功能时间[53]。
CAR-NK疗法凭借其独特的安全性和“现货型”制备优势,正在重塑细胞免疫治疗的临床格局。以iPSC为代表的制备技术正逐步解决细胞来源的异质性难题,结合基因编辑对细胞功能的深度改造,该疗法有望克服持久性瓶颈,发展成为一种能够广泛覆盖血液及实体肿瘤、兼具高效性与高可及性的标准化治疗手段。
3 讨论
CAR-T细胞疗法已在血液系统恶性肿瘤中取得显著研究进展,并在多项适应证中获批临床应用,但其进一步普及仍受制于制造流程的复杂性及毒性的可控性。目前,细胞免疫治疗的发展重点正从单纯追求缓解率转向对可及性、可控性与可规模化生产的综合优化。尽管新型CAR-T技术在降低制备难度、缩短患者等待时间和提高安全性方面展现出优势,其成熟应用仍受若干关键问题制约。
对于通用型产品,其临床疗效上限在很大程度上受制于细胞的体内持久性。通过敲除TCR降低GVHD风险的策略已较为明确,但宿主免疫清除所导致的CAR-T细胞存留时间短暂仍是制约疗效的普遍难题。未来的解决策略需要在多维度寻求平衡,如在敲除HLA的同时引入过表达CD47或HLA-E等免疫逃逸模块,以拮抗巨噬细胞和内源性NK细胞的识别;或将长效细胞因子(如IL-15)的自分泌功能与优化的非清淋预处理方案深度融合,以重塑宿主免疫微环境[56]。同时,多重基因编辑所带来的基因组不稳定性亦不容忽视,需建立更为严格的质量控制与长期随访框架[57]。
in vivo CAR-T疗法的临床转化核心在于构建高效且具备细胞类型特异性的基因递送系统。目前两大主流平台在机制上展现出不同的优势、局限及优化方向。整合型病毒载体(如慢病毒)的优势在于单次给药即可实现CAR基因在内源性T细胞上的稳定整合与长效表达。然而,其安全性挑战主要源于给药时非目标细胞的脱靶转导及半随机整合伴随的插入突变风险。针对上述问题,现阶段的优化策略集中于引入细胞特异性配体、组织/细胞特异性启动子及可控表达元件,以实现精准递送和安全可控的表达[58]。相比之下,以LNP-mRNA为代表的非病毒平台凭借瞬时表达特性与无基因组整合风险,展现出更优的安全性窗口,但其短板在于抗原暴露时间短,临床需采取重复给药策略,这可能诱导机体产生针对脂质组分的抗药物抗体,引发加速血液清除现象,并增加CARPA等输注反应风险。突破此局限需向新型低免疫原性脂质材料更迭,或结合分层剂量方案以弥补持久性不足[58]。
以血液系统恶性肿瘤为例,传统自体CAR-T虽已报道较高的ORR,但CAR-T细胞在体内呈急剧的指数级扩增,常伴随高比例的3级及以上CRS及ICANS风险。相比之下,通用型CAR-T产品在实现较高ORR的同时,能够在一定程度上规避GVHD及严重神经毒性的发生,展现出更宽泛的安全窗口。与此同时,in vivo CAR-T虽在早期临床试验中显示出良好的安全性并可诱导部分缓解,但其达到深度CR的比例及疾病复发的长期随访结果仍需进一步的样本验证。上述体内命运与动力学的异质性,本质上决定了不同新兴平台在各类疾病模型中的应用潜力。针对实体瘤微环境,鉴于其物理屏障与高度免疫抑制状态,细胞移植物的长效存续及多靶点逻辑门控设计成为克服抗原异质性与免疫细胞耗竭的关键要求。此外,CAR-NK及部分通用型细胞疗法在自身免疫疾病中的探索提示其应用边界正在拓展,亦需建立与肿瘤治疗不同的疗效终点与风险评估体系[59-60]。
未来,CAR-T疗法的演进趋势可能集中于底层可控性基因工程的深化、载体递送平台的多样化适配及高通量动态监测体系的融合应用。该领域的实质性突破有赖于分子生物学技术创新与临床精细化分层管理的深度协同,以期在疗效、安全性与可及性之间实现更优的整体平衡。
[1] June C H, O′Connor R S, Kawalekar O U, et al. CAR T cell immunotherapy for human cancer [J]. Science, 2018, 359(6382): 1361-1365. DOI: 10.1126/science.aar6711.
[2] Maus M V, Alexander S, Bishop M R, et al. Society for Immunotherapy of Cancer (SITC) clinical practice guideline on immune effector cell-related adverse events [J]. J Immunother Cancer, 2020, 8(2): e001511. DOI: 10.1136/jitc-2020-001511.
[3] Rafiq S, Hackett C S, Brentjens R J. Engineering strategies to overcome the current roadblocks in CAR T cell therapy [J]. Nat Rev Clin Oncol, 2020, 17(3): 147-167. DOI: 10.1038/s41571-019-0297-y.
[4] June C H, Sadelain M. Chimeric antigen receptor therapy [J]. N Engl J Med, 2018, 379(1): 64-73. DOI: 10.1056/NEJMra1706169.
[5] Jayaraman J, Mellody M P, Hou A J, et al. CAR-T design: elements and their synergistic function [J]. EBioMedicine, 2020, 58: 102931. DOI: 10.1016/j.ebiom.2020.102931.
[6] Cook M S, King E, Flaherty K R, et al. CAR-T cells containing CD28 versus 4-1BB co-stimulatory domains show distinct metabolic profiles in patients [J]. Cell Rep, 2025, 44(7): 115973. DOI: 10.1016/j.celrep.2025.115973.
[7] Benmebarek M R, Karches C H, Cadilha B L, et al. Killing mechanisms of chimeric antigen receptor (CAR) T cells [J]. Int J Mol Sci, 2019, 20(6):1283. DOI: 10.3390/ijms20061283.
[8] Hay K A, Hanafi L A, Li D, et al. Kinetics and biomarkers of severe cytokine release syndrome after CD19 chimeric antigen receptor-modified T-cell therapy [J]. Blood, 2017, 130(21): 2295-2306. DOI: 10.1182/blood-2017-06-793141.
[9] Gust J, Hay K A, Hanafi L A, et al. Endothelial activation and blood-brain barrier disruption in neurotoxicity after adoptive immunotherapy with CD19 CAR-T cells [J]. Cancer Discov, 2017, 7(12): 1404-1419. DOI: 10.1158/2159-8290.CD-17-0698.
[10] Neelapu S S, Tummala S, Kebriaei P, et al. Chimeric antigen receptor T-cell therapy-assessment and management of toxicities [J]. Nat Rev Clin Oncol, 2018, 15(1): 47-62. DOI:10.1038/nrclinonc.2017.148.
[11] Cappell K M, Kochenderfer J N. Long-term outcomes following CAR T cell therapy: what we know so far [J]. Nat Rev Clin Oncol, 2023, 20(6): 359-371. DOI: 10.1038/s41571-023-00754-1.
[12] Pfeiffer A, Thalheimer F B, Hartmann S, et al. In vivo generation of human CD19-CAR T cells results in B-cell depletion and signs of cytokine release syndrome [J]. EMBO Mol Med, 2018, 10(11): e9158. DOI: 10.15252/emmm.201809158.
[13] Rurik J G, TombáCz I, Yadegari A, et al. CAR T cells produced in vivo to treat cardiac injury [J]. Science, 2022, 375(6576): 91-96. DOI: 10.1126/science.abm0594.
[14] Smith T T, Stephan S B, Moffett H F, et al. In situ programming of leukaemia-specific T cells using synthetic DNA nanocarriers [J]. Nat Nanotechnol, 2017, 12(8): 813-820. DOI:10.1038/nnano.2017.57.
[15] Xu J, Liu L, Parone P, et al. In-vivo B-cell maturation antigen CAR T-cell therapy for relapsed or refractory multiple myeloma [J]. Lancet, 2025, 406(10500): 228-231. DOI: 10.1016/S0140-6736(25)01030-X.
[16] Nicolai C J, Parker M H, Qin J, et al. In vivo CAR T-cell generation in nonhuman primates using lentiviral vectors displaying a multidomain fusion ligand [J]. Blood, 2024, 144(9): 977-987. DOI: 10.1182/blood.2024024523.
[17] Bimbo J F, Van Diest E, Murphy D E, et al. T cell-specific non-viral DNA delivery and in vivo CAR-T generation using targeted lipid nanoparticles [J]. J Immunother Cancer, 2025, 13(7): e011759. DOI: 10.1136/jitc-2025-011759.
[18] Xu J, Liu L, Parone P, et al. In-vivo B-cell maturation antigen CAR T-cell therapy for relapsed or refractory multiple myeloma [J]. Lancet, 2025, 406(10500): 228-231. DOI:10.1016/S0140-6736(25)01030-X.
[19] Harrison S, Ho P J, Lim S, et al. Minimal residual disease (MRD)-negative outcomes following a novel, in vivo gene therapy generating anti-B-cell maturation antigen (BCMA) chimeric antigen receptor (CAR)-T cells in patients with relapsed and refractory multiple myeloma (RRMM): preliminary results from inMMyCAR, the first-inhuman phase 1 study of KLN-1010 [J]. Blood, 2025, 146(Suppl 2): LBA-1.
[20] Chen X F, Huang K, Liu J Y, et al. 1482 In-vivo CAR-T cells produced by specific virus in refractory B cell lymphoma [J]. J Immunother Cancer, 2024, 12(Suppl 3): A1684-A1736. DOI:10.1136/jitc-2024-sitc2024.1482.
[21] Sun J W, Zhu X, Xu Z, et al. Precision in vivo CAR-T generation via CLAMP-enabled mRNA delivery: toward scalable and translatable cell therapy [J]. Blood, 2025, 146: 103. DOI:10.1182/blood-2025-103.
[22] A study to investigate safety of INT2104 infusions in participants aged 18 years of age and older who have b-cell cancers that came back after previous treatment (INVISE)[EB/OL]. (2026-02-04) [2026-03-05]. https://clinicaltrials.gov/study/NCT06539338.
[23] Garcia J R. A phase I, multicenter, open-label study of UB-VV111 in combination with rapamycin in relapsed/refractory CD19+ B-cell malignancies [C/OL]//ASCO, 2025: TPS2681. https://www.asco.org/abstracts-presentations/252262/abstract. DOI: 10.1200/JCO.2025.43.16_suppl.TPS2681.
[24] Wang Q, Xiao Z X, Zheng X, et al. In vivo CD19 CAR T-cell therapy for refractory systemic lupus erythematosus [J]. N Engl J Med, 2025, 393(15): 1542-1544. DOI: 10.1056/NEJMc2509522.
[25] Zhao J, Lin Q, Song Y, et al. Universal CARs, universal T cells, and universal CAR T cells [J]. J Hematol Oncol, 2018, 11(1): 132. DOI: 10.1186/s13045-018-0677-2.
[26] Jiang N, Yang Z, Miao H, et al. Recent advances in universal chimeric antigen receptor T cell therapy [J]. J Hematol Oncol, 2025, 18(1): 82. DOI: 10.1186/s13045-025-01737-8.
[27] Lu Q Z, Yang D H, Li H X, et al. Delivery of CD47-SIRPα checkpoint blocker by BCMA-directed UCAR-T cells enhances antitumor efficacy in multiple myeloma [J]. Cancer Lett, 2024, 585: 216660. DOI: 10.1016/j.canlet.2024.216660.
[28] Lei J, Ni Z, Zhang R. Universal CAR-T cell therapy for cancer treatment: advances and challenges [J]. Oncol Res, 2025, 33(11): 3347-3373. DOI: 10.32604/or.2025.067445.
[29] Torikai H, Reik A, Liu P Q, et al. A foundation for universal T-cell based immunotherapy: T cells engineered to express a CD19-specific chimeric-antigen-receptor and eliminate expression of endogenous TCR [J]. Blood, 2012, 119(24): 5697-5705. DOI: 10.1182/blood-2012-01-405365.
[30] Qasim W, Zhan H, Samarasinghe S, et al. Molecular remission of infant B-ALL after infusion of universal TALEN gene-edited CAR T cells [J]. Sci Transl Med, 2017, 9(374): eaaj2013. DOI: 10.1126/scitranslmed.aaj2013.
[31] Eyquem J, Mansilla-Soto J, Giavridis T, et al. Targeting a CAR to the TRAC locus with CRISPR/Cas9 enhances tumour rejection [J]. Nature, 2017, 543(7643): 113-117. DOI:10.1038/nature21405.
[32] Ren J T, Liu X J, Fang C Y, et al. Multiplex genome editing to generate universal CAR T cells resistant to PD1 inhibition [J]. Clin Cancer Res, 2017, 23(9): 2255-2266. DOI: 10.1158/1078-0432.CCR-16-1300.
[33] 齐文昕, 张伟龙, 景红梅. 肿瘤免疫疗法中细胞来源对治疗效果的影响[J]. 中华血液学杂志, 2024, 45(7): 699-704. DOI: 10.3760/cma.j.cn121090-20240321-00104.
[34] Depil S, Duchateau P, Grupp S A, et al. ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges [J]. Nat Rev Drug Discov, 2020, 19(3): 185-199. DOI: 10.1038/s41573-019-0051-2.
[35] Qasim W, Amrolia P J, Samarasinghe S, et al. First clinical application of talen engineered universal CAR19 T cells in B-ALL [J]. Blood, 2015, 126(23): 2046. DOI: 10.1182/blood.V126.23.2046.2046.
[36] Gornalusse G G, Hirata R K, Funk S E, et al. HLA-E-expressing pluripotent stem cells escape allogeneic responses and lysis by NK cells [J]. Nat Biotechnol, 2017, 35(8): 765-772. DOI: 10.1038/nbt.3860.
[37] Depil S, Duchateau P, Grupp S A, et al. ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges [J]. Nat Rev Drug Discov, 2020, 19(3): 185-199. DOI: 10.1038/s41573-019-0051-2.
[38] Locke F L, Munoz J L, Tees M T, et al. Allogeneic chimeric antigen receptor T-cell products cemacabtagene ansegedleucel/ALLO-501 in relapsed/refractory large B-cell lymphoma: phase I experience from the ALPHA2/ALPHA clinical studies [J]. J Clin Oncol, 2025, 43(14): 1695-1705. DOI: 10.1200/JCO-24-01933.
[39] Wang C Q, Lim P Y, Tan A H. Gamma/delta T cells as cellular vehicles for anti-tumor immunity [J]. Front Immunol, 2024, 14: 1282758. DOI: 10.3389/fimmu.2023.1282758.
[40] Yu J W, Cao L L, Li L F, et al. A phase 1 study of lucar-G39D: a novel anti-CD20/CD19 dual-CAR allogeneic gamma delta T cells in adults with relapsed/refractory B-cell non-Hodgkin lymphoma (NHL) [J]. Blood, 2025, 146 (Supplement 1): 266-267. DOI: 10.1182/blood-2025-266.
[41] Rozenbaum M, Meir A, Aharony Y, et al. Gamma-delta CAR-T cells show CAR-directed and independent activity against leukemia[J]. Front Immunol, 2020, 11: 1347. DOI: 10.3389/fimmu.2020.01347.
[42] Li C, Zhou F, Wang J, et al. Novel CD19-specific γ/δ TCR-T cells in relapsed or refractory diffuse large B-cell lymphoma [J]. J Hematol Oncol, 2023, 16(1): 5. DOI: 10.1186/s13045-023-01402-y.
[43] Makkouk A, Yang X C, Barca T, et al. Off-the-shelf Vδ1 gamma delta T cells engineered with glypican-3 (GPC-3)-specific chimeric antigen receptor (CAR) and soluble IL-15 display robust antitumor efficacy against hepatocellular carcinoma [J]. J Immunother Cancer, 2021, 9(12): e003441. DOI: 10.1136/jitc-2021-003441.
[44] Hattori Y, Ohshima N, Taniguchi Y, et al. Development of anti-CD38-CAR allogeneic γδt cells as an off-the-shelf use for myeloma [J]. ESMO Open, 2025, 10(suppl 2): 104179. DOI:10.1016/j.esmoop.2025.104179.
[45] Peng L, Sferruzza G, Yang L J, et al. CAR-T and CAR-NK as cellular cancer immunotherapy for solid tumors [J]. Cell Mol Immunol, 2024, 21(10): 1089-1108. DOI: 10.1038/s41423-024-01207-0.
[46] Pan K, Farrukh H, Chittepu V C S R, et al. CAR race to cancer immunotherapy: from CAR T, CAR NK to CAR macrophage therapy [J]. J Exp Clin Cancer Res, 2022, 41(1): 119. DOI: 10.1186/s13046-022-02327-z.
[47] Xie G Z, Dong H, Liang Y, et al. CAR-NK cells: a promising cellular immunotherapy for cancer [J]. EBioMedicine, 2020, 59: 102975. DOI: 10.1016/j.ebiom.2020.102975.
[48] Lin X T, Sun Y, Dong X, et al. IPSC-derived CAR-NK cells for cancer immunotherapy [J]. Biomed Pharmacother, 2023, 165: 115123. DOI: 10.1016/j.biopha.2023.115123.
[49] Zhang L, Meng Y, Feng X, et al. CAR-NK cells for cancer immunotherapy: from bench to bedside [J]. Biomark Res, 2022, 10(1):12. DOI: 10.1186/s40364-022-00364-6.
[50] Li T, Niu M, Zhang W, et al. CAR-NK cells for cancer immunotherapy: recent advances and future directions [J]. Front Immunol, 2024, 15: 1361194. DOI: 10.3389/fimmu.2024. 1361194.
[51] Klingemann H, Boissel L, Toneguzzo F. Natural killer cells for immunotherapy-advantages of the NK-92 cell line over blood NK cells[J]. Front Immunol, 2016, 7: 91. DOI: 10.3389/fimmu.2016.00091.
[52] Zhang C, Oberoi P, Oelsner S, et al. Chimeric antigen receptor-engineered NK-92 cells: an off-the-shelf cellular therapeutic for targeted elimination of cancer cells and induction of protective antitumor immunity [J]. Front Immunol, 2017, 8: 533. DOI: 10.3389/fimmu.2017.00533.
[53] Gong Y, Klein Wolterink R G J, Wang J, et al. Chimeric antigen receptor natural killer (CAR-NK) cell design and engineering for cancer therapy [J]. J Hematol Oncol, 2021, 14(1): 73. DOI: 10.1186/s13045-021-01083-5.
[54] Lei W, Liu H, Deng W H, et al. Safety and feasibility of 4-1BB co-stimulated CD19-specific CAR-NK cell therapy in refractory/relapsed large B cell lymphoma: a phase 1 trial [J]. Nat Cancer, 2025, 6(5): 786-800. DOI: 10.1038/s43018-025-00940-3.
[55] Ghobadi A, Bachanova V, Patel K, et al. Induced pluripotent stem-cell-derived CD19-directed chimeric antigen receptor natural killer cells in B-cell lymphoma: a phase 1, first-in-human trial [J]. Lancet, 2025, 405(10473): 127-136. DOI:10.1016/S0140-6736(24)02462-0.
[56] Liu E, Tong Y, Dotti G, et al. Cord blood NK cells engineered to express IL-15 and a CD19-targeted CAR show long-term persistence and potent antitumor activity [J]. Leukemia, 2018, 32(2): 520-531. DOI: 10.1038/leu.2017.226.
[57] Stadtmauer E A, Fraietta J A, Davis M M, et al. CRISPR-engineered T cells in patients with refractory cancer [J]. Science, 2020, 367(6481): eaba7365. DOI: 10.1126/science.aba7365.
[58] Billingsley M M, Singh N, Ravikumar P, et al. Ionizable lipid nanoparticle-mediated mRNA delivery for human CAR T cell engineering [J]. Nano Lett, 2020, 20(3): 1578-1589. DOI:10.1021/acs.nanolett.9b04246.
[59] Labanieh L, Mackall C L. CAR immune cells: design principles, resistance and the next generation [J]. Nature, 2023, 614(7949): 635-648. DOI: 10.1038/s41586-023-05707-3.
[60] MüLler F, Taubmann J, Bucci L, et al. CD19 CAR T-cell therapy in autoimmune disease-a case series with follow-up [J]. N Engl J Med, 2024, 390(8): 687-700. DOI: 10.1056/NEJMoa2308917.
《肿瘤药学》是由湖南省卫生健康委员会主管,湖南省肿瘤医院(中南大学湘雅医学院附属肿瘤医院)主办的我国唯一一本肿瘤领域对接药学领域的核心期刊,是中国抗癌协会系列期刊。自2016年已连续10年入选《中国科技核心期刊》目录。目前已被美国《化学文摘》、荷兰《医学文摘》、波兰《哥白尼索引》、美国《乌利希期刊指南》、中国生物医学文摘数据库、知网、万方、维普等数据库收录。经携手合作与共同努力,本刊正式入选“中国科技期刊卓越行动计划(二期)”集群(集团)化试点项目,并成功立项“湖南省培育世界一流湘版科技期刊建设工程项目”。
网站链接:www.zgzlyx.com
工作邮箱:zgzlyx2011@163.com
电话号码:0731-89762609
来源:肿瘤药学杂志