王赢宣, 彭智
北京大学肿瘤医院消化肿瘤内科, 北京 100142
通信作者:彭智,Email:zhipeng@bjmu.edu.cn.
作者简介

彭 智
主任医师、教授、博士生导师
北京大学肿瘤医院主任医师,北京大学博雅青年学者
国家级青年人才项目获得者
中国抗癌协会胃癌专委会委员
中国抗癌协会肿瘤转移专委会委员
中国抗癌协会肿瘤精准治疗委员会委员
CSCO胃癌专家委员会委员兼秘书
CSCO肿瘤营养治疗专家委员会委员
中国免疫学会临床免疫分会委员
北京癌症防治学会胃癌防治专委会主任委员
《中华医学杂志》和《肿瘤综合治疗电子杂志》编委
在BMJ、Lancet和JAMA Oncology发表多篇论著,改变了多项胃癌诊治指南。获得中华医学会医学科学技术奖一等奖、中国抗癌协会青年科学家奖和中国抗癌协会科技奖一等奖等
据2022年全球癌症数据统计,全球胃癌新发96.8万例,死亡66万例,发病率和死亡率均居恶性肿瘤第5位[1]。中国是胃癌高发国家,2022年新发35.9万例,死亡26.0万例[2],分别占全球的37%和39%,发病率和死亡率在国内恶性肿瘤中居第5位和第3位,疾病负担极为沉重。随着分子病理检测的普及,人类表皮生长因子受体2(human epidermal growth factor receptor 2, HER2)扩增、错配修复缺陷/微卫星不稳定性高(deficient mismatch repair/high microsatellite instability, dMMR/MSI-H)、Epstein-Barr病毒(Epstein-Barr virus, EBV)感染和紧密连接蛋白18.2(claudin 18.2, CLDN18.2)高表达等分子亚型不断被识别,为胃癌精准治疗奠定基础。
三大指南在诊疗原则上总体一致,但在具体策略、药物选择和证据分级方面存在差异。比较三大指南有助于:(1)把握不同地区胃癌诊疗特色;(2)为临床提供多维度参考;(3)促进个体化精准治疗。本文将围绕分子检测策略、围手术期治疗和晚期治疗,对CSCO胃癌诊疗指南(2025版)[3]、NCCN胃癌指南(Version 1.2026)[4]和ESMO胃癌在线指南(Living Guideline,Version 1.4;2024年9月更新)[5]进行对比分析。
1 分子检测策略
分子检测是胃癌精准治疗的基础。三大指南均建议在拟接受系统治疗的晚期胃癌患者中检测HER2、错配修复蛋白/微卫星不稳定性(mismatch repair/microsatellite instability, MMR/MSI)、程序性死亡配体1(programmed death-ligand 1, PD-L1)和CLDN18.2。其在检测路径和罕见靶点筛查的覆盖范围等方面有不同侧重点。
HER2是最早被证实有效的靶点。三大指南均推荐所有晚期或转移性胃癌患者进行HER2检测。传统分类采用二分法:HER2阳性[免疫组织化学(immunohistochemistry, IHC)3+或IHC 2+/荧光原位杂交技术(fluorescence in situ hybridization, FISH)+]患者可在曲妥珠单抗治疗中获益。随着抗体偶联药物(antibody-drug conjugate, ADC)在HER2中低表达胃癌人群中取得突破性疗效,传统的HER2表达“阳性/阴性”二分法已无法满足临床需求。基于德曲妥珠单抗(trastuzumab deruxtecan, T-DXd)相关的DESTINY-Gastric系列与中国桥接研究[6]和维迪西妥单抗(RC48)相关的C008研究[7]等的结果,2025版CSCO指南创新性地确立了HER2表达的“四分类法”:高表达(IHC 3+或IHC 2+/FISH+)、中表达(IHC 2+/FISH-)、低表达(IHC 1+)和不表达(IHC 0)。该分类可用于识别和关注HER2中表达人群等潜在获益者。
基于GLOW[8]和SPOTLIGHT[9]等研究结果,CLDN18.2已被三大指南纳入HER2阴性晚期或转移性胃癌的一线分层标志物。CSCO指南将CLDN18.2检测推荐等级提升至Ⅰ级,建议采用IHC,阈值参考临床试验证实的标准化方案。NCCN明确以“≥75%活性肿瘤细胞2+/3+膜染色”为阳性标准。ESMO指南同样建议在HER2阴性的晚期或转移性胃癌患者中检测CLDN18.2表达以筛选佐妥昔单抗治疗获益人群。
免疫治疗相关标志物方面,dMMR/MSI-H是预测胃癌患者能否从免疫检查点抑制剂治疗中获益的强效预测生物标志物。三大指南均推荐所有胃癌患者评估MMR/MSI。
PD-L1表达是预测晚期胃癌免疫治疗获益的重要生物标志物。三大指南均推荐采用IHC检测程序性死亡受体-1(programmed death-1, PD-1)/PD-L1表达情况,并主要采用联合阳性评分(combined positive score, CPS)作为评估标准。CPS=PD-L1阳性的肿瘤细胞、淋巴细胞和巨噬细胞数量之和/活性肿瘤细胞总数×100。NCCN认为CPS和肿瘤区域阳性评分(tumor area positivity, TAP)具有很高的一致性,两者可能可以互换使用。
CSCO指南将神经营养性酪氨酸受体激酶基因(neurotrophic tyrosine receptor kinase gene, NTRK)融合、成纤维细胞生长因子受体2b(fibroblast growth factor receptor 2b, FGFR2b)和间质-上皮转化因子(mesenchymal-epithelial transition factor, MET)等检测列为Ⅲ级推荐,主要用于针对标准治疗失败患者寻找潜在的治疗靶点和筛选相关的临床研究,EBV状态检测主要用于分子分型。NCCN指南倾向于以二代测序(next generation sequencing, NGS)一次性覆盖NTRK融合、转染重排基因(rearranged during transfection, RET)融合和B-Raf原癌基因丝氨酸/苏氨酸蛋白激酶(B-Raf proto oncogene serine/threonine protein kinase, BRAF)V600E突变等基因检测,但成本较高,在注释中强调如果肿瘤的形态中存在明显的淋巴样组织结构,应考虑进行EBV检测。ESMO指南仅在拟入组临床试验、穷尽标准治疗或已上市相关靶向药的地区推荐进行罕见靶点检测,避免过度筛查。
比较三大指南推荐的生物标志物检测显示(表 1):总体上,CSCO指南建立了覆盖较全的靶点检测体系,强调从一线到后线的全程管理;NCCN指南以治疗决策为导向,倡导在关键标志物基础上联合NGS;ESMO指南更注重资源效率,仅特定情境下推荐检测。
表1 最新CSCO、NCCN和ESMO胃癌指南中生物标志物检测推荐对比

2 围手术期治疗
三大指南关于围手术期治疗的适应证的界定略有不同。NCCN指南推荐对cT2期及以上或N+期可切除胃癌患者行围手术期化疗,ESMO指南推荐对于≥cⅠB期(即cT2N0M0期或cT1N1M0期)胃癌患者行围手术期化疗,而CSCO指南推荐对Ⅱ~Ⅲ期局部进展期胃癌患者行围手术期治疗。
在围手术期化疗方案选择方面,三大指南均以含氟尿嘧啶和铂类的联合方案为基础。NCCN指南将FLOT(氟尿嘧啶+亚叶酸钙+奥沙利铂+多西他赛)作为能够耐受三药联合化疗的胃癌患者的标准围手术期方案。FLOT4研究显示,与ECF/ECX(表柔比星+顺铂+氟尿嘧啶/卡培他滨)比较,围手术期FLOT化疗显著改善胃癌患者总生存期(overall survival, OS)并提高R0切除率[10]。而双药化疗可用于不适合三药方案的胃癌患者。CSCO指南将SOX方案(替吉奥+奥沙利铂)作为中国可切除局部进展期胃癌的标准治疗方案。RESOLVE研究显示,与术后XELOX(卡培他滨+奥沙利铂)辅助化疗比较,围手术期SOX方案显著改善中国可切除局部进展期胃癌患者的3年无瘤生存(disease-free survival, DFS)率(59.4% vs 51.1%,HR=0.77)[11]。CSCO指南亦将FLOT和DOS(多西他赛+奥沙利铂+替吉奥)方案作为Ⅰ级推荐(1B类证据)用于体能状态良好、可耐受三药化疗的可切除局部进展期胃癌患者,但需加强毒性监测。
围手术期免疫治疗方面,MATTERHORN研究显示,FLOT化疗进一步联合度伐利尤单抗可提高可切除胃癌患者的病理完全缓解(pathological complete response, pCR)率(19% vs 7%)并使无事件生存期(event-free survival, EFS)改善(HR=0.71,P < 0.001)[12]。基于该研究结果,NCCN指南已将“FLOT+度伐利尤单抗”正式纳入围手术期治疗推荐方案,适用于PD-L1 CPS≥1或TAP≥1%的可切除胃癌患者。CSCO和ESMO指南目前尚未作出围手术期免疫治疗推荐。对于dMMR/MSI-H特殊亚型胃癌的围手术期治疗,CSCO指南提出新辅助可考虑PD-1单抗联合细胞毒性T淋巴细胞相关抗原4(cytotoxic T-lymphocyte-associated protein 4,CTLA-4)单抗或PD-1单抗联合化疗;NCCN指南指出dMMR/MSI-H特殊亚型胃癌的围手术期可考虑免疫治疗,可选方案包括多塔利单抗(仅限术前新辅助)、纳武利尤单抗+伊匹木单抗后序贯纳武利尤单抗、帕博利珠单抗单药和曲美木单抗+度伐利尤单抗(仅限术前新辅助)。
在胃癌根治术后辅助治疗方面,如术前治疗评估有效且术后可耐受,三大指南建议继续完成围手术期系统治疗;未接受术前系统治疗的患者,三大指南推荐采用以氟尿嘧啶联合铂类为基础的术后辅助化疗方案。CSCO指南依据术后病理分期进一步细化推荐:对于D2切除且达到R0的Ⅱ~Ⅲ期患者,SOX方案为Ⅰ级推荐,XELOX等方案列为Ⅱ级推荐,FOLFOX(氟尿嘧啶+亚叶酸钙+奥沙利铂)方案为Ⅲ级推荐;部分低风险Ⅱ期患者可考虑替吉奥单药。ESMO指南指出MSI-H胃癌患者通常不从辅助化疗中获益,不建议常规给予术后辅助化疗。
3 转化治疗
4 晚期治疗
4.1 晚期胃癌一线治疗
4.1.1 HER2阳性(高表达)
HER2阳性(IHC 3+或IHC 2+/FISH+)约占晚期胃癌的15%。三大指南均根据PD-L1 CPS进一步分层。若PD-L1 CPS≥1时,推荐帕博利珠单抗+曲妥珠单抗+含铂-氟尿嘧啶化疗。本推荐基于KEYNOTE-811研究结果,CPS≥1亚组中,帕博利珠单抗+曲妥珠单抗+含铂-氟尿嘧啶化疗较曲妥珠单抗+化疗中位PFS延长(10.9个月 vs 7.3个月,HR=0.72),客观缓解率(objective response rate, ORR)提高(73.2% vs 58.4%),中位OS亦有改善;CPS < 1亚组未见获益,推荐曲妥珠单抗+化疗方案[13]。
4.1.2 HER2阴性(中低或不表达)
对于HER2阴性且错配修复正常/微卫星稳定(proficient mismatch repair/microsatellite stable, pMMR/MSS)晚期胃癌患者,三大指南均基于PD-L1 CPS评分对免疫联合化疗进行分层推荐。国际指南均认为,PD-L1 CPS≥1人群可考虑联合免疫治疗,其中CPS≥5的人群获益更为明确。CheckMate 649研究显示,纳武利尤单抗联合化疗在CPS≥5的晚期胃癌患者人群中显著改善中位OS(14.4个月 vs 11.1个月,HR=0.71)[14]。KEYNOTE-859研究结果提示,帕博利珠单抗联合化疗在CPS≥10的人群中获益最明显(中位OS 15.7个月 vs 11.8个月,HR=0.65)[15]。基于RATIONALE-305Ⅲ期研究证据[16],NCCN指南也将替雷利珠单抗纳入晚期胃癌患者的免疫治疗选择。CSCO指南除纳武利尤单抗和帕博利珠单抗外,将信迪利单抗、替雷利珠单抗和舒格利单抗等多款国产PD-1/PD-L1单抗均列为晚期胃癌一线治疗的Ⅰ级推荐,PD-L1阈值依各Ⅲ期研究入组标准设定,如ORIENT-16研究[17]采用CPS≥5和RATIONALE-305研究[16]采用TAP≥5%等(表 2)。此外,CSCO指南纳入PD-1/CTLA-4双抗卡度尼利联合XELOX方案,该推荐不考虑PD-L1表达状态。基于COMPASSION-15研究证据,该方案可显著延长全人群中位OS(14.1个月 vs 11.1个月,HR=0.66),且在PD-L1低表达亚组(CPS < 5)中获益一致(13.7个月 vs 11.4个月,HR=0.75)[18]。CSCO指南构建出较国际指南更为多元且覆盖范围更广的晚期胃癌免疫治疗体系。
表2 最新CSCO、NCCN和ESMO胃癌指南中pMMR/MSS胃癌免疫治疗药物汇总

针对CLDN18.2阳性(IHC 2-3+且≥75%肿瘤细胞)的HER2阴性晚期胃癌人群,基于两项全球Ⅲ期研究SPOTLIGHT与GLOW的结果[8-9],三大指南一致推荐佐妥昔单抗联合化疗。其中,SPOTLIGHT研究显示,全球人群中位OS达18.2个月,中位PFS为10.6个月[9];GLOW研究中,全球人群中位OS为14.4个月[8];两项研究中,佐妥昔单抗联合化疗均显著优于化疗。中国患者亚组分析显示获益趋势与全球一致[19]。
总体而言,三大指南在HER2阴性胃癌一线治疗的核心策略上具有一致性,即以含氟尿嘧啶和铂类的双药化疗为基础,并在此框架内根据分子标志物加以免疫或靶向治疗。
4.1.3 dMMR/MSI-H患者
dMMR/MSI-H约占晚期胃癌的6%,对化疗不敏感,对免疫治疗高度敏感。NCCN指南将帕博利珠单抗单药、多塔利单抗单药、纳武利尤单抗联合伊匹木单抗和帕博利珠单抗或纳武利尤单抗联合含铂-氟嘧啶方案列为晚期dMMR/MSI-H人群的一线治疗首选方案。ESMO指南认可PD-1单抗单药显著获益,但认为单药与联合化疗孰优尚不明确,因此强调个体化决策:若症状负担重或重要脏器受累、需快速缓解,可在起始阶段采用PD-1单抗联合化疗。CSCO指南推荐首选纳武利尤单抗联合伊匹木单抗,可考虑帕博利珠单抗单药,免疫联合化疗及其他国产免疫检查点抑制剂列为Ⅲ级推荐,仅在免疫药物可及性受限或免疫检查点抑制剂治疗禁忌时考虑单纯化疗。
4.1.4 特殊临床亚型
产甲胎蛋白胃癌(alpha-fetoprotein-producing gastric cancer, AFPGC)在胃癌中约占3%,侵袭性高,易肝和淋巴结转移。一项中国Ⅱ期研究显示,SOX方案联合卡瑞利珠单抗/阿帕替尼治疗的AFPGC患者ORR可达55.6%,12个月PFS率和OS率分别为42.1%和63.7%[20]。因此,CSCO指南将该亚型单独列出,一线SOX方案联合卡瑞利珠单抗/阿帕替尼给出Ⅱ级推荐。NCCN与ESMO指南目前未对AFPGC给出独立治疗策略。
4.1.5 胃癌伴腹膜转移
针对胃癌腹膜转移,CSCO指南根据腹腔脱落细胞学与腹膜种植情况将患者分为仅有细胞学阳性(CY1P0)、仅有肉眼腹膜转移(CY0P1)或两者均存在(CY1P1),推荐系统化疗联合腹腔化疗。DRAGON-01研究显示,S-1+紫杉醇静脉及腹腔灌注紫杉醇可改善CY0P1患者OS[21]。CY1P0患者若经转化治疗转为CY0且无远处转移,可行根治性手术。NCCN指南对“仅腹膜转移”患者,建议系统治疗后复评若腹膜癌指数(peritoneal cancer index, PCI)低、疾病稳定/改善、无腹膜外转移且预计可完全细胞减灭者,经MDT可考虑胃切除+细胞减灭术±腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy, HIPEC)/腹腔化疗;若PCI较高、疾病进展或预计难以完全减灭,以系统治疗为主。ESMO指南对胃癌伴腹膜转移无特殊建议。
4.2 晚期胃癌二线及后线治疗
4.2.1 HER2阳性(高表达)
在HER2阳性晚期胃癌的二线治疗中,国际指南已形成以ADC为核心的共识。NCCN与ESMO指南均不推荐曲妥珠单抗跨线使用,并基于DESTINY-Gastric02研究(ORR 41.8%,中位PFS 5.6个月,中位OS 12.1个月)[22],将T-DXd作为二线及后线主要推荐,强调在治疗前尽可能进行再活检以确认HER2状态。CSCO指南出于可及性和证据成熟度考虑,尚未将其列入二线标准,更鼓励患者进入相关临床研究;对未在一线使用曲妥珠单抗而铂类失败的HER2阳性患者,可考虑曲妥珠单抗联合紫杉醇。
DESTINY-Gastric01研究显示,在二线及以上治疗失败且接受过曲妥珠单抗的HER2阳性晚期胃癌患者中,T-DXd优于化疗(ORR:51% vs 14%;中位OS:12.5个月 vs 8.4个月,HR=0.59)[6]。中国桥接研究DESTINY-Gastric06进一步验证了其在亚洲人群中的疗效[23]。CSCO指南因此将T-DXd纳入三线首选推荐。C008研究表明,国产HER2-ADC RC48治疗的患者ORR达24.4%,IHC 2+与IHC 3+均可获益[7]。CSCO指南同样将RC48列为三线的首选推荐。
4.2.2 HER2阴性(中低或不表达)
对HER2阴性的晚期胃癌患者,三大指南均将雷莫西尤单抗联合紫杉醇作为优选二线方案。RAINBOW研究显示,该组合显著延长晚期胃癌患者的中位OS(9.6个月 vs 7.4个月)[24]。RAINBOW-Asia研究在亚洲人群中验证了该结果[25]。单药化疗(紫杉类或伊立替康)为可考虑方案。基于REGARD研究[26],对于不适合化疗的患者,NCCN与ESMO指南均将雷莫芦单抗单药列为可考虑方案。CSCO指南额外可考虑呋喹替尼联合紫杉醇(1B类)。FRUTIGA研究显示,呋喹替尼联合紫杉醇治疗晚期胃癌患者较紫杉醇单药中位PFS延长(5.6个月 vs 2.7个月),ORR提高(42.5% vs 22.4%),OS有延长的趋势,但差异无统计学意义(P=0.606)[27]。一线免疫联合化疗失败后的二线治疗模式正在探索。Ⅰ/Ⅱ期研究AK109-201显示,卡度尼利单抗联合普洛西单抗(pulocimab)和紫杉醇可延长OS和PFS[28],但目前三大指南均未常规推荐。
在HER2阴性晚期胃癌三线治疗中,CSCO指南按HER2高、中、低和不表达分层管理,与NCCN和ESMO指南的“阳性/阴性”二分法不同。在HER2低/不表达人群中,CSCO指南推荐阿帕替尼,Ⅲ期研究证实其显著改善中位PFS(2.6个月 vs 1.8个月)并提高疾病控制率(42.0% vs 8.8%)[29];纳武利尤单抗可用于既往未接受免疫治疗的患者。在HER2中表达(IHC 2+/FISH-)人群中推荐使用RC48,为CSCO指南独有。NCCN与ESMO指南不单独划分HER2中表达亚组,三线主要采用紫杉类、伊立替康、TAS-102或最佳支持治疗。
4.2.3 dMMR/MSI-H人群
对于dMMR/MSI-H晚期胃癌,若患者既往未接受免疫检查点抑制剂,三大指南均将免疫治疗列为二线核心策略。ESMO指南推荐帕博利珠单抗。NCCN指南扩展至帕博利珠单抗、多塔利单抗及纳武利尤单抗联合伊匹木单抗。CSCO指南则将帕博利珠单抗、恩沃利单抗、替雷利珠单抗和斯鲁利单抗均列为Ⅰ级推荐(2A类),其中恩沃利单抗、替雷利珠单抗和斯鲁利单抗的推荐分别源于包含胃癌队列的国产Ⅱ期研究,ORR约为44.4%、55.5%和39.7%[30-32]。一线已接受免疫治疗的患者应根据HER2状态选择相应方案。
4.2.4 特殊靶点的治疗
5 总结与展望
总体来看,胃癌已迈入分子分型指导下的精准治疗时代。HER2、PD-L1、MMR/MSI与CLDN18.2的检测构成治疗决策的基础框架。三大指南在关键生物标志物和含铂-氟嘧啶化疗骨架方面达成高度共识,并普遍认可免疫治疗和新型靶向药物在晚期胃癌中的地位。然而,由于药物可及性、人群差异、医疗资源配置和本土循证证据的不同,各指南在分子检测深度、围手术期方案、转化治疗策略以及免疫治疗与靶向治疗体系上仍呈现区域特征(表 1~3)。
表3 最新CSCO、NCCN和ESMO胃癌指南中pMMR/MSS胃癌治疗关键差异分析
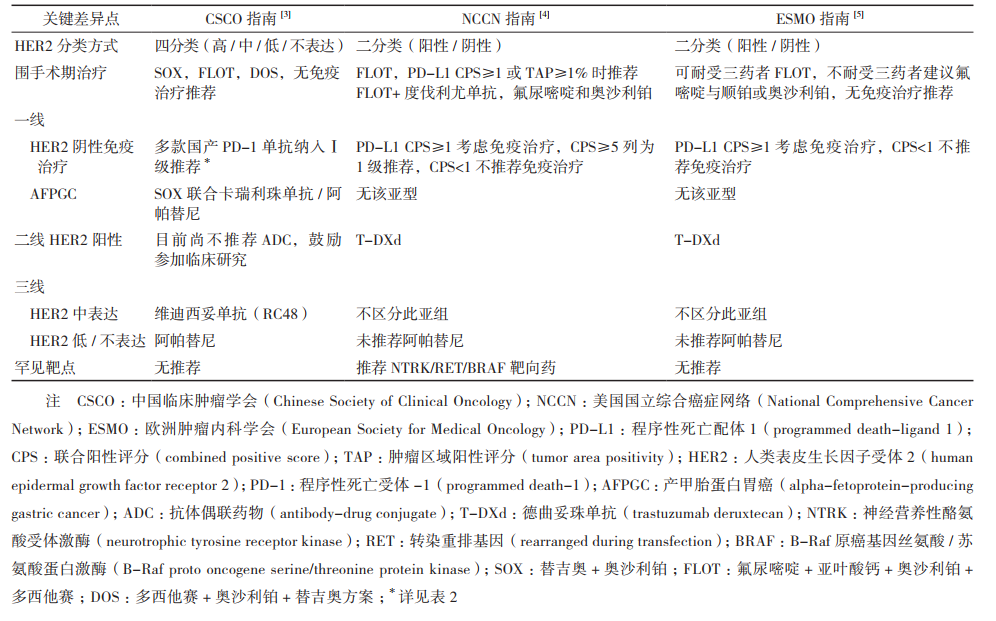
CSCO指南立足中国国情,在吸收国际循证证据的基础上,充分纳入本土临床试验结果,并考虑药物可及性和经济负担,形成具有中国特色的诊疗路径。免疫治疗和ADC靶向治疗时代,国产PD-1抑制剂和本土ADC药物适应证的获批,为中国患者提供更多可行选择。临床实践中,医生既应掌握三大指南的共识内容,也应理解不同推荐背后的证据基础和适用边界,在MDT框架下结合患者具体情况进行个体化决策。
参考文献
[1] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024, 74(3): 229-263.
[2] Han BF, Zheng RS, Zeng HM, et al. Cancer incidence and mortality in China, 2022[J]. J Natl Cancer Cent, 2024, 4(1): 47-53.
[3] 中国临床肿瘤学会胃癌专家委员会. 中国临床肿瘤学会(CSCO)胃癌诊疗指南[M]. 2025版. 北京: 人民卫生出版社, 2025.
[4] National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology: gastric cancer (version 1.2026)[EB/OL]. (2025-12-12)[2025-12-28]. https://www.nccn.org/professionals/physician_gls/pdf/gastric.pdf.
[5] European Society for Medical Oncology. ESMO living guideline: gastric cancer[EB/OL]. (2024-09)[2025-12-28]. https://www.esmo.org/guidelines/living-guidelines/esmo-living-guideline-gastric-cancer.
[6] Shitara K, Bang YJ, Iwasa S, et al. Trastuzumab deruxtecan in previously treated HER2-positive gastric cancer[J]. N Engl J Med, 2020, 382(25): 2419-2430.
[7] Peng Z, Liu TS, Wei J, et al. Efficacy and safety of a novel anti-HER2 therapeutic antibody RC48 in patients with HER2-overexpressing, locally advanced or metastatic gastric or gastroesophageal junction cancer: a single-arm phase Ⅱ study[J]. Cancer Commun, 2021, 41(11): 1173-1182.
[8] Shah MA, Shitara K, Ajani JA, et al. Zolbetuximab plus CAPOX in CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: the randomized, phase 3 GLOW trial[J]. Nat Med, 2023, 29(8): 2133-2141.
[9] Shitara K, Lordick F, Bang YJ, et al. Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT): a multicentre, randomised, double-blind, phase 3 trial[J]. Lancet, 2023, 401(10389): 1655-1668.
[10] Al-Batran SE, Homann N, Pauligk C, et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomised, phase 2/3 trial[J]. Lancet, 2019, 393(10184): 1948-1957.
[11] Zhang XT, Liang H, Li ZY, et al. Perioperative or postoperative adjuvant oxaliplatin with S-1 versus adjuvant oxaliplatin with capecitabine in patients with locally advanced gastric or gastro-oesophageal junction adenocarcinoma undergoing D2 gastrectomy (RESOLVE): final report of a randomised, open-label, phase 3 trial[J]. Lancet Oncol, 2025, 26(3): 312-319.
[12] Janjigian YY, Al-Batran SE, Wainberg ZA, et al. Event-free survival (EFS) in MATTERHORN: A randomized, phase 3 study of durvalumab plus 5-fluorouracil, leucovorin, oxaliplatin and docetaxel chemotherapy (FLOT) in resectable gastric/gastroesophageal junction cancer (GC/GEJC)[J]. J Clin Oncol, 2025, 43(17_suppl): LBA5.
[13] Janjigian YY, Kawazoe A, Bai YX, et al. Pembrolizumab plus trastuzumab and chemotherapy for HER2-positive gastric or gastro-oesophageal junction adenocarcinoma: interim analyses from the phase 3 KEYNOTE-811 randomised placebo-controlled trial[J]. Lancet, 2023, 402(10418): 2197-2208.
[14] Janjigian YY, Shitara K, Moehler M, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial[J]. Lancet, 2021, 398(10294): 27-40.
[15] Rha SY, Oh DY, Yañez P, et al. Pembrolizumab plus chemotherapy versus placebo plus chemotherapy for HER2-negative advanced gastric cancer (KEYNOTE-859): a multicentre, randomised, double-blind, phase 3 trial[J]. Lancet Oncol, 2023, 24(11): 1181-1195.
[16] Qiu MZ, Oh DY, Kato K, et al. Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first line treatment for advanced gastric or gastro-oesophageal junction adenocarcinoma: RATIONALE-305 randomised, double blind, phase 3 trial[J]. BMJ, 2024, 385: e078876.
[17] Xu JM, Jiang HP, Pan YY, et al. Sintilimab plus chemotherapy for unresectable gastric or gastroesophageal junction cancer: the ORIENT-16 randomized clinical trial[J]. JAMA, 2023, 330(21): 2064-2074.
[18] Shen L, Zhang YQ, Li ZY, et al. First-line cadonilimab plus chemotherapy in HER2-negative advanced gastric or gastroesophageal junction adenocarcinoma: a randomized, double-blind, phase 3 trial[J]. Nat Med, 2025, 31(4): 1163-1170.
[19] Astellas Pharma. China's National Medical Products Administration approves zolbetuximab for first-line treatment of advanced gastric or gastroesophageal junction adenocarcinoma[EB/OL]. (2025-01-05)[2025-12-28]. https://www.prnewswire.com/news-releases/chinas-national-medical-products-administration-nmpa-approves-vyloy-zolbetuximab-for-first-line-treatment-of-advanced-gastric-or-gastroesophageal-junction-adenocarcinoma-302342446.html
[20] Wang YK, Lu JL, Chong XY, et al. PD-1 antibody camrelizumab plus apatinib and SOX as first-line treatment in patients with AFP-producing gastric or gastro-esophageal junction adenocarcinoma (CAP 06): a multi-center, single-arm, phase 2 trial[J]. Signal Transduct Target Ther, 2025, 10(1): 100.
[21] Yan C, Yang Z, Shi Z, et al. Intraperitoneal and intravenous paclitaxel plus S-1 vs intravenous paclitaxel plus S-1 in gastric cancer patients with peritoneal metastasis: results from the multicenter, randomized, phase 3 DRAGON-01 trial[C]//2024 ASCO Gastrointestinal Cancers Symposium. Alexandria: ASCO, 2024: G125.
[22] Van Cutsem E, di Bartolomeo M, Smyth E, et al. Trastuzumab deruxtecan in patients in the USA and Europe with HER2-positive advanced gastric or gastroesophageal junction cancer with disease progression on or after a trastuzumab-containing regimen (DESTINY-Gastric02): primary and updated analyses from a single-arm, phase 2 study[J]. Lancet Oncol, 2023, 24(7): 744-756.
[23] Peng Z, Chen P, Lu J, et al. Trastuzumab deruxtecan in patients from China with previously treated human epidermal growth factor receptor 2-positive locally advanced/metastatic gastric or gastroesophageal junction adenocarcinoma (DESTINY-Gastric06): results from a single-arm, multicenter, phase 2 trial[J]. EClinicalMedicine, 2025, 87: 103404.
[24] Wilke H, Muro K, Van Cutsem E, et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomised phase 3 trial[J]. Lancet Oncol, 2014, 15(11): 1224-1235.
[25] Xu RH, Zhang YQ, Pan HM, et al. Efficacy and safety of weekly paclitaxel with or without ramucirumab as second-line therapy for the treatment of advanced gastric or gastroesophageal junction adenocarcinoma (RAINBOW-Asia): a randomised, multicentre, double-blind, phase 3 trial[J]. Lancet Gastroenterol Hepatol, 2021, 6(12): 1015-1024.
[26] Fuchs CS, Tomasek J, Yong CJ, et al. Ramucirumab monotherapy for previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (REGARD): an international, randomised, multicentre, placebo-controlled, phase 3 trial[J]. Lancet, 2014, 383(9911): 31-39.
[27] Wang F, Shen L, Guo WJ, et al. Fruquintinib plus paclitaxel versus placebo plus paclitaxel for gastric or gastroesophageal junction adenocarcinoma: the randomized phase 3 FRUTIGA trial[J]. Nat Med, 2024, 30(8): 2189-2198.
[28] Zhang XT, Wang YK, Xiang XJ, et al. Efficacy and safety of cadonilimab in combination with pulocimab and paclitaxel as second-line therapy in patients with advanced gastric or gastroesophageal junction (G/GEJ) cancer who failed immunochemotherapy: a multicenter, double-blind, randomized trial[J]. J Clin Oncol, 2024, 42(16_suppl): 4012.
[29] Li J, Qin SK, Xu JM, et al. Randomized, double-blind, placebo-controlled phase Ⅲ trial of apatinib in patients with chemotherapy-refractory advanced or metastatic adenocarcinoma of the stomach or gastroesophageal junction[J]. J Clin Oncol, 2016, 34(13): 1448-1454.
[30] Shen L, Li J, Deng Y, et al. Envafolimab (KN035) in advanced tumors with mismatch-repair deficiency[J]. J Clin Oncol, 2020, 38(15_suppl): 3021.
[31] Li J, Xu Y, Zang AM, et al. Tislelizumab in previously treated, locally advanced unresectable/metastatic microsatellite instability-high/mismatch repair-deficient solid tumors[J]. Chin J Cancer Res, 2024, 36(3): 257-269.
[32] Qin SK, Li J, Zhong HJ, et al. Serplulimab, a novel anti-PD-1 antibody, in patients with microsatellite instability-high solid tumours: an open-label, single-arm, multicentre, phase Ⅱ trial[J]. Br J Cancer, 2022, 127(12): 2241-2248.
来源:实用肿瘤杂志