2026年4月15日,中山大学肿瘤防治中心徐淼教授团队,联合新加坡基因组研究所刘建军教授、中科院动物研究所翟巍巍教授、哥伦比亚大学刘中华教授在国际顶级期刊《自然》(Nature)上发表了题为《EBV毒株与宿主HLA互作驱动鼻咽癌发病风险》的研究成果。该研究首次揭示,鼻咽癌的高发并非由高危EB病毒或宿主遗传背景单一因素决定,而是两者“里应外合”协同作用的结果——特定宿主基因型与高危EB病毒亚型互作,使发病风险飙升17倍,从病毒-宿主互作的全新角度,解开了华南地区鼻咽癌高发的“地域魔咒”。

论文要点速览:
高发之谜:为什么EB病毒几乎人人感染,鼻咽癌却在华南等少数地区高发?这一现象长期困扰科学界。
两条线索:围绕鼻咽癌高发,过去的研究逐渐积累出两条重要线索:一条指向高危EB病毒亚型,另一条指向宿主遗传易感性。
新的推进:最新研究揭示,真正关键的,或许不是单独看病毒或宿主哪一方更“危险”,而是二者相遇时如何互作,并由此决定宿主免疫系统能否有效识别和控制高危病毒。
风险组合:风险最高的,并不是单独携带高危EB病毒,或单独具有某种易感背景,而是高危EB病毒与特定宿主HLA背景形成了高风险组合。
免疫机制:这种风险差异的背后,是一个具体的免疫学机制:宿主能否有效呈递病毒抗原,并激活特异T细胞识别和控制高危EB病毒感染细胞。
区域格局:华南高发并非由单一因素造成,而是高危EB病毒在当地富集、与之发生关键互作的宿主HLA背景也在当地富集,二者共同塑造了华南鼻咽癌的高风险格局。
防控意义:这项研究的意义,不只是解释鼻咽癌为何高发于华南,更在于进一步回答了“哪些宿主对高危EB病毒致癌更易感”以及“何种生物学过程是控制EB病毒致癌的关键”,为高危人群识别、早诊早治和疫苗研发提供了更清晰的方向。
谜题:鼻咽癌为何“青睐”华南?
鼻咽癌是极具地域特征的恶性肿瘤。华南地区仅占全球2%人口,却负担超过40%的全球新发病例。这一“地域魔咒”困扰科学界已久。
EB病毒是鼻咽癌的重要致病因素。在高发地区,几乎所有鼻咽癌肿瘤组织均为EB病毒阳性,并持续表达病毒编码的蛋白或RNA。那么,鼻咽癌在华南地区高发,究竟是因为华南人群存在遗传易感背景,还是当地流行着更高危的EB病毒亚型?
为了寻找鼻咽癌高发的病因,中肿团队于2002年和2010年在《自然·遗传学》(Nature Genetics)上发表两项研究成果,分别鉴定出鼻咽癌家系和散发人群的基因易感位点,从遗传学角度阐明了鼻咽癌发病因素。然而,一个长期未解的关键问题是:既往发现的遗传易感因素和环境暴露因素,通常仅增加鼻咽癌发病风险1-3倍,仍不足以解释华南地区的聚集性高发。与此同时,EB病毒虽是鼻咽癌发生发展的核心病因,但是全球人群普遍感染,而鼻咽癌却只在特定地区高发。这一“广泛感染”与“局部高发”之间的矛盾,提示在遗传和环境之外,可能还存在尚未被识别的关键致病因素,也由此引出了一个重要科学问题:在鼻咽癌高发区,是否存在特异EB病毒亚型,从而导致鼻咽癌的发生?
破局:锁定高危病毒,却非唯一答案
围绕这一问题,徐淼团队联合新加坡基因组研究所刘建军、中科院动物研究所翟巍巍、哥伦比亚大学刘中华和福建医科大学叶为民等团队,开展了持续近十年的系统合作研究。
2019年,研究团队率先鉴定出鼻咽癌致瘤高危EB病毒亚型BALF2-CCT,成果发表在《自然·遗传学》杂志。该亚型是目前已知最强鼻咽癌风险因素,可增加约7倍的发病风险。更为重要的是,其地理分布与鼻咽癌发病格局高度一致:华南地区携带率高达35-40%,而北方地区不到5%,欧美几乎没有。该发现揭示了高危EB病毒感染是华南地区鼻咽癌高发的主要驱动因素,从病毒层面解释了“EB病毒普遍感染、鼻咽癌局部高发”的关键悖论。
然而,高危病毒虽在华南人群中广泛传播,却仅有少数感染者最终进展为鼻咽癌,提示高危EB病毒本身并不足以决定发病,其致癌效应可能取决于特定宿主遗传背景。然而,宿主与病毒风险因素如何协同致癌长期不清楚。基于上述发现,研究进一步提出本领域另一个亟待突破的核心科学问题:高危EB病毒究竟更易导致哪些宿主发病?决定其致癌易感性的宿主—病毒互作机制是什么?
解密:病毒与宿主“里应外合”,风险飙升17倍
这一问题是疾病相关宿主-病原互作研究中极具挑战性的关键问题。研究不仅需要配对的宿主-EB病毒基因组信息,更要从约3Gb的人类基因组与170kb的 EB病毒全基因组的大规模变异组合中,识别真正具有致病意义的互作位点。
研究团队利用先进的广义线性混合模型,创新性地建立宿主-EB病毒双基因组互作分步扫描的分析框架,突破了病毒和宿主复杂遗传结构混杂和双基因组高维扫描带来的方法学瓶颈,最终鉴定出决定鼻咽癌易感性的核心高危EB病毒-宿主HLA基因互作对,并在分子水平进一步解析其作用机制。
研究发现,鼻咽癌发病风险由HLA-A等位基因和高危EB病毒的85841位点A>G 变异互作共同决定,并非由宿主或病毒亚型单一因素决定。在功能层面,该高危EB病毒变异通过改变EBNA3B抗原表位(VVI表位第9位氨基酸Q>R),决定其能否被HLA-A*11:01有效呈递,并直接影响CD8 T细胞对高危EB病毒感染细胞的识别和杀伤效率。
通俗地说,HLA-A*11:01就像一把“钥匙”,能帮助免疫系统识别被病毒感染的细胞;高危EB病毒则像一把“变形的锁”,只有特定钥匙才能打开;当“变形的锁”遇到“不匹配的钥匙”,免疫系统就无法识别并清除感染细胞。
这一“病毒-宿主”互作效应,导致感染高危病毒且缺失A*11:01的“双重风险因素携带者”,其鼻咽癌发病风险比基线提高约17倍,远大于单一高危病毒或遗传风险的简单加和。
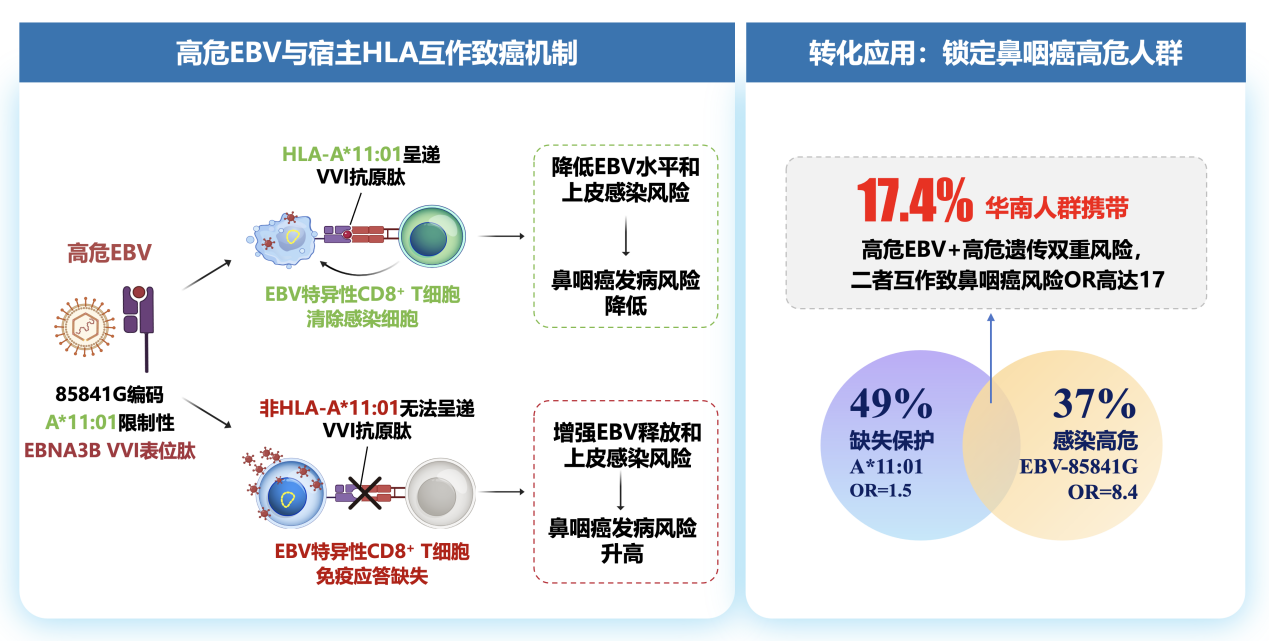
该研究回答了“高危病毒-宿主互作决定发病风险的机制是什么”以及“什么样的宿主感染高危病毒后更易发病”,为高效的高危人群筛查奠定理论基础。
溯源:高危病毒为何在华南富集?
研究团队进一步追溯高危EB病毒的演化起源,发现约4000年前,中国南北方EB病毒谱系在华南发生重组,形成高危型中最主要一支。这一病毒表现出适应性优势并发生克隆扩散,目前已感染约35%华南人群,成为该地区感染率最高的亚型(相关成果2024年发表于National Science Review)。
更重要的是,高危EB病毒与互作HLA-A亚型在华南共富集,从群体层面强化了“病毒-宿主”互作的遗传效应,共同塑造了华南人群鼻咽癌风险结构。
展望:从“事后治疗”迈向“事前预防”
开发疫苗是预防病毒感染肿瘤最有效、经济的手段。EB病毒是人类于1964年发现的第一个致瘤病毒,该病毒结构和生活周期复杂,人类对其十分易感。明确预防哪种病毒亚型、保护哪些高危人群对研发疫苗预防鼻咽癌十分重要。
研究团队的一系列研究,首次鉴别出驱动鼻咽癌高发的高危EB病毒亚型,为今后疫苗研发提供了重要依据;另一方面,通过识别对高危病毒致癌更易感的宿主特征,联合高危病毒与宿主易感因素,可实现鼻咽癌风险分层与高危人群的识别。
未来,对识别出的高危人群开展定期随访和持续监测,是实现鼻咽癌早诊早治的基础;同时,这部分人群也是未来疫苗接种和精准预防策略实施的重点目标人群。
中山大学肿瘤防治中心徐淼教授、新加坡基因组研究所刘建军教授、中科院动物研究所翟巍巍教授、哥伦比亚大学刘中华教授为该论文的共同通讯作者。中山大学肿瘤防治中心陈燕洪博士、梁婧彤博士为该论文的共同第一作者。该研究获得国家自然科学基金和国家重点研发计划支持。获得福建医科大学叶为民、中国医学科学院李贵登、上海科技大学李哲、西湖大学杨剑、中山大学肿瘤防治中心高嵩和曹雨露等多位专家的宝贵指导。
主要研究者介绍

通讯作者:徐淼
中山大学肿瘤防治中心教授、研究员、博士生导师,获国家自然科学基金优秀青年科学基金项目资助,中国抗癌协会青年科学家奖,现担任国际EB病毒协会理事。长期致力于EB病毒高危亚型与鼻咽癌预防研究,在Nature、Cancer Cell、Nature Genetics、PNAS等国际高水平期刊发表多篇研究论文;相关研究成果入选2019年中国医药生物技术十大进展,获国家自然科学奖二等奖(排名第四)、教育部高等学校自然科学奖一等奖(排名第二)、广东省自然科学奖一等奖(排名第二)。获鼻咽癌风险预测芯片相关专利多项,主持国家自然科学基金优秀青年科学基金、重大研究计划(培育)及国家重点研发计划青年科学家等项目,担任多个国际基金评审。

第一作者:陈燕洪
中山大学肿瘤防治中心博士生,2026年入选中心“志光计划”杰出青年医师-科学家。主要研究方向为肿瘤中宿主与病原体互作的遗传和分子机制研究。以第一作者(含共同)在Nature、National Science Review、Emerging Microbes & Infections等高水平期刊上发表论文。

共同第一作者:梁婧彤
中山大学肿瘤防治中心博士生,近五年以第一作者(含共同)在Nature, National Science Review,Journal of Infectious Diseases等杂志发表学术论文。
来源:中山大学肿瘤防治中心订阅号