引用本文:黄文钦, 杨亚龙, 吴新红, Matteo LAMBERTINI, 郑红梅. 激素受体阳性/HER2阴性早期乳腺癌内分泌治疗研究进展[J]. 肿瘤防治研究, 2026, 53(3): 169-175.
基金项目:湖北省肿瘤医院人才项目(2025HBCHLHRC002;2025HBCHHHRC005;2025HBCHQHRC018);楚天英才项目(CTYC002);吴阶平基金(320.6750.2024-21-5;320.6750.2025-21-13);湖北省医学青年拔尖人才项目(鄂卫通[2023]65号);湖北省肿瘤医院乳腺癌国家临床重点专科建设项目(HBCHBBC-A01);湖北省肿瘤医院院内科研项目(2025HBCHYN24;2025HBCHYN35)
作者单位:1. 430079 武汉,湖北省肿瘤医院(华中科技大学同济医学院附属湖北肿瘤医院)乳腺中心,国家临床重点专科建设学科,湖北省乳腺癌临床医学研究中心,武汉市乳腺癌临床医学研究中心;2. 16132 热那亚,IRCCS圣马蒂诺医院综合医院肿瘤内科;3. 16132 热那亚,热那亚大学医学院内科学与医学专科系
通信作者:郑红梅,女,博士,副主任医师,主要从事乳腺癌的基础和临床研究,E-mail: 2022ZL0002@hust.edu.cn,ORCID: 0009-0009-9541-1462;Matteo LAMBERTINI,男,博士,副教授,肿瘤内科顾问医师,主要从事乳腺癌的系统综合治疗, E-mail: matteo.lambertini@unige.it,ORCID: 0000-0003-1797-5296
作者简介:黄文钦,男,硕士在读,主要从事乳腺癌的基础和临床研究,ORCID: 0009-0002-1749-8530;杨亚龙*,男,博士,主治医师,主要从事乳腺癌的基础和临床研究,ORCID: 0000-0002-4167-3311(*:并列第一作者)
通信作者简介

郑红梅 教授
医学博士,硕士生导师,湖北省肿瘤医院乳腺中心牵头负责人、乳腺癌多学科联合诊疗团队(MDT)核心成员。曾赴美国约翰•霍普金斯大学乳腺肿瘤中心访问学习。2015年入选武汉市中青年医学骨干人才,2023年入选湖北省医学青年拔尖人才。长期从事乳腺癌临床与科研工作,主持湖北省自然科学基金面上项目2项、联合基金1项及湖北省卫健委青年人才项目1项;参与国际国内多中心乳腺癌药物临床试验(GCP)100余项;发表学术论文60余篇,其中以第一或通讯作者身份发表SCI论文20余篇。担任《中华乳腺病杂志(电子版)》通讯编委、《Cancer中文版》编委,以及《中国肿瘤临床》和Frontiers in Oncology审稿专家。作为第二完成人获湖北省科技进步二等奖1项,完成国际先进水平科技成果鉴定1项。主要学术兼职包括中国抗癌协会乳腺癌专委会委员、中华医学会肿瘤学分会乳腺肿瘤学组青年学者、中国抗癌协会肿瘤整形外科专委会第一届青年专家组成员、中国医药教育协会肿瘤药物临床研究专委会委员、湖北省抗癌协会乳腺癌专委会青委会副主委、湖北省临床肿瘤学会乳腺癌专委会青委会副主委、湖北省微循环学会乳腺甲状腺专业委员会副主委等。

Matteo LAMBERTINI
医学博士,意大利热那亚大学副教授、IRCCS圣马蒂诺综合医院肿瘤内科主任医师,年轻乳腺癌与生育力保存领域国际知名学者。长期致力于年轻乳腺癌个体化治疗与长期生存管理,核心研究方向为癌症治疗期间的生育力保存策略及治疗后安全妊娠问题。其系列研究成果为国际临床实践提供了关键循证依据。欧洲肿瘤内科学会(ESMO)指南委员会核心成员,《ESMO癌症患者生育力保存临床指南》工作组主席,并主持该国际指南的制定与更新。Annals of Oncology、Journal of Clinical Oncology及JAMA Oncology等多本国际顶尖期刊编委。截至2023年,发表学术论文220余篇,主持或参与多项具有里程碑意义的国际临床试验。通过系统而深入的临床与转化研究,以及广泛的学术领导工作,积极推动乳腺癌诊疗理念从“单纯治愈疾病”向“同时守护未来”的模式转变,其工作成果已转化为国际临床指南,深刻影响了全球年轻乳腺癌患者的诊疗路径与长期预后 。
摘 要:激素受体(HR)阳性/HER2阴性是早期乳腺癌最常见的亚型,内分泌治疗是其辅助治疗的基石。近年来,随着SOFT、TEXT、monarchE等关键研究结果的公布,以及以lidERA研究为代表的新药探索取得突破,HR阳性/HER2阴性早期乳腺癌的内分泌治疗策略正朝着更加精准和强化的方向发展。本文系统综述了该领域的最新进展,重点包括卵巢功能抑制(OFS)在绝经前高危患者中标准地位的巩固及其长期随访证据;延长内分泌治疗疗程的获益与风险评估;CDK4/6抑制剂在辅助治疗中的应用现状及不同药物间的差异。同时,探讨了当前治疗面临的问题与挑战,如治疗相关生活质量的优化与获益人群的精准筛选,并简要介绍了口服选择性雌激素受体降解剂(SERD)等新型药物的临床研究进展。此外,针对年轻患者的特殊需求,概述了化疗期间卵巢功能保护与生育力保存策略的循证医学依据。本文旨在为临床实践提供全面参考,协助临床医师在追求疗效最大化的同时,更好地平衡患者的长期生活质量和个体化需求。
关键词:乳腺肿瘤;激素受体阳性;人表皮生长因子受体2;内分泌治疗;卵巢功能抑制;CDK4/6抑制剂;卵巢保护;生育力保存
中图分类号:R737.9
0 引言
激素受体(Hormone receptor, HR)阳性/HER2阴性早期乳腺癌约占所有乳腺癌的70%[1],其治疗核心在于通过内分泌治疗阻断雌激素对肿瘤细胞的刺激,降低复发风险。过去十年间,HR阳性早期乳腺癌的辅助内分泌治疗模式经历了深刻变革:从以他莫昔芬单药为主,发展到芳香化酶抑制剂(AI)与卵巢功能抑制(OFS)联合方案的广泛应用,再到延长治疗策略的探索,以及CDK4/6抑制剂和口服选择性雌激素受体降解剂(SERD)等靶向药物在辅助治疗中的研究,治疗决策日趋精细化[2]。然而,如何进一步降低高危人群的复发风险、如何平衡强化治疗的获益与毒性、如何精准筛选最佳获益人群,以及如何管理治疗对患者生活质量(包括生育需求)的长期影响,仍是当前临床面临的关键问题。与此同时,新型内分泌药物(如口服SERD)的出现为辅助治疗带来了新的可能。针对年轻患者,化疗期间的卵巢功能保护与生育力保存策略也是关注的重点。本文旨在梳理HR阳性早期乳腺癌内分泌治疗的最新循证医学进展,讨论现存挑战,并展望未来的研究方向。
1 内分泌治疗的强化策略
1.1 OFS措施的地位巩固与最新证据
对于绝经前中高危HR阳性早期乳腺癌患者,在内分泌治疗基础上联合OFS已成为标准治疗策略。SOFT试验的长期随访数据进一步巩固了这一地位。其15年随访结果显示,与他莫昔芬单药相比,OFS联合他莫昔芬或依西美坦能持续改善无病生存率(DFS)[3]。分析显示,在整体人群中,OFS联合依西美坦相较于他莫昔芬单药显示出最终的总生存(OS)获益趋势(HR=0.83,95%CI: 0.69~1.00,P=0.05);在年龄<35岁的极高危年轻患者中,该获益更为显著[4]。TEXT与SOFT联合分析同样证实了OFS联合AI的长期生存优势[5]。ASTRRA研究的最新分析(中位随访106个月)则进一步证实,对于化疗后仍保留卵巢功能的患者,加用2年OFS可带来持续且显著的DFS(HR=0.56)和OS(HR=0.58)获益[6]。这些数据不仅巩固了OFS的标准地位,也提示其对年轻高危患者的获益可能更为突出,见表1。
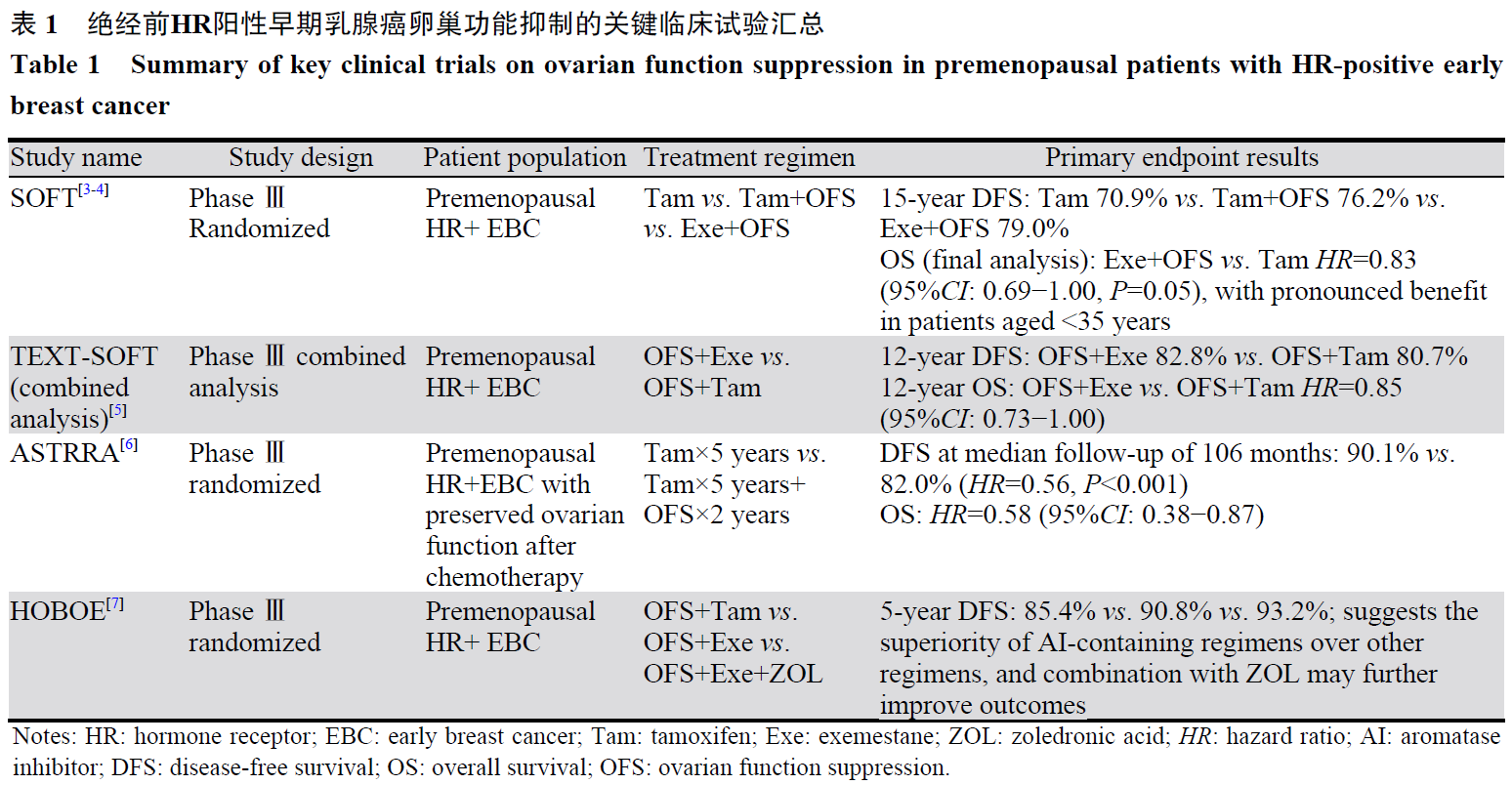
然而,OFS联合治疗伴随的潮热、盗汗、关节疼痛、骨质疏松及情绪影响等不良反应,显著影响了患者的生活质量与治疗依从性[8]。因此,管理这些不良反应已成为优化治疗的重要组成部分。最新研究关注的管理策略包括:使用非激素类药物,如加巴喷丁、选择性血清素再摄取抑制剂5-羟色胺等控制血管舒缩症状;以及通过基线骨密度监测、补充钙剂与维生素D、并在必要时使用双膦酸盐以预防和治疗骨质疏松[2]。此外,充分的治疗前教育、症状的主动监测与管理,以及多学科支持,对于提升OFS治疗的耐受性与依从性至关重要。
1.2 延长内分泌治疗的获益与风险平衡
对于已完成初始5年辅助内分泌治疗的患者,延长治疗(总疗程至10年)可进一步降低远期复发风险,尤其适用于具有高危因素的患者,如淋巴结阳性、组织学分级3级、诊断时年龄<35岁等[9]。MA.17R、NSABP B-42等研究证实了延长AI治疗可改善无病生存。然而,延长治疗的决策需高度个体化,必须权衡其带来的绝对复发风险降低与长期用药可能增加的不良反应(如骨质疏松、骨折、关节疼痛、心血管代谢影响)及对生活质量的潜在影响[10]。使用基因组检测工具(如Oncotype DX、MammaPrint)并综合肿瘤大小、淋巴结状态、分级、Ki-67指数等临床病理特征进行风险分层,有助于精准识别远期复发高风险且可能从延长治疗中显著获益的人群[11]。此外,真实世界数据显示,年轻患者的内分泌治疗依从性是其预后的关键影响因素,临床需采取有效措施加强支持与管理[12]。
2 CDK4/6抑制剂在辅助治疗中的应用:现状与差异
CDK4/6抑制剂在晚期HR阳性乳腺癌治疗取得成功后,其在辅助治疗阶段的探索成为研究热点,但不同药物的临床试验结果呈现明显异质性。
阿贝西利(Abemaciclib)在monarchE研究中取得了明确阳性结果。该研究入组了高危HR+/HER2-早期乳腺癌患者,其高危定义为:≥4枚阳性淋巴结,或1~3枚阳性淋巴结并同时伴有至少一项以下特征:肿瘤大小≥5厘米、组织学分级3级、Ki-67指数≥20%。中位随访76个月的最新数据显示,与安慰剂联合内分泌治疗相比,阿贝西利联合内分泌治疗持续改善无浸润性疾病生存期(IDFS)(HR=0.66),7年IDFS率的绝对差异达6.5%(77.4% vs. 70.9%),并显示出OS的改善趋势(HR=0.842)[13]。基于此,阿贝西利已成为多个国际指南推荐用于此类高危人群的辅助强化治疗的标准选择之一。
瑞波西利(Ribociclib)的NATALEE研究则将目标人群扩展至更广泛的Ⅱ~Ⅲ期患者(包括淋巴结阴性高危患者)。中位随访55.4个月的分析显示,瑞波西利联合ET可将复发风险降低28.4%,5年IDFS率分别为85.5%与81.0%[14]。然而,其在淋巴结阴性亚组中的绝对获益相对有限,风险获益比需审慎评估。
相比之下,帕博西利(Palbociclib)在辅助治疗领域的两项大型Ⅲ期研究(PALLAS和PENELOPE-B)均未达到主要终点,未能证明在标准内分泌治疗基础上加用帕博西利可显著改善IDFS[15-16]。这提示CDK4/6抑制剂在辅助治疗中的疗效存在药物特异性差异,可能与药物的选择性、治疗持续时间及入组人群的风险阈值不同有关。
达尔西利(Dalpiciclib)作为一种中国原研的CDK4/6抑制剂,其在DAWNA-A研究中针对伴有高危因素(如≥4枚阳性淋巴结)的Ⅱ~Ⅲ期中国患者取得了阳性结果,IDFS风险显著降低44%(HR=0.56)[17],为中国高危患者提供了新的治疗选择。
总体而言,现有证据支持在高复发风险的HR+/HER2-早期乳腺癌辅助治疗中,可考虑加用阿贝西利或瑞波西利进行强化,但必须严格筛选获益人群。帕博西利目前不推荐用于辅助治疗。不同药物疗效差异背后的生物学机制,以及对最佳获益人群的精细化筛选,是未来研究的重要方向,见表2。
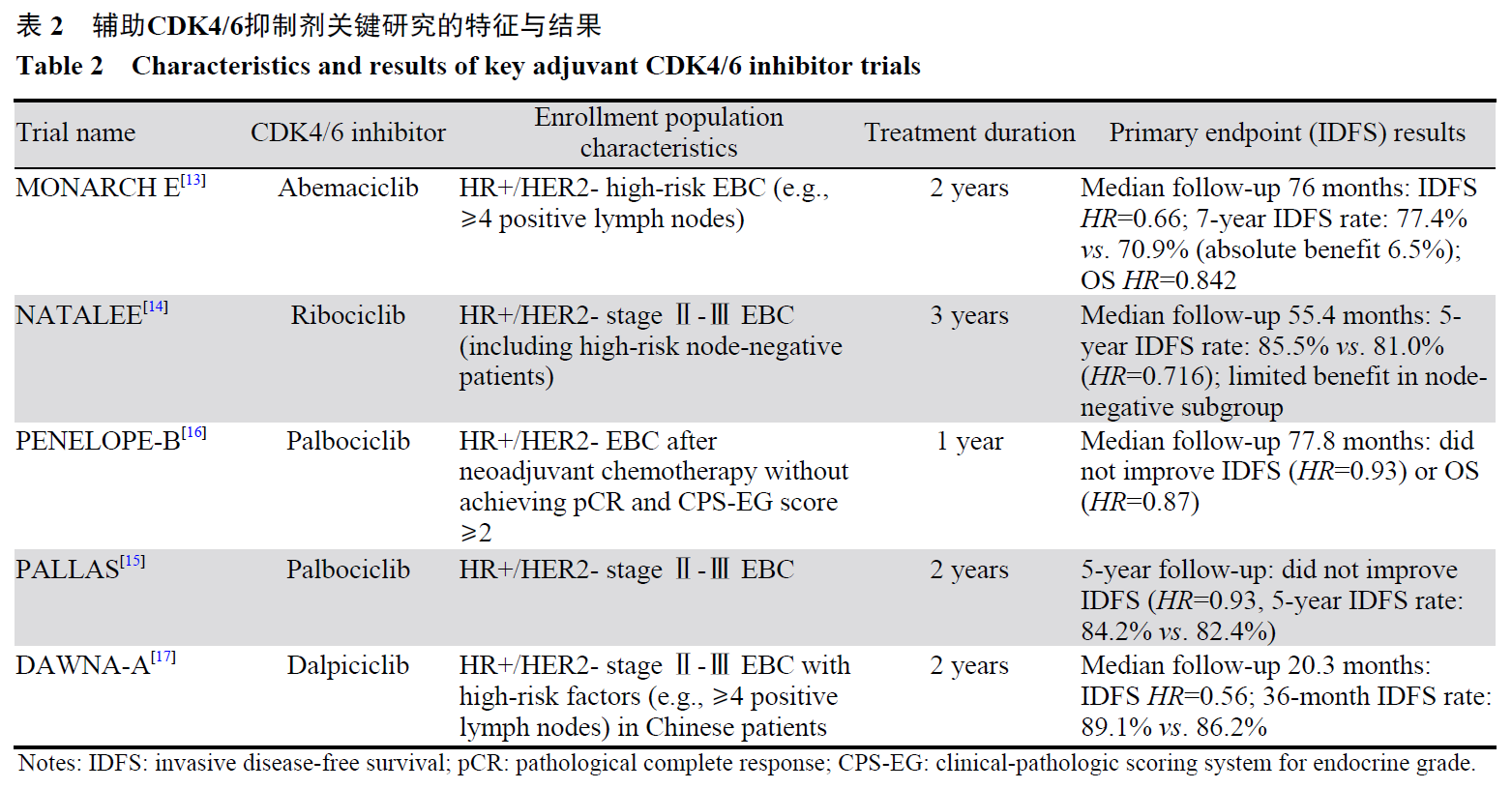
3 新型内分泌治疗药物的突破:口服SERD的辅助治疗前景
尽管现有强化策略已取得进展,但仍存在未被满足的临床需求。口服选择性雌激素受体降解剂(SERD)作为新一代内分泌治疗药物,因其可完全拮抗并降解雌激素受体,且口服给药便利,成为研发热点。
近期在2025年圣安东尼奥乳腺癌研讨会(SABCS)上报告的Bardia等开展的lidERA乳腺癌研究取得了里程碑式结果(尚未发表)。这项全球Ⅲ期临床试验纳入了4170例ER+/HER2−、分期为Ⅰ~Ⅲ期的乳腺癌患者,比较了口服SERD Giredestrant与标准辅助内分泌治疗(他莫昔芬或AI)的疗效与安全性。中位随访32个月的结果显示:主要终点IDFS:Giredestrant组显著优于对照组,疾病复发或死亡风险降低30%(HR=0.70, 95%CI: 0.57~0.87, P=0.0014),3年IDFS率分别为92.4%和89.6%;关键次要终点:无远处复发生存期(DRFI)的风险降低31%(HR=0.69)。安全性:Giredestrant耐受性良好,不良事件谱与标准治疗相似,且因不良事件导致的停药率更低。这是自AI获批用于辅助治疗20余年来,首个在早期乳腺癌辅助治疗中显示出显著阳性结果的新型内分泌治疗Ⅲ期研究,为高危患者提供了前景广阔的新选择。作为lidERA项目的子研究,评估Giredestrant联合阿贝西利的辅助治疗疗效的研究正在进行中,旨在探索进一步强化的联合策略。
除Giredestrant外,其他口服SERD如Imlunestrant(EMBER-3研究)、Elacestrant等,也正在晚期和早期乳腺癌中进行多项Ⅱ/Ⅲ期临床试验评估。此外,针对PI3K/AKT/mTOR通路抑制剂、组蛋白去乙酰化酶抑制剂(Histone deacetylase inhibitor, HDACi)等与内分泌药物联合的辅助治疗研究也在探索中,旨在克服内分泌耐药问题。
4 卵巢保护与生育力保存
4.1 化疗期间的卵巢功能保护
化疗对卵巢功能有明确的损伤风险,可能导致早发性卵巢功能不全(POI)甚至不孕[18]。在化疗期间使用促性腺激素释放激素激动剂(GnRHa)是保护卵巢功能、降低POI发生率的有效策略[19]。其作用机制可能与诱导卵巢处于暂时的“休眠”状态,从而减少原始卵泡被化疗药物损伤有关。多项随机临床试验的荟萃分析证实,GnRHa可将年轻乳腺癌患者化疗后POI发生率降低约50%[20],并提高化疗后月经恢复率。
新兴研究表明,二甲双胍作为一种潜在的卵巢保护药物,也显示出对抗化疗相关卵巢损伤的可能性。临床前研究提示,其可能通过抑制PI3K/Akt/FOXO3a通路、抗细胞凋亡、抗炎和促进自噬等机制改善卵巢储备功能。在动物模型中,二甲双胍被证实能显著改善化疗诱导的卵巢储备下降和激素分泌紊乱[21-22]。有临床研究进一步提示,二甲双胍具有保护女性生殖内分泌功能的潜力,例如在抗精神病药物引起的闭经患者中,二甲双胍(1 000 mg/d)可有效逆转闭经,月经恢复率达66.7%[23]。一项大型队列研究显示,父亲在备孕期间使用二甲双胍,并未增加后代的先天性畸形风险[24]。一项旨在评估二甲双胍在乳腺癌、宫颈癌等女性恶性肿瘤患者中卵巢保护作用的多中心随机对照试验(RCT)正在进行中[25]。这些发现为化疗期间的卵巢保护提供了潜在的补充策略思路,尤其适用于合并代谢异常的患者,但其在HR阳性乳腺癌患者中的长期疗效和安全性尚需进一步验证。
4.2 生育力保存策略与治疗中断
对于有生育需求的年轻患者,应在开始全身性抗肿瘤治疗前尽快咨询生殖医学专家[26]。胚胎冻存和卵母细胞冻存是当前成熟的、标准的生育力保存技术[27]。对于HR阳性患者,可采用联合来曲唑或他莫昔芬的卵巢刺激方案,以控制雌激素暴露水平,确保治疗的安全性[28]。在成功率方面,冻存胚胎的移植后活产率约为40%~50%,而冻存卵母细胞的移植后活产率约为30%~40%,具体取决于女性年龄和技术因素[29]。
POSITIVE试验是一项改变临床实践的重要研究。该试验结果显示,对于有生育需求的HR阳性早期乳腺癌女性,在完成18~30个月辅助内分泌治疗后,计划性中断治疗最多2年以尝试妊娠,并未导致短期乳腺癌复发风险的显著增加[30]。这为患者在疾病控制后实现生育需求提供了高级别循证医学证据支持。基于此,临床指南建议将生育咨询纳入所有年轻乳腺癌患者的初始治疗讨论。然而,对于复发风险极高的年轻患者,临床决策需更为审慎。通常建议优先在化疗前完成卵母细胞冻存,并考虑完成标准疗程(如5年)的内分泌治疗后,再计划妊娠,见表3。
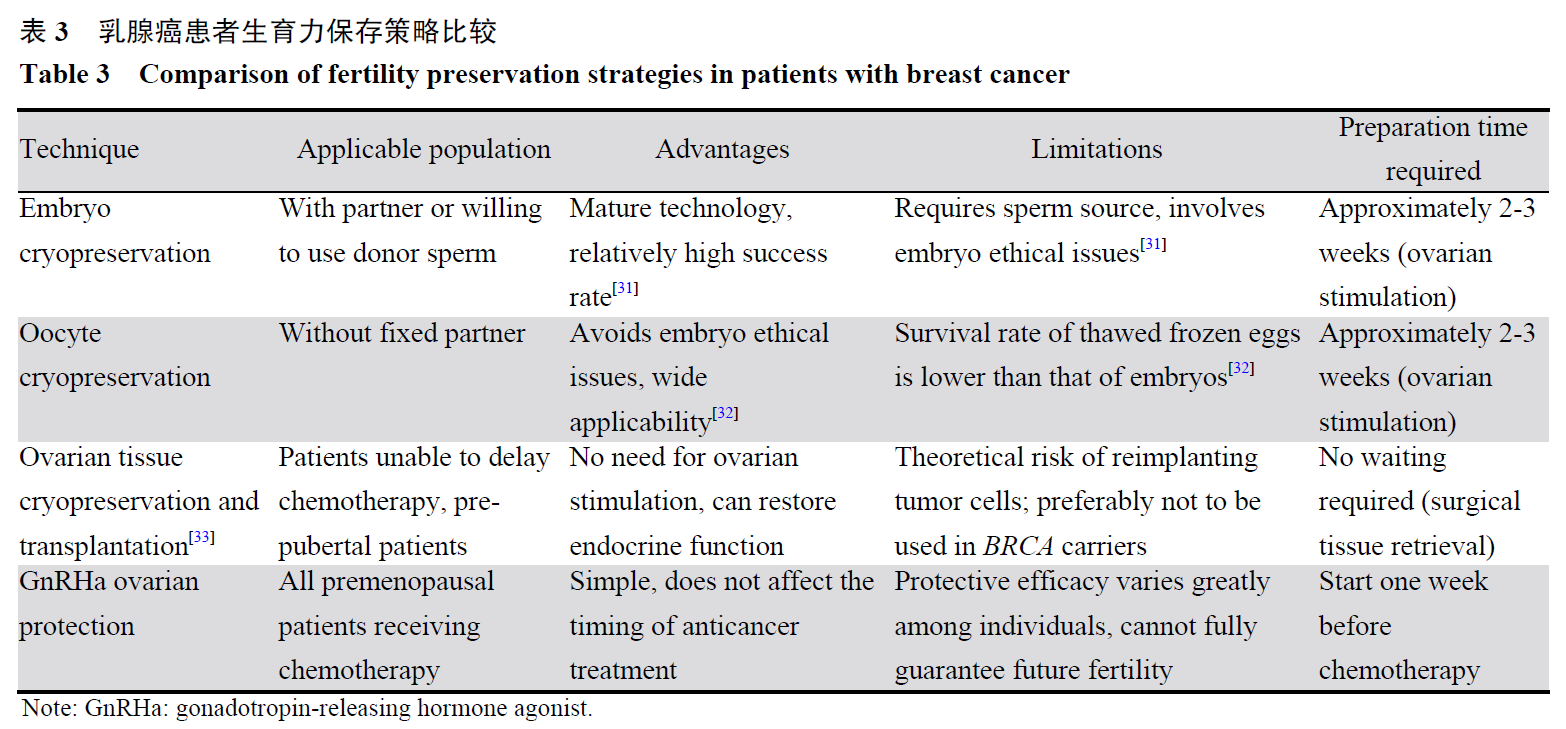
5 总结与展望
HR阳性/HER2阴性早期乳腺癌的辅助内分泌治疗已进入精准强化与个体化管理的新阶段。现有证据表明,OFS联合AI或他莫昔芬能显著改善绝经前高危患者的长期预后;CDK4/6抑制剂(如阿贝西利、瑞波西利等)为特定高危人群提供了有效的辅助强化手段;而延长治疗策略则进一步优化了远期复发风险的管理。
近期,口服选择性雌激素受体降解剂(SERD)在辅助治疗领域取得了里程碑式突破。Ⅲ期lidERA研究证实,Giredestrant对比标准内分泌治疗,可显著降低高危患者的复发风险,且耐受性良好,为临床提供了前景广阔的新选择。
然而,临床挑战依然存在:如何更精准地识别OFS、延长治疗及CDK4/6抑制剂的最佳获益人群,避免过度治疗;如何更有效地管理强化治疗相关不良反应,优化患者生活质量与治疗依从性;以及如何克服内分泌治疗耐药。未来,整合基因组学、液体活检(如ctDNA监测)及人工智能等工具,有望实现更精细的风险分层和动态疗效监控。
展望未来,HR阳性早期乳腺癌的治疗将继续朝着“疗效最大化、不良反应最小化、决策个体化”的方向发展。我们期待lidERA研究的长期随访数据以确认其总生存获益;评估其与CDK4/6抑制剂(如阿贝西利)联合应用的探索也值得关注。同时,其他口服SERD(如Imlunestrant)及针对不同耐药通路的新型药物联合辅助治疗研究正在积极开展。在充分利用现有强化策略、积极探索新型治疗手段的同时,始终将患者的生活质量、生育需求等长期关怀目标置于核心地位,将是临床实践与未来研究共同的努力方向。
参考文献
References
[1] Burstein HJ, Lacchetti C, Anderson H, et al. Adjuvant Endocrine Therapy for Women With Hormone Receptor-Positive Breast Cancer: ASCO Clinical Practice Guideline Focused Update[J]. J Clin Oncol, 2019, 37(5): 423-438. doi: 10.1200/JCO.18.01160
[2] Francis PA, Pagani O, Fleming GF, et al. Tailoring Adjuvant Endocrine Therapy for Premenopausal Breast Cancer[J]. N Engl J Med, 2018, 379(2): 122-137. doi: 10.1056/NEJMoa1803164
[3] Francis PA, Regan MM, Fleming GF, et al. Adjuvant Ovarian Suppression in Premenopausal Breast Cancer[J]. N Engl J Med, 2015, 372(5): 436-446. doi: 10.1056/NEJMoa1412379
[4] Francis PA, Fleming GF, Pagani O, et al. 15-year outcomes for women with premenopausal hormone receptor-positive early breast cancer (BC) in the SOFT and TEXT trials assessing benefits from adjuvant exemestane (E) + ovarian function suppression (OFS) or tamoxifen (T)+OFS[J]. J Clin Oncol, 2025, 43(16_suppl): 505. doi: 10.1200/jco.2025.43.16_suppl.505
[5] Pagani O, Walley BA, Fleming GF, et al. Adjuvant Exemestane With Ovarian Suppression in Premenopausal Breast Cancer: Long-Term Follow-Up of the Combined TEXT and SOFT Trials[J]. J Clin Oncol, 2023, 41(7): 1376-1382. doi: 10.1200/JCO.22.01064
[6] Baek SY, Noh WC, Ahn SH, et al. Adding Ovarian Suppression to Tamoxifen for Premenopausal Women With Hormone Receptor-Positive Breast Cancer After Chemotherapy: An 8-Year Follow-Up of the ASTRRA Trial[J]. J Clin Oncol, 2023, 41(31): 4864-4871. doi: 10.1200/JCO.23.00557
[7] Francis PA, Fleming GF, Láng I, et al. Adjuvant Endocrine Therapy in Premenopausal Breast Cancer: 12-Year Results From SOFT[J]. J Clin Oncol, 2023, 41(7): 1370-1375. doi: 10.1200/JCO.22.01065
[8] Gravina A, Gargiulo P, De Laurentiis M, et al. Ten-year update of HOBOE phase Ⅲ trial comparing triptorelin plus either tamoxifen or letrozole or zoledronic acid + letrozole in premenopausal hormone receptor-positive early breast cancer patients[J]. ESMO Open, 2025, 10(1): 104085. doi: 10.1016/j.esmoop.2024.104085
[9] Gnant M, Fitzal F, Rinnerthaler G, et al. Duration of Adjuvant Aromatase-Inhibitor Therapy in Postmenopausal Breast Cancer[J]. N Engl J Med, 2021, 385(5): 395-405. doi: 10.1056/NEJMoa2104162
[10] Mamounas EP, Bandos H, Rastogi P, et al. Ten-year update: NRG Oncology/National Surgical Adjuvant Breast and Bowel Project B-42 randomized trial: extended letrozole therapy in early-stage breast cancer[J]. J Natl Cancer Inst, 2023, 115(11): 1302-1309. doi: 10.1093/jnci/djad078
[11] Mamounas EP, Bandos H, Rastogi P, et al. Breast Cancer Index and Prediction of Extended Aromatase Inhibitor Therapy Benefit in Hormone Receptor-Positive Breast Cancer from the NRG Oncology/NSABP B-42 Trial[J]. Clin Cancer Res, 2024, 30(9): 1984-1991. doi: 10.1158/1078-0432.CCR-23-1977
[12] Walbaum B, García-Fructuoso I, Martínez-Sáez O, et al. Hormone receptor-positive early breast cancer in young women: A comprehensive review[J]. Cancer Treat Rev, 2024, 129: 102804. doi: 10.1016/j.ctrv.2024.102804
[13] Johnston S, Martin M, O'Shaughnessy J, et al. Overall survival with abemaciclib in early breast cancer[J]. Ann Oncol, 2025: S0923-7534(25)04948-8.
[14] Slamon D, Lipatov O, Nowecki Z, et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer[J]. N Engl J Med, 2024, 390(12): 1080-1091. doi: 10.1056/NEJMoa2305488
[15] Mayer EL, Dueck AC, Martin M, et al. Palbociclib with adjuvant endocrine therapy in early breast cancer (PALLAS): interim analysis of a multicentre, open-label, randomised, phase 3 study[J]. Lancet Oncol, 2021, 22(2): 212-222. doi: 10.1016/S1470-2045(20)30642-2
[16] Loibl S, Marmé F, Martin M, et al. Palbociclib for Residual High-Risk Invasive HR-Positive and HER2-Negative Early Breast Cancer-The Penelope-B Trial[J]. J Clin Oncol, 2021, 39(14): 1518-1530. doi: 10.1200/JCO.20.03639
[17] Shao ZM, Hao J, Wang S, et al. Dalpiciclib (Dalp) plus endocrine therapy (ET) as adjuvant treatment for HR+/HER2–early breast cancer (BC): The randomized, phase 3, DAWNA-A trial[J]. J Clin Oncol, 2025, 43(16_suppl): 515. doi: 10.1200/jco.2025.43.16_suppl.515
[18] Moore HC, Unger JM, Phillips KA, et al. Goserelin for Ovarian Protection during Breast-Cancer Adjuvant Chemotherapy[J]. N Engl J Med, 2015, 372(10): 923-932. doi: 10.1056/NEJMoa1413204
[19] Lambertini M, Moore HCF, Leonard RCF, et al. Gonadotropin-Releasing Hormone Agonists During Chemotherapy for Preservation of Ovarian Function and Fertility in Premenopausal Patients With Early Breast Cancer: A Systematic Review and Meta-Analysis of Individual Patient-Level Data[J]. J Clin Oncol, 2018, 36(19): 1981-1990. doi: 10.1200/JCO.2018.78.0858
[20] Lambertini M, Ceppi M, Poggio F, et al. Ovarian suppression using luteinizing hormone-releasing hormone agonists during chemotherapy to preserve ovarian function and fertility of breast cancer patients: a meta-analysis of randomized studies[J]. Ann Oncol, 2015, 26(12): 2408-2419. doi: 10.1093/annonc/mdv374
[21] Zatalian N, Dalman A, Afsharian P, et al. Metformin protects prepubertal mice ovarian reserve against cyclophosphamide via regulation of the PI3K/Akt/mTOR signaling pathway and Yap-1[J]. J Ovarian Res, 2024, 17: 251. doi: 10.1186/s13048-024-01572-4
[22] Yang Y, Tang X, Yao T, et al. Metformin protects ovarian granulosa cells in chemotherapy-induced premature ovarian failure mice through AMPK/PPAR-γ/SIRT1 pathway[J]. Sci Rep, 2024, 14: 1447. doi: 10.1038/s41598-024-51990-z
[23] Wu RR, Jin H, Gao KM, et al. Metformin for treatment of antipsychotic-induced amenorrhea and weight gain in women with first-episode schizophrenia: a double-blind, randomized, placebo-controlled study[J]. Am J Psychiatry, 2012, 169(8): 813-821. doi: 10.1176/appi.ajp.2012.11091432
[24] Meng LC, van Gelder MMHJ, Chuang HM, et al. Paternal metformin use and risk of congenital malformations in offspring in Norway and Taiwan: population based, cross national cohort study[J]. BMJ, 2024, 387: e080127. doi: 10.1136/bmj-2024-080127
[25] Zhang J, Ma X, Li Y, et al. Metformin intervention against ovarian toxicity during chemotherapy for early breast cancer: Study protocol for a randomized double-blind placebo-controlled trial[J]. Maturitas, 2020, 137: 1-6. doi: 10.21203/rs.2.22188/v1
[26] Oktay K, Turan V, Bedoschi G, et al. Fertility Preservation Success Subsequent to Concurrent Aromatase Inhibitor Treatment and Ovarian Stimulation in Women With Breast Cancer[J]. J Clin Oncol, 2015, 33(22): 2424-2429. doi: 10.1200/JCO.2014.59.3723
[27] Rodriguez-Wallberg KA, Anastacio A, Vonheim E, et al. Fertility preservation for young adults, adolescents, and children with cancer[J]. Ups J Med Sci, 2020, 125(2): 112-120. doi: 10.1080/03009734.2020.1737601
[28] Rodriguez-Wallberg KA, Eloranta S, Krawiec K, et al. Safety of fertility preservation in breast cancer patients in a register-based matched cohort study[J]. Breast Cancer Res Treat, 2018, 167(3): 761-769. doi: 10.1007/s10549-017-4555-3
[29] Su HI, Lacchetti C, Letourneau J, et al. Fertility Preservation in People With Cancer: ASCO Guideline Update[J]. J Clin Oncol, 2025, 43(12): 1488-1515. doi: 10.1200/JCO-24-02782
[30] Partridge AH, Niman SM, Ruggeri M, et al. Interrupting Endocrine Therapy to Attempt Pregnancy after Breast Cancer[J]. N Engl J Med, 2023, 388(18): 1645-1656. doi: 10.1056/NEJMoa2212856
[31] Dolmans MM, Hossay C, Nguyen TYT, et al. Fertility preservation: How to preserve ovarian function in children, adolescents and adults[J]. J Clin Med, 2021, 10(22): 5247. doi: 10.3390/jcm10225247
[32] Practice Committees of the American Society for Reproductive Medicine and the Society for Assisted Reproductive Technology. Mature oocyte cryopreservation: a guideline[J]. Fertil Steril, 2013, 99(1): 37-43. doi: 10.1016/j.fertnstert.2012.09.028
[33] Donnez J, Martinez-Madrid B, Jadoul P, et al. Ovarian tissue cryopreservation and transplantation: a review[J]. Hum Reprod Update, 2006, 12(5): 519-535. doi: 10.1093/humupd/dml032
来源:《肿瘤防治研究》官网