本文刊登于《现代妇产科进展》2026年第35卷第3期
引用本文:
中华医学会妇科肿瘤学分会.妇科肿瘤治疗相关血小板减少症临床管理专家共识[J].现代妇产科进展,2026,35(3):161-172.
DOI:
10.13283/j.cnki.xdfckjz.2026.03.001
通信作者:
原文下载:
血小板减少症是妇科肿瘤治疗中常见的血液学不良反应,不仅可能导致治疗延迟或剂量强度降低,影响治疗效果,还会增加出血倾向,严重时可导致患者死亡。目前,针对妇科肿瘤治疗相关血小板减少症的临床管理尚缺乏高级别循证医学证据,长期以来临床处理主要依据化疗所致血小板减少症(chemotherapy-induced thrombocytopenia,CIT)的小样本临床研究和临床经验处理方案。近年来,随着靶向治疗和免疫治疗的广泛应用,妇科肿瘤治疗进入了新时代,疗效显著提升,但这些靶向和免疫治疗药物亦可引起不同程度的血小板减少症,其发生机制与CIT有所不同。因此,将“CIT”拓展为“肿瘤治疗相关血小板减少症(cancer therapy induced thrombocytopenia,CTIT)”进行系统全面管理,具有重要的临床意义。促血小板生成药物可以防治肿瘤治疗引起的血小板减少症,有助于降低患者的出血风险,减少血小板输注,避免血制品相关不良反应。掌握各种促血小板生成药物的作用机制、用药指征、剂量和疗程,以确保疗效最大化并减轻毒副反应,是临床合理用药的前提。为此,中华医学会妇科肿瘤学分会组织专家组,基于现有循证医学证据,结合临床防治经验,经过深入讨论和投票表决形成推荐等级,达成《妇科肿瘤治疗相关的血小板减少症临床管理专家共识》,旨在为临床合理应用提供参考。
本指南采用中华医学会妇科肿瘤学分会推荐分类,见表1。

1 概述
妇科三大恶性肿瘤(子宫颈癌、子宫内膜癌和卵巢癌)在全球范围内约占女性所有新发肿瘤的14.4%,在中国约占12.6%,是威胁女性身体健康的重大疾病[1]。骨髓抑制是抗肿瘤治疗常见的不良反应,血小板减少症是最常见的剂量限制性毒性反应之一。妇科肿瘤治疗过程中,CTIT发生率较高。CTIT可能增加出血风险,严重时需输注血小板,延长住院时间、增加治疗费用,继而引起药物剂量强度降低及治疗时间延迟,最终影响抗肿瘤治疗的效果和生存质量,导致不良预后。
1.1 定义及诊断
1.1.1 定义及分级
CTIT是指由抗肿瘤治疗导致的血小板生成减少或(和)破坏增加或(和)分布异常,临床表现为外周血中血小板计数低于100×109/L。
根据血小板减少的程度,具体分级标准参考美国国家癌症研究所常见不良反应术语标准(common terminology criteria for adverse event,CTCAE)5.0版(表2)。

1.1.2 诊断及鉴别诊断
多种疾病或治疗相关因素可通过影响血小板生成、破坏、消耗及分布等环节,导致血小板减少症(表3)。CTIT的诊断需结合血小板计数动态变化与患者的肿瘤治疗史,在详细采集病史基础上,结合体格检查及辅助检查结果,排除其他非肿瘤治疗相关因素,明确诊断。

详尽而具有针对性的病史询问与体格检查,有助于明确血小板减少症的原因。采集病史时,除需明确血小板减少症的持续时间、严重程度及出血倾向等,还应系统询问患者的既往史、用药史、酗酒史、妊娠史、家族史等信息,以全面收集可能与血小板减少相关的重要线索。体格检查的重点在于评估有无出血倾向,同时需关注有无脾脏肿大、面部红斑、关节肿痛等。在询问病史和体格检查基础上,应针对性地选择辅助检查手段。外周血检查是血小板计数的主要检查方法。除血小板计数检查外,血小板形态学和免疫学相关检查对进一步明确血小板减少症的病因亦具有一定的参考价值,检测血小板相关抗体有助于鉴别诊断。骨髓检查适用于病因不明或疑有原发性血液系统疾病的患者。
CTIT的诊断流程主要包括:确认患者接受过可能引起血小板减少的抗肿瘤治疗史,分析血小板减少的模式(包括发生时间、具体数值、恢复情况)是否符合所用治疗方案的典型特征,开展必要的鉴别诊断,评估出血风险和临床症状,最终根据严重程度分级,制定个体化的治疗和监测方案。
1.2 发病机制及流行病学
妇科肿瘤相关治疗,包括化疗、放疗、靶向治疗和免疫治疗等,均可导致血小板减少症。其发生风险与患者自身因素、肿瘤特征及治疗方案密切相关。CTIT的发生机制主要包括血小板生成减少、血小板破坏增加以及血小板分布异常(表4)。按照是否由免疫机制介导,可进一步分为以下两类:(1)非免疫介导型:主要由肿瘤治疗对骨髓巨核细胞或血小板的直接毒性作用所致,导致血小板生成障碍或破坏增多。该类型通常呈现剂量和时间依赖性。(2)免疫介导型:通过免疫机制导致血小板减少。
1.2.1 化疗相关血小板减少症
血小板减少症的发生时间与严重程度受多种因素影响,包括化疗药物的种类与剂量、是否联合治疗、患者自身特征以及化疗周期。一项纳入15521例接受化疗的实体瘤患者的大型研究显示,在3个月内发生血小板减少症的比例为13%,其中3级血小板减少症占4%,4级血小板减少症占2%。接受吉西他滨和铂类为基础化疗方案的实体瘤患者,血小板减少症发生率(分别为14.8%和13.5%)明显高于接受蒽环类或紫杉类为基础化疗方案的患者(分别为9.3%和6.5%)。多数化疗方案,首次出现血小板减少症的中位时间约为化疗开始后1~2周。但在大多数肿瘤类型中,以铂类为基础的化疗方案,首次出现血小板减少症的中位时间超过2周[2]。
妇科恶性肿瘤常用化疗方案多是以铂类为基础的联合方案,因此CTIT发生率较高,特别是卡铂联合吉西他滨治疗时,3级以上血小板减少症的发生率超过30%(表5)。
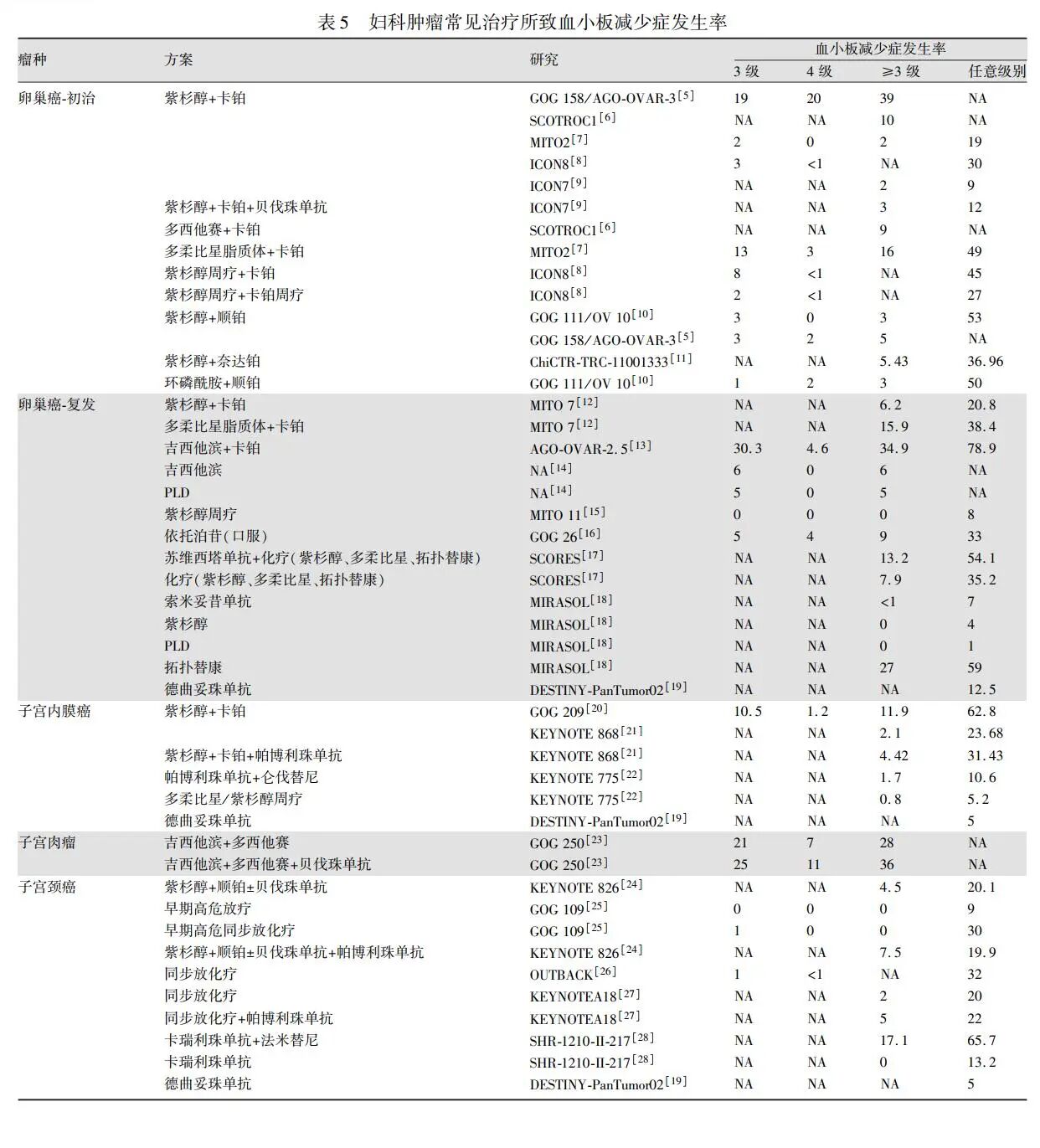
1.2.2 放疗相关血小板减少症
放疗是妇科肿瘤的重要治疗手段,尤其适用于子宫内膜癌和子宫颈癌。骨髓作为人体中最大的造血器官,其中红骨髓承担着红细胞、粒细胞、血小板及部分淋巴细胞的生成功能。成人红骨髓主要分布于颅底骨、胸骨、肋骨、肩胛骨、脊柱及髂骨等区域。盆腔放疗常导致血小板减少症,不仅可能引起放疗中断、剂量降低,还会增加出血风险,从而影响疗效和患者安全。妇科肿瘤放疗导致的CTIT发生率低于化疗,但在同步放化疗时风险升高。目前,国内外关于放疗所致血小板减少症的研究大多为小样本研究,证据级别不高。
1.2.3 靶向治疗和免疫治疗相关血小板减少症
靶向药物和免疫检查点抑制剂等抗肿瘤药物在妇科肿瘤治疗中应用日趋广泛,其所致血小板减少症的发生机制与化疗有所不同,尤其免疫检查点抑制剂并非通过骨髓抑制发挥作用,其管理策略更为复杂,应引起临床医师的关注。
1.2.3.1 靶向治疗相关血小板减少症
靶向药物的不良反应主要分为在靶效应和脱靶效应,在靶效应是指靶向药物在抑制肿瘤靶点的同时,不可避免地抑制了正常组织的相应靶点功能,从而导致不良反应。在靶效应多可通过降低剂量得以控制。目前,针对靶向药物相关血小板减少症的临床管理策略以暂停用药和降低剂量为主,后续用药方案根据血小板恢复情况以及是否再次出现血小板减少决定。
妇科肿瘤靶向治疗中,较易引起CTIT的药物为多腺苷二磷酸核糖聚合酶(poly ADP ribose polymerase,PARP)抑制剂。PARP1在巨核细胞谱系中表达,对造血干细胞具有调节作用。PARP抑制剂通过抑制PARP1,进而减少血小板形成。PARP抑制剂相关血小板减少症的发生率为8%~70%,其中3~4级血小板减少症的发生率为1%~34%(表6)。
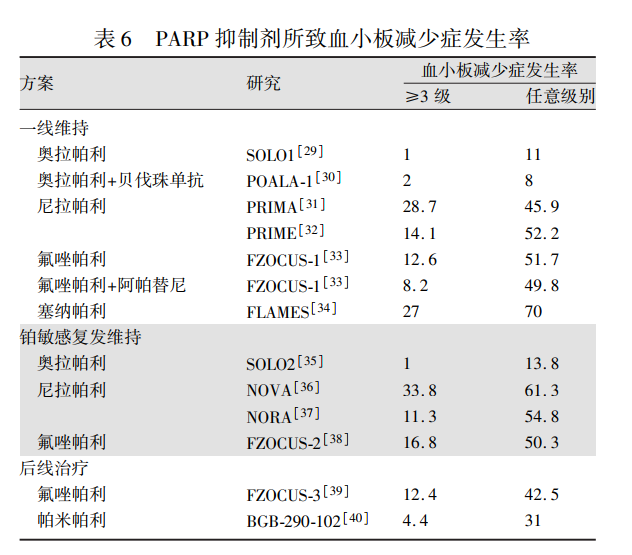
贝伐珠单抗可能引起少见但严重的急性免疫性血小板减少症。血清血小板抗体检测显示,患者体内存在针对糖蛋白Ⅱb的抗体,经糖皮质激素及对症支持治疗后有效,提示贝伐珠单抗引起CTIT的机制可能与免疫反应相关[3]。
抗体偶联药物(antibody drug conjugate,ADC)通过将小分子细胞毒性药物连接至单克隆抗体,通过抗体对靶标的识别作用,实现细胞毒性药物向目标肿瘤细胞的定向运输,从而在实现定向杀伤肿瘤细胞的同时,降低全身毒性。ADC相关血小板减少症的管理策略与化疗相关血小板减少症相似。
1.2.3.2 免疫治疗相关血小板减少症
免疫检查点抑制剂(immune checkpoint inhibitor,ICI)在发挥正性免疫调节作用的同时,亦可引起全身各种器官组织的免疫相关性不良反应。其中,免疫性血小板减少症(immune thrombocytopenia,ITP)相对罕见。与放化疗多直接损伤骨髓、靶向药物通过靶点作用影响造血功能的机制不同,ICI相关血小板减少症多为继发自身免疫反应所致。文献报道其发生率为0.2%~2.8%。一项大型多中心回顾性研究共纳入86467例接受ICI治疗的患者,其中214例(0.25%)发生ITP。独立危险因素包括基线血小板计数较低、ICI联合治疗、Ⅳ期肿瘤以及合并其他免疫相关不良事件。ITP中位发病时间为ICI启动后8周,血小板计数中位最低值为41×109/L。在76例重启ICI治疗的患者中,23例(30.3%)再次出现ITP[4]。
妇科肿瘤治疗常采用联合治疗模式,CTIT的发生率较高(表5、6)。不同肿瘤治疗手段及药物所致CTIT的发生机制各异,涉及血小板生成、破坏及分布等多个环节。对于接受化疗联合免疫治疗的患者,若出现血小板减少症,应仔细鉴别是免疫相关性还是化疗所致,以指导后续治疗策略的制定。
2 治疗
2.1 治疗原则及流程
CTIT的治疗目的主要包括:提高抗肿瘤治疗过程中血小板计数的最低值,缩短CTIT的持续时间,减少甚至避免输注血小板,从而有效预防出血事件的发生;同时,避免因CTIT导致的抗肿瘤计划延迟或剂量强度降低。
在CTIT治疗决策中,病因评估是治疗决策的基础,准确判断患者的出血风险及出血程度是选择适宜治疗措施的重要依据[世界卫生组织(WHO)出血分级标准见表7]。

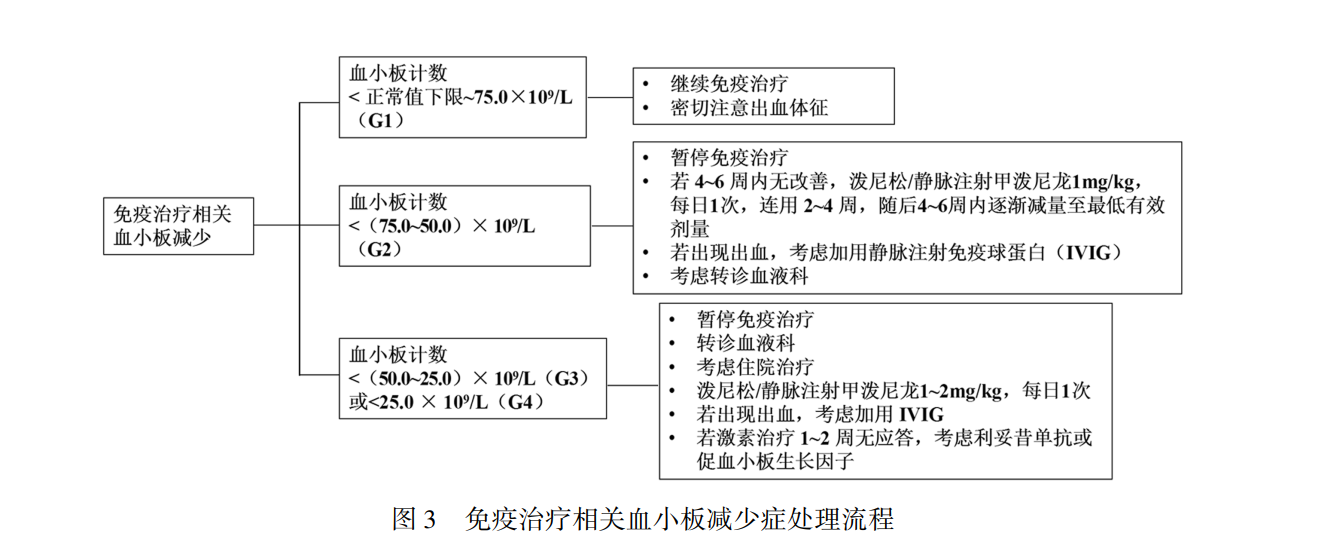
CTIT的主要治疗措施包括血小板输注与促血小板生长因子治疗。促血小板生长药物主要包括重组人血小板生成素(recombinant human thrombopoietin,rhTPO)、重组人白介素-11(rhIL-11)、血小板生成素受体激动剂(thrombopoietin receptor agonist,TPO-RA)以及咖啡酸片等药物。血小板减少症处理流程:化疗相关血小板减少症处理流程(图1),PARP抑制剂相关血小板减少症处理流程(图2),免疫治疗相关血小板减少症处理流程(图3)。
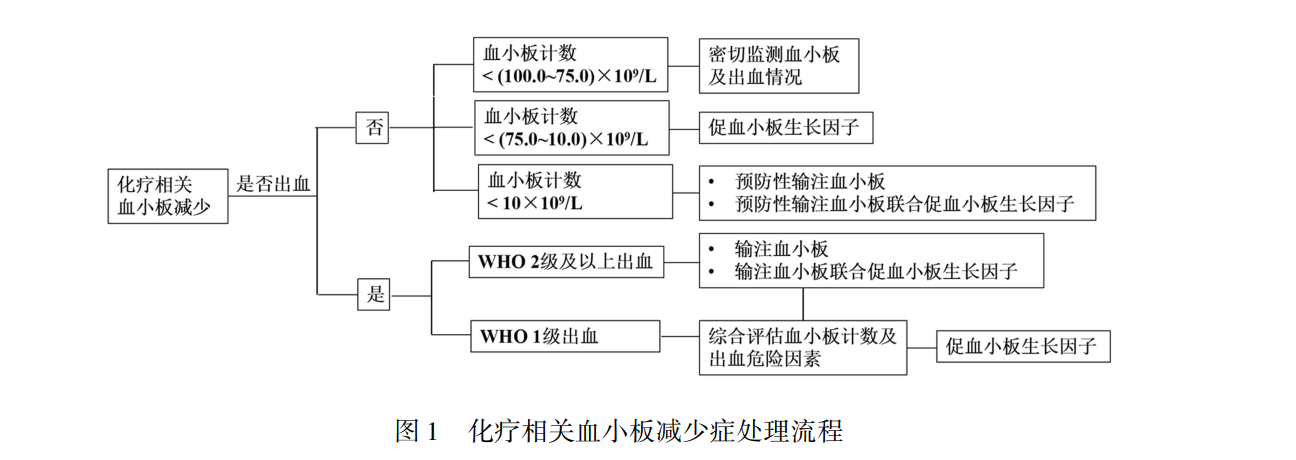
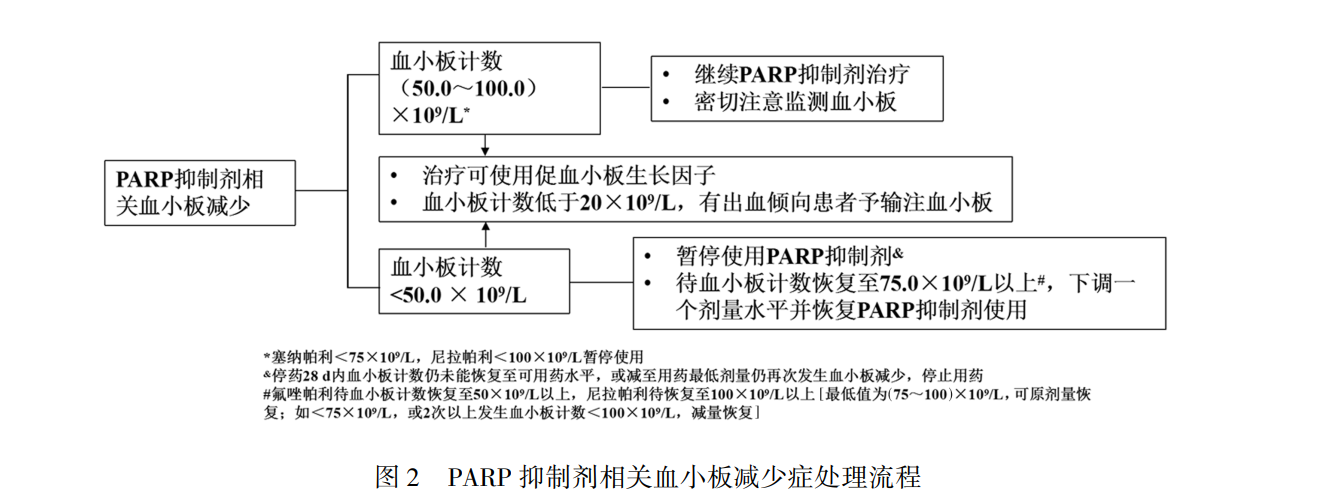
2.2 治疗措施
2.2.1 输注血小板
输注血小板是纠正重度血小板减少症最快、最有效的治疗方法,能有效降低严重出血的风险和死亡率。血小板减少症患者发生活动性出血时,多数情况下应立即输注血小板,使血小板计数维持在>50×109/L;而对于中枢神经系统出血,则应保证血小板计数维持在>100×109/L。
目前尚无理想的预测自发性出血的方法,即使在血小板计数>50×109/L时,患者仍可能发生出血。对于血小板计数为(5~50)×109/L的患者,结合临床表现及危险因素有助于制定血小板输注决策。美国血液和生物治疗促进协会(AABB)与国际输血医学指南协作组(ICTMG)联合发布的2025年《血小板输注指南》中,对于正在接受化疗的非出血性低增生性血小板减少症患者,当血小板计数小于10×109/L时,强烈建议输注血小板[41]。若患者合并炎症、感染、发热或肿瘤坏死,出血风险增加,输注血小板的阈值可适当提高到20×109/L。
基于以上研究,对于血小板计数≤10×109/L或CTIT合并出血的患者,推荐输注血小板(1类)。
输注的异体血小板消耗迅速,维持期仅3~5天,且存在多种风险,包括可能增加血液传播的感染性疾病风险(如艾滋病、乙型及丙型肝炎等)、输血反应及输血后紫癜等。此外,同种异体免疫反应介导产生的血小板抗体可能引起血小板输注无效。
除规范血小板输注外,促血小板生长药物是治疗CTIT的重要手段。
2.2.2 促血小板生成药物
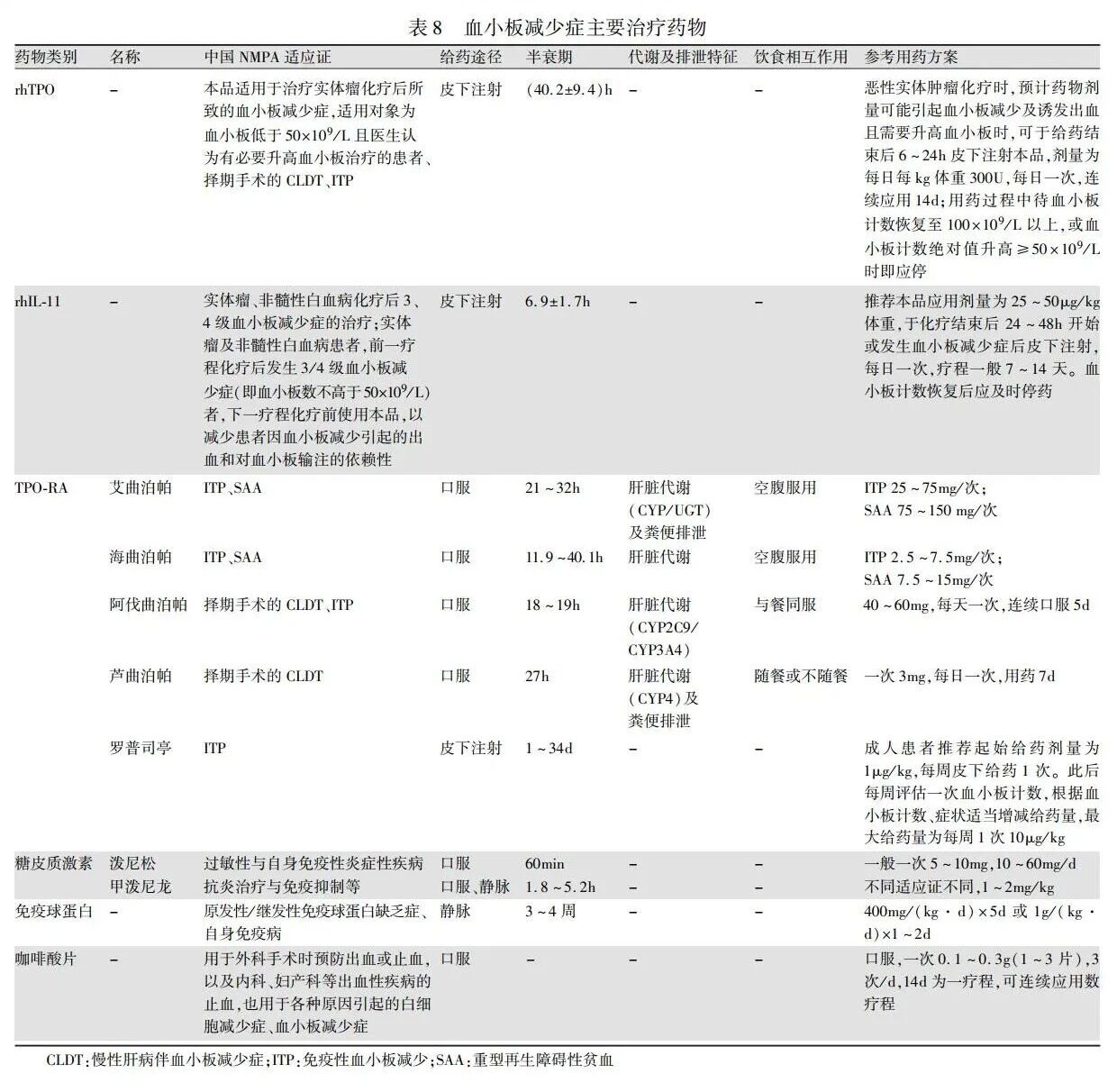
促血小板生长药物主要包括rhTPO、rhIL-11和TPO-RA。中国国家药品监督管理局(National Medical Products Administration,NMPA)已批准rhTPO和rhIL-11用于化疗所致血小板减少症。长期以来,CTIT可用的治疗手段较有限。近年来,TPO-RA在CTIT治疗的临床研究数据不断积累,显示出一定的临床疗效。此外,咖啡酸片等药物也已获批用于血小板减少症(表8)。
2.2.2.1 重组人血小板生成素
2.2.2.1.1 机制
血小板生成素(thrombopoietin,TPO)是刺激巨核细胞生长及分化的内源性细胞因子,对巨核细胞生成的各阶段均有刺激作用,包括前体细胞的增殖、多倍体巨核细胞的发育及成熟,从而升高血小板数目。rhTPO是利用基因重组技术由中国仓鼠卵巢细胞表达、经提纯制成的全长糖基化血小板生成素,与内源性血小板生成素具有相似的升高血小板的药理作用。
2.2.2.1.2 临床研究疗效分析
一项回顾性研究评估了妇科恶性肿瘤患者应用rhTPO治疗化疗期间血小板减少症(血小板计数<80×109/L)的疗效与安全性。20例使用rhTPO者为用药组,10例未使用rhTPO者为对照组。用药组平均(10.5±4.9)天血小板升高并恢复正常,而对照组平均(21.4±8.6)天恢复正常(P<0.001)[42]。另一项rhTPO治疗同步放化疗肿瘤患者血小板减少症的临床疗效观察显示,38例患者(包括9例子宫颈癌)在同步放化疗后出现血小板计数<50×109/L,接受rhTPO治疗后,血小板降低发生于(5.2±1.9)天;胸骨和盆骨照射体积≥50%者用药后恢复至正常所需时间更长;血小板计数恢复至≥75×109/L所需时间为(6.1±2.4)天,恢复至≥100×109/L所需时间为(7.9±2.5)天。研究结论认为,rhTPO能有效减轻同步放化疗后血小板降低的程度与持续时间,促进血小板恢复[43]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用rhTPO(1类)。
2.2.2.1.3 不良反应及注意事项
rhTPO较少引起不良反应,偶有发热、肌肉酸痛、头晕等,一般不需处理,多可自行恢复。个别症状明显者可对症处理。在CITⅢ期临床试验中未见严重不良反应。74例患者在治疗周期中接受了抗体动态检测,其中3例患者(4%)于给药后第21天和第28天血清中检测出低滴度(1∶5)非中和性抗rhTPO抗体,但未发现对rhTPO升高血小板的作用产生影响。
血小板计数过度升高可能增加血栓形成或血栓栓塞风险,因此应用rhTPO时不应试图使血小板计数提升至正常值。对低反应性或不能维持血小板应答者,应进一步查找诱因,包括rhTPO的中和抗体或骨髓纤维化。此外,刺激造血细胞表面的TPO受体可能增加恶性血液病的发生风险。用药期间应定期检查血常规,一般隔日一次,密切注意血小板计数变化,达到所需指标后应及时停药。在用药前、用药过程中及停药后随访中,应监测包括血小板计数和外周血涂片在内的血常规。用药前应检查外周血分类,建立红细胞和白细胞异常形态的基线水平,停药后定期监测至少两周。
2.2.2.2 rhIL-11
2.2.2.2.1 机制
rhIL-11是利用基因重组技术生产的促血小板生长因子,可直接刺激造血干细胞和巨核祖细胞的增殖,诱导巨核细胞成熟分化,增加体内血小板生成,从而提高血小板计数,而对血小板功能无明显影响。
2.2.2.2.2 临床研究疗效分析
一项多中心、随机、安慰剂对照试验纳入93例因化疗导致严重血小板减少症且已接受血小板输注的肿瘤患者(其中5例卵巢癌),评估rhIL-11的疗效。入组前一个化疗周期中,所有患者均因血小板最低值≤20000/μL而接受血小板输注。研究期间患者继续接受原剂量化疗。患者随机接受安慰剂或rhIL-11皮下注射,于化疗后第1天开始,每日1次,连续14~21天。结果显示,在27例可评估的rhIL-11 50μg/kg剂量组患者中,8例(30%)未再需要血小板输注,而安慰剂组27例患者中仅1例(4%)未需输注(P<0.05)[44]。
另一项随机对照试验评估了rhIL-11用于妇科肿瘤患者化疗诱导的血小板减少症的疗效与安全性,给药剂量为50μg/kg,以无治疗观察组作为对照。结果显示,与对照组相比,rhIL-11组患者的血小板最低值升高更显著,且血小板计数恢复至≥100000/μL的时间显著缩短[45]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,血小板计数<75.0×109/L时,推荐应用rhIL-11(1类)。
2.2.2.2.3 不良反应及注意事项
rhIL-11的大部分不良反应均为轻至中度,停药后均可迅速消退。约有10%的患者在用药期间出现以下不良事件,包括乏力、疼痛、寒战、腹痛、感染、恶心、便秘、消化不良、瘀斑、肌痛、骨痛、神经紧张及脱发等。
临床使用过程中应警惕可能发生的过敏反应,并告知患者一旦出现过敏症状需及时报告医务人员。已报道的过敏反应相关体征和症状包括面部、舌体或喉部水肿,呼吸急促,喘息,胸痛,低血压(包括休克),发音困难,意识丧失,精神状态改变,皮疹,荨麻疹,潮红和发热等。过敏反应在本品首次给药或多次给药后均可能发生,一旦发生过敏反应,应永久停用。
器质性心脏病患者,尤其是有充血性心衰及房颤、房扑病史的患者应慎用。用药期间应严密观察心力衰竭相关症状和体征,如出现呼吸困难、端坐呼吸、运动耐量降低、肺部啰音、颈静脉充盈、双下肢水肿等表现,应停药并采取适当的处置措施。
用药期间还应严密观察毛细血管渗漏综合征相关症状和体征,如出现尿量减少、体重快速增加、水肿、憋气、血压降低、肺水肿、胸腹腔积液等情况,应停药并采取适当的处置措施。
2.2.2.3 TPO-RA
TPO-RA主要通过结合并激活TPO受体发挥作用,主要包括小分子拟肽类和小分子非肽类TPO-RA。小分子拟肽类TPO-RA与TPO受体的结合位点位于胞外区,小分子非肽类TPO-RA则与TPO受体的跨膜区结合。
2.2.2.3.1 小分子拟肽类TPO-RA
小分子拟肽类TPO-RA主要包括罗普司亭(romiplostim)和其生物类似物罗普司亭N01。罗普司亭是全球首个上市的拟肽类长效血小板生成素受体激动剂,随机对照研究证实其具有确切的促血小板生成疗效。国产生物类似物罗普司亭N01具有与罗普司亭相似的质量、疗效和安全性,已获批临床应用。罗普司亭/罗普司亭N01用于治疗CIT的起始剂量为2~4μg/kg,每周1次皮下注射,每周可增加1~2μg/kg,最大剂量为10μg/kg,直到血小板计数升至(100~150)×109/L,具体用药方案可参考表9。

RECITE研究是一项全球多中心、随机双盲、安慰剂对照的Ⅲ期临床研究,纳入165例持续性化疗相关血小板减少症(计划化疗第1天血小板≤85×109/L)的消化道恶性肿瘤患者,旨在评估罗普司亭的安全性与有效性。主要研究终点为在第2或第3个化疗周期中,未因CIT对任何骨髓抑制药物进行剂量调整的患者比例。结果显示,罗普司亭组维持足剂量化疗的比例显著高于安慰剂组(84% vs 36%,OR=10.16;95%CI:4.44~23.72;P<0.001)。与安慰剂组相比,罗普司亭组患者的血小板应答率显著升高(97% vs 77%),血小板谷值显著升高(87×109/L vs 58×109/L,P=0.005);首次血小板反应中位时间显著缩短(1.1周 vs 2.1周,P<0.001)[46]。
罗普司亭N01治疗化疗引起血小板减少症的Ⅱ/Ⅲ期临床研究Part A为开放标签、剂量探索研究,纳入50例血小板计数≤200×109/L的患者,主要终点为抗肿瘤治疗周期最后一天的血小板应答率。其中组3为20例血小板计数<100×109/L者,应答率为90%[47]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用罗普司亭或罗普司亭N01(2A类)。
2.2.2.3.2 小分子非肽类TPO-RA
小分子非肽类TPO-RA主要分为偶氮苯衍生物(艾曲泊帕和海曲泊帕)和噻唑类衍生物(芦曲泊帕和阿伐曲泊帕),均为口服制剂(具体见表8)。此类药物可与TPO受体的跨膜区结合,启动信号级联反应,诱导骨髓祖细胞和巨核细胞的增殖和分化,从而促进血小板的生成。
艾曲泊帕和海曲泊帕含有金属离子螯合基团,与抗酸药或含多价阳离子的其他产品(如奶制品和矿物质补充剂)合用时,会显著降低药物暴露量,因此需空腹口服,且给药前后与食物或其他药品间隔至少2h。阿伐曲泊帕在空腹条件下的暴露量差异较大,但与食物同服时可增加吸收并降低变异性,故应与餐同服。芦曲泊帕是目前已获批的小分子非肽类TPO-RA中可空腹或随餐服用的药物。
2.2.2.3.2.1 海曲泊帕相关临床研究
2.2.2.3.2.1.1单药治疗化疗相关血小板减少症
一项Ⅱ期研究(NCT03976882)纳入60例因血小板减少症导致化疗较原计划延迟≥7天且血小板计数<75×109/L的恶性肿瘤患者,按1∶1随机分配至海曲泊帕组或安慰剂组。研究采用连续给药模式,起始剂量7.5mg/d,连续口服直至完成2个周期化疗,期间可根据血小板计数进行剂量调整或暂停给药。主要研究终点为总体治疗有效率(定义为在开始研究药物治疗后14天内血小板计数≥100×109/L并恢复化疗,后续能够完成两个连续化疗周期,且无因血小板减少症导致的化疗方案调整,亦未使用任何升血小板援救治疗)。结果显示,海曲泊帕组的治疗有效率显著高于安慰剂组(60.7% vs 12.9%,P<0.001)。在接受研究药物治疗14天内,海曲泊帕组85.7%的受试者血小板计数≥100×109/L并开始第1个周期化疗,显著高于对照组的48.4%。从开始接受研究药物治疗到血小板计数≥100×109/L的中位时间分别为7.5天和13.0天。恢复化疗后,海曲泊帕组和安慰剂组分别有17例(60.7%)和8例(25.8%)受试者能够完成两个连续化疗周期,且未因血小板减少症导致化疗方案调整或接受升血小板援救治疗[48]。
一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究纳入192例接受含铂联合治疗方案后出现血小板减少症(血小板计数<75×109/L)且导致化疗较预计时间延迟≥7天的恶性肿瘤患者,随机分配至海曲泊帕连续给药组、海曲泊帕转换组和对照组。纠正治疗期:连续给药组和转换组口服海曲泊帕(起始剂量7.5 mg/d),对照组口服安慰剂。进入维持治疗期后,完成2个连续周期(C1和C2)的化疗用药,连续给药组和对照组继续接受海曲泊帕或安慰剂;转换组改为连续口服2周期安慰剂。主要研究终点为治疗有效的患者比例(需同时满足以下条件:①14天内血小板计数恢复至≥100×109/L;②完成第一个化疗周期[C1]并在C1D21[+4天]时血小板计数≥75×109/L,且未接受升血小板援救治疗)。结果显示,海曲泊帕连续给药组治疗有效率为75.7%,海曲泊帕转换组为48.6%,对照组为39.4%。海曲泊帕连续给药组的治疗有效率显著高于对照组(组间差异为36.2%;95%CI:21.0~51.3;P<0.0001),而海曲泊帕转换组与对照组无显著差异(组间差异为9.0%;95%CI:-7.2~25.1;P=0.2757)。研究结论:在实体瘤CTIT患者中,海曲泊帕纠正CTIT后连续给药能够稳定维持血小板计数在正常水平,保障患者按计划足剂量完成后续抗肿瘤治疗周期[49]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用海曲泊帕(2A类)。
2.2.2.3.2.1.2 单药治疗PARP抑制剂相关血小板减少症
一项Ⅱ期前瞻性研究纳入21例接受PARP抑制剂治疗且血小板计数在50×109/L至100×109/L的卵巢癌患者,予海曲泊帕治疗直至血小板计数达到≥100×109/L或相对于基线升高≥50×109/L。达到者进入维持期,继续应用海曲泊帕14天。主要研究终点为血小板计数≥100×109/L且相对于基线升高≥25×109/L的患者比例。结果显示,在17例可评估患者中,52.9%达到主要终点,中位恢复时间为10天,76.4%的患者血小板计数恢复至正常范围,且17例可评估患者中均未因血小板减少症延迟或调整PARP抑制剂剂量[50]。
基于以上研究,对于妇科肿瘤PARP抑制剂相关血小板减少症(50×109/L≤血小板计数≤100×109/L)患者,推荐应用海曲泊帕(2B类)。
2.2.2.3.2.1.3 联合治疗CTIT
海曲泊帕和rhTPO与TPO受体的结合区域不同,基础研究提示两者联合呈现促血小板生成的协同增效作用[51]。
一项回顾性研究纳入294例CTIT(血小板计数<50×109/L)实体瘤患者,对比海曲泊帕联合rhTPO组(146例)与单药rhTPO组(148例)的疗效。结果显示,联合组14天内血小板计数较基线升高≥50×109/L的比例显著高于单药组(82.2% vs 67.6%,P=0.005)。两组不良事件发生率无显著差异[52]。
一项前瞻性双队列研究纳入28例同步或序贯放化疗后血小板减少症的实体瘤患者。队列1[血小板计数(30~50)×109/L]患者接受海曲泊帕联合rhIL-11治疗;队列2[血小板计数(50~75)×109/L]患者接受海曲泊帕单药治疗。主要研究终点为血小板计数恢复至≥75×109/L的患者比例及血小板恢复的中位时间。队列1(10例)中60.0%的患者血小板计数恢复至≥75×109/L,中位恢复时间为4.5天;队列2(18例)中77.8%的患者血小板计数恢复至≥75×109/L,中位恢复时间为4.5天[53]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用海曲泊帕联合rhTPO治疗(2B类);当血小板计数<50.0×109/L时,推荐应用海曲泊帕联合rhTPO(2A类)或海曲泊帕联合rhIL-11(2A类)治疗。
2.2.2.3.2.2 艾曲泊帕
应用艾曲泊帕开展临床研究探索化疗相关血小板减少症的应用,可能受限于给药方案的设计,虽未达到主要研究终点,但显示出一定的临床获益趋势。
一项多中心、随机双盲、安慰剂对照的Ⅱ期研究,纳入183例一线接受卡铂联合紫杉醇治疗的晚期实体瘤患者(其中46例卵巢癌),于每个化疗周期的第2~11天口服研究药物,至少治疗2个周期。主要研究终点为第2个化疗周期第1天血小板计数与第2个化疗周期血小板计数最低值的差值,研究未达到主要研究终点[54]。另一项Ⅱ期随机、安慰剂对照研究纳入75例接受吉西他滨单药或联合顺铂/卡铂方案治疗并发生血小板减少症的晚期实体瘤患者(其中9例卵巢癌),于化疗前5天及化疗后5天接受艾曲泊帕或安慰剂治疗。主要研究终点为第1~6个化疗周期内,每个化疗周期第1天化疗开始前的血小板计数。结果显示,艾曲泊帕组各周期第1天血小板计数数值上均高于安慰剂组,但未达到统计学显著差异;艾曲泊帕治疗可缩短血小板计数从最低点恢复的时间,并减少因血小板减少症导致的化疗剂量延迟与减量[55]。
2.2.2.3.2.3 阿伐曲泊帕
一项多中心、随机双盲的Ⅲ期研究纳入了122例血小板计数<50×109/L的实体瘤患者,于化疗前5天及化疗后5天接受阿伐曲泊帕或安慰剂治疗。主要研究终点为治疗有效率,定义为无需血小板输注,且未因血小板减少症导致的化疗方案减量≥15%或化疗延迟≥4天的患者比例。结果显示,阿伐曲泊帕组与安慰剂组的治疗有效率无显著差异,研究未达到主要研究终点[56]。一项真实世界研究纳入101例化疗后血小板计数≤100×109/L的恶性肿瘤患者,阿伐曲泊帕连续口服5天或用药至血小板恢复,升血小板有效率达87.1%,仅1%发生出血事件,24.8%接受血小板输注[57]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用阿伐曲泊帕或艾曲泊帕(2B类)。
2.2.2.3.3 不良反应和注意事项
2.2.2.3.3.1 肝毒性
艾曲泊帕及海曲泊帕的肝毒性较同类药物的发生率略高,用药前需全面评估患者肝功能,肝功能损害者应慎用,并在治疗过程中密切监测相关指标。芦曲泊帕和阿伐曲泊帕对肝功能的影响较小。
2.2.2.3.3.2 血栓形成和血栓栓塞并发症
当血小板计数升高至正常范围以上时,理论上存在血栓形成/血栓栓塞并发症的风险。值得注意的是,既往在血小板计数正常或低于正常值范围时,亦有血栓事件的临床报道。对于存在易栓症风险因素的患者(包括但不限于因子V Leiden突变、ATⅢ缺乏、抗磷脂综合征、恶性肿瘤、避孕和激素替代治疗、长期制动、手术/外伤、高龄、肥胖及吸烟等),应慎用本品。为降低血栓/栓塞事件的发生风险,应严格遵守剂量调整方案,将血小板计数控制在目标范围内。用药期间应密切监测血小板计数,一旦超过一定水平,应考虑减量、暂停或终止治疗。
2.2.2.3.3.3 骨髓纤维化和恶性克隆增生
TPO-RA可能增加骨髓中网硬蛋白纤维化的风险,骨髓网硬蛋白增加被认为是TPO受体刺激导致骨髓中巨核细胞数量增加的结果,进而可能释放细胞因子。目前关于TPO-RA是否促进恶性克隆增生或克隆演化尚无定论。TPO-RA治疗前和治疗期间建议通过外周血涂片和全血细胞计数监测细胞形态学异常。如果出现血细胞减少或形态异常,建议及时行骨髓活检。
2.2.2.4 免疫检查点抑制剂相关血小板减少症的治疗药物
免疫检查点抑制剂相关血小板减少症处理可参考图3。糖皮质激素为此类血小板减少症的主要治疗药物(表8),其使用应遵循“早期、足量、足疗程”的原则,并在病情稳定后逐步减量。促血小板生长因子可作为二线治疗药物。
2.2.2.5 咖啡酸片
咖啡酸片的主要成分为咖啡酸,通过刺激巨核细胞成熟、增加巨核细胞总数,可有效预防及治疗药物相关的血小板减少。一项研究纳入60例肿瘤化疗所致血小板减少症(50×109/L<血小板计数<100×109/L)患者,采用自身对照设计,给予咖啡酸片/模拟剂治疗。第1个化疗周期(阴性对照期)于化疗开始第1天给予咖啡酸片模拟剂;第2、3个化疗周期(药物治疗期)采用与第1个化疗周期相同方案及剂量的化疗,并于化疗第1天开始给予咖啡酸片。研究结果显示,药物治疗期血小板最低值较阴性对照期显著升高(P<0.001);药物治疗期化疗后血小板计数恢复至最高值亦显著高于阴性对照期(P<0.001);药物治疗期血小板计数<50×109/L的持续天数与阴性对照期无显著差异,但有缩短趋势(P>0.05);药物治疗期化疗后血小板计数恢复至≥75×109/L和≥100×109/L所需天数较阴性对照期均明显减少(P<0.001);研究期间无一例患者需要血小板输注[58]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少症患者,当血小板计数<75.0×109/L时,推荐应用咖啡酸片(2B类)。
3 预 防
血小板自然寿命较短,通常在化疗1~2周后开始下降。内源性TPO的反馈上升较为缓慢,起效延迟,因此在血小板计数回升前可能出现出血风险增加甚至发生严重并发症。对于既往发生严重CTIT或合并高风险因素者,可考虑采取预防性干预。
妇科肿瘤治疗相关血小板减少症的预防需综合评估以下因素:患者一般情况与病史、抗肿瘤治疗导致血小板减少症的发生时间及下降幅度、不同种类升血小板药物的作用机制、疗效和不良反应等因素。
CTIT的高风险因素主要包括:体能状态ECOG评分≥2分或严重营养不良;肿瘤细胞骨髓浸润;易引起CTIT的靶向药物(如PARP抑制剂)、化疗药物(铂类、吉西他滨以及蒽环类等)的应用,尤其是联合治疗时;既往或当前接受放疗,特别是放疗部位包括长骨、扁骨(如骨盆、胸骨等)。
3.1 一级预防
一级预防是指在疾病发生前进行的预防。血小板减少症的一级预防是指对于易发生CTIT的患者,在首次抗肿瘤药物治疗后即开始使用升血小板药物进行预防。目前,妇科肿瘤治疗相关血小板减少症的一级预防尚缺乏明确的循证医学证据,其适用人群、用药时机及方式尚未明确。
3.2 二级预防
二级预防是临床前期预防。血小板减少症的二级预防是指上一个化疗周期发生过≥3级严重血小板减少症的患者,针对可能导致血小板再次减少、出血风险较高的致病因素所采取的预防性措施。其目的是预防化疗后血小板减少症的发生,从而保障化疗按时足量进行,避免化疗减量或延迟。CTIT的二级预防主要适用于以下两类患者:上一个化疗周期发生过≥3级的严重血小板减少症的患者;发生过2级血小板减少症但合并CTIT高风险因素者。
3.2.1 重组人血小板生成素
一项多中心Ⅲ期临床试验采用随机交叉自身对照设计,纳入311例实体瘤患者,其中92例为化疗后血小板减少症患者。治疗周期于化疗结束后6~24h皮下注射rhTPO 300U/kg,1次/日,疗程7~14天,对照周期化疗后不注射rhTPO,作为自身对照。结果显示,治疗周期与对照周期相比,化疗后血小板下降的最低值分别为(66±41)×109/L和(55±27)×109/L(P<0.001),化疗后血小板计数恢复的最高值分别为(266±126)×109/L和(146±56)×109/L(P<0.001),化疗后血小板恢复至≥75×109/L的中位天数分别为11天和16天(P<0.001)。研究结论认为,对于化疗后血小板减少症,rhTPO能显著升高血小板计数,减轻血小板下降幅度,加快血小板恢复[59]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少的二级预防,推荐应用rhTPO(1类)。
3.2.2 重组人白介素11
一项研究纳入100例化疗后血小板减少症(血小板计数<75×109/L)的实体肿瘤患者,首先给予rhIL-11治疗;在下一化疗周期,所有患者于化疗结束后24h内即开始使用rhIL-11二级预防,对比两个阶段患者血小板减少症的持续时间、严重程度等指标。结果显示,与治疗阶段相比,rhIL-11的二级预防可显著降低化疗相关血小板减少症的严重程度,缩短血小板减少症持续时间及血小板恢复时间,减少血小板输注需求,同时缩短rhIL-11的用药时长[60]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少的二级预防,推荐应用rhIL-11(1类)。
3.2.3 血小板生成素受体激动剂
PLATUM研究是一项Ⅱ期多中心单臂研究,纳入20例接受同步放化疗过程中发生3级或4级血小板减少症的胶质母细胞瘤患者,所有患者接受每周一次的罗普司亭皮下注射,研究终点为接受罗普司亭治疗的血小板减少症患者中能够完成6个周期替莫唑胺维持化疗的比例。结果显示,60%的患者完成了既定6个周期的替莫唑胺维持治疗,与历史对照(10%)相比,罗普司亭显著提高了3/4级CTIT患者完成既定6个周期的替莫唑胺维持化疗的比例[61]。
罗普司亭N01治疗化疗相关血小板减少症的Ⅱ/Ⅲ期临床研究Part B为随机双盲、安慰剂对照研究,纳入60例患者血小板计数为(75~200)×109/L,旨在比较罗普司亭N01与安慰剂预防CTIT的疗效和安全性。主要研究终点为应答患者比例[定义为能连续完成两个化疗周期,且未发生因血小板减少症导致的剂量调整(剂量减少≥15%或延迟≥4天或停药)且不需要挽救治疗]。结果显示,罗普司亭N01组应答率显著高于安慰剂组(40.9% vs 68.3%),校正后的率差为27.6%[47]。
一项前瞻性临床研究纳入20例上一个化疗周期发生过≥2级血小板减少症,经干预后血小板恢复至≥100×109/L的妇科肿瘤患者,于化疗结束后24h内开始口服海曲泊帕5mg/d,连续服用10天,以维持血小板计数≥100×109/L。结果显示,预防用药的化疗周期内,35%的患者出现血小板计数<75×109/L;化疗周期第21天时,95%的患者血小板计数≥75×109/L,65%的患者血小板计数≥100×109/L;海曲泊帕治疗期间,化疗第4、7、10、14、21天中位血小板计数分别为203.2×109/L、150.05×109/L、131.2×109/L、108.7×109/L、120.8×109/L[62]。
基于以上研究,对于妇科肿瘤治疗相关血小板减少患者的二级预防,推荐应用罗普司亭/罗普司亭N01(2A类)、海曲泊帕(2A类)。
3.2.4 咖啡酸片
一项研究将82例肿瘤患者随机分为AB组和BA组,每例患者均接受2个疗程化疗。AB组第一疗程(A周期)于化疗前3天开始口服咖啡酸片,持续至化疗结束;第二疗程(B周期)则不服药;BA组顺序相反。所有患者均按指定化疗方案完成化疗,且A、B两个周期必须使用相同方案。结果显示:化疗第7天,A周期与B周期血小板计数无显著差异;第14天及第21天,A周期血小板计数显著高于B周期(P<0.05)。A周期血小板减少症发生率显著低于B周期(P<0.05)[63] 。
基于以上研究,对于妇科肿瘤治疗相关血小板减少患者的二级预防,推荐应用咖啡酸片(2B类)。
4 结 语
妇科肿瘤治疗相关血小板减少症是抗肿瘤治疗中的常见不良反应,加强其防治管理非常必要。CTIT的治疗应首先明确病因,评估出血风险,再根据病因及严重程度采取相应的治疗策略,主要措施包括输注血小板以及应用促血小板生长药物。目前,现有临床证据多来源于化疗相关血小板减少症,而放疗、靶向治疗和免疫治疗所致血小板减少症的处理同等重要,但相关研究较少且样本量较小,临床实践中多参照化疗相关血小板减少症进行处理。需特别注意的是,免疫治疗相关血小板减少症的发生机制与化疗不同,应遵循免疫相关不良反应处理原则管理。重组人血小板生成素和白介素-11在CTIT中获得Ⅰ类推荐;血小板生成素受体激动剂罗普司亭/罗普司亭N01、海曲泊帕获得ⅡA类推荐。促血小板生成药物既可用于CTIT治疗,亦可用于二级预防。临床应用促血小板生成药物时,需要考虑适应证、禁忌证及推荐等级,严密监测疗效与不良反应,必要时需多学科参与管理,以避免血栓形成和其他严重不良反应的发生。
指南专家组成员:
孔北华 向 阳 刘继红 宋 坤 姜 洁 殷爱军
张 青 尹如铁 李小平 李秀琴 李艳芳 李 晓
夏百荣 李 斌 鹿 欣 金 平 张正茂 高庆蕾
张丙忠 王世宣 吴琪俊 刘木彪 陈 刚 娄 阁
谭文华 王彦龙 汪 辉 张国楠 梁志清 王建六
马 丁
指南评审组成员:
马 丁 华中科技大学同济医学院附属同济医院
王丹波 辽宁省肿瘤医院
王世宣 华中科技大学同济医学院附属同济医院
王彦龙 厦门市妇幼保健院
王建六 北京大学人民医院
王新宇 浙江大学医学院附属第一医院
王登凤 四川省肿瘤医院
王颖梅 天津医科大学总医院
王 薇 上海市第一妇婴保健院
尹如铁 四川大学华西第二医院
孔北华 山东大学齐鲁医院
曲芃芃 天津市中心妇产科医院
向 阳 中国医学科学院北京协和医院
刘开江 上海交通大学医学院附属仁济医院
刘木彪 珠海市妇幼保健院
刘继红 中山大学附属肿瘤医院
孙 阳 福建省肿瘤医院
李小平 北京大学人民医院
李秀琴 中国医科大学附属盛京医院
李科珍 华中科技大学同济医学院附属同济医院
李俊东 中山大学附属肿瘤医院
李艳芳 中山大学附属肿瘤医院
李 晓 浙江大学医学院附属妇产科医院
李 斌 中国医学科学院肿瘤医院
杨 红 空军军医大学西京医院
杨佳欣 中国医学科学院北京协和医院
吴琪俊 中国医科大学公共卫生学院
汪 辉 浙江大学医学院附属妇产科医院
宋 坤 山东大学齐鲁医院
张正茂 河北医科大学附属肿瘤医院
张丙忠 中山大学孙逸仙纪念医院
张 青 山东大学齐鲁医院
张国楠 四川省肿瘤医院
张 瑜 中南大学湘雅医院
陈 刚 华中科技大学同济医学院附属同济医院
陈晓军 上海市第十人民医院
易 萍 重庆医科大学附属第一医院
金 平 深圳市妇幼保健院
周圣涛 四川大学华西第二医院
郑文新 美国西南医学中心妇科肿瘤病理科
郑 虹 北京大学肿瘤医院
孟元光 中国人民解放军总医院
赵 霞 四川大学华西第二医院
哈春芳 宁夏医科大学总医院
姜 洁 山东大学齐鲁医院
姜 桦 复旦大学附属妇产科医院
娄 阁 哈尔滨医科大学附属肿瘤医院
夏百荣 中国科学技术大学附属第一医院
(安徽省肿瘤医院)
徐丛剑 西湖大学医学院附属杭州市第一人民医院
殷爱军 山东大学齐鲁医院
高庆蕾 华中科技大学同济医学院附属同济医院
郭瑞霞 郑州大学第一附属医院
曹冬焱 中国医学科学院北京协和医院
崔 恒 北京大学人民医院
康 山 河北医科大学附属肿瘤医院
鹿 欣 复旦大学附属妇产科医院
梁志清 重庆医科大学附属第三医院
程文俊 江苏省人民医院
靳英辉 武汉大学中南医院循证与转化医学中心
臧荣余 复旦大学附属中山医院
谭文华 哈尔滨医科大学附属第二医院
参考文献
[1]Sung H,Ferlay J,Siegel R L,et al.Global cancer statistics 2020:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J].CA Cancer J Clin,2021,71(3):209-249
[2]Shaw JL,Nielson CM,Park JK,et al.The incidence of thrombocytopenia in adult patients receiving chemotherapy for solid tumors or hematologic malignancies[J].Eur J Haematol,2021,106(5):662-672
[3]Zhang Y,Yang F,Wang J,et al.Bevacizumab-induced immune thrombocytopenia in an ovarian cancer patient with mixed connective tissue disease:case report and literature review[J].Front Immunol,2024,15:1382964
[4]Leaf RK,Mones JV,Shenoy T,et al.Immune thrombocytopenia in patients treated with immune checkpoint inhibitors[J].Blood,2025 Dec 8:blood.2025031449.doi:10.1182/blood.2025031449.Epub ahead of print
[5]Ozols RF,Bundy BN,Greer BE,et al.Phase III trial of carboplatin and paclitaxel compared with cisplatin and paclitaxel in patients with optimally resected stage III ovarian cancer:a Gynecologic Oncology Group study[J].J Clin Oncol,2003,21(17):3194-3200
[6]Vasey PA,Jayson GC,Gordon A,et al.Phase III randomized trial of docetaxel-carboplatin versus paclitaxel-carboplatin as first-line chemotherapy for ovarian carcinoma[J].J Natl Cancer Inst,2004,96(22):1682-1691
[7]Pignata S,Scambia G,Ferrandina G,et al.Carboplatin plus paclitaxel versus carboplatin plus pegylated liposomal doxorubicin as first-line treatment for patients with ovarian cancer:the MITO-2 randomized phase III trial[J].J Clin Oncol,2011,29(27):3628-3635
[8]Clamp AR,James EC,Mcneish IA,et al.Weekly dose-dense chemotherapy in first-line epithelial ovarian,fallopian tube,or primary peritoneal cancer treatment (ICON8):overall survival results from an open-label,randomised,controlled,phase 3 trial[J].Lancet Oncol,2022,23(7):919-930
[9]Perren TJ,Swart AM,Pfisterer J,et al.A phase 3 trial of bevacizumab in ovarian cancer[J].New Engl J Med,2011,365(26):2484-2496
[10]Mcguire WP,Hoskins WJ,Brady MF,et al.Cyclophosphamide and cisplatin compared with paclitaxel and cisplatin in patients with stage III and stage IV ovarian cancer[J].New Engl J Med,1996,334(1):1-6
[11]Li L,Zhuang Q,Cao Z,et al.Paclitaxel plus nedaplatin vs.paclitaxel plus carboplatin in women with epithelial ovarian cancer:a multi-center,randomized,open-label,phase III trial[J].Oncol Lett,2018,15(3):3646-3652
[12]Pujade-Lauraine E,Wagner U,Aavall-Lundqvist E,et al.Pegylated liposomal Doxorubicin and Carboplatin compared with Paclitaxel and Carboplatin for patients with platinum-sensitive ovarian cancer in late relapse[J].J Clin Oncol,2010,28(20):3323-3329
[13]Pfisterer J,Plante M,Vergote I,et al.Gemcitabine plus carboplatin compared with carboplatin in patients with platinum-sensitive recurrent ovarian cancer:an intergroup trial of the AGO-OVAR,the NCIC CTG,and the EORTC GCG[J].J Clin Oncol,2006,24(29):4699-4707
[14]Mutch DG,Orlando M,Goss T,et al.Randomized phase III trial of gemcitabine compared with pegylated liposomal doxorubicin in patients with platinum-resistant ovarian cancer[J].J Clin Oncol,2007,25(19):2811-2818
[15]Pignata S,Lorusso D,Scambia G,et al.Pazopanib plus weekly paclitaxel versus weekly paclitaxel alone for platinum-resistant or platinum-refractory advanced ovarian cancer (MITO 11):a randomised,open-label,phase 2 trial[J].Lancet Oncol,2015,16(5):561-568
[16]Rose PG,Blessing JA,Mayer AR,et al.Prolonged oral etoposide as second-line therapy for platinum-resistant and platinum-sensitive ovarian carcinoma:a Gynecologic Oncology Group study[J].J Clin Oncol,1998,16(2):405-410
[17]Yuan G,Li Q,Lou G,et al.Final analysis of SCORES,a phase III randomized,double-blinded,placebo-controlled study of suvemcitug combined with chemotherapy for platinum-resistant ovarian cancer[J].J Clin Oncol,2025,43(16_suppl):5554
[18]Moore KN,Angelergues A,Konecny GE,et al.Mirvetuximab soravtansine in FRα-positive,platinum-resistant ovarian cancer[J].New Engl J Med,2023,389(23):2162-2174
[19]Meric-Bernstam F,Makker V,Oaknin A,et al.Efficacy and safety of trastuzumab deruxtecan in patients with HER2-expressing solid tumors:primary results from the DESTINY-PanTumor02 phase II trial[J].J Clin Oncol,2024,42(1):47-58
[20]Miller DS,Filiaci VL,Mannel RS,et al.Carboplatin and paclitaxel for advanced endometrial cancer:final overall survival and adverse event analysis of a phase III trial (NRG Oncology/GOG0209)[J].J Clin Oncol,2020,38(33):3841-3850
[21]Eskander RN,Sill MW,Beffa L,et al.Pembrolizumab plus chemotherapy in advanced endometrial cancer[J].New Engl J Med,2023,388(23):2159-2170
[22]Makker V,Colombo N,Casado Herráez A,et al.Lenvatinib plus Pembrolizumab for advanced endometrial cancer[J].New Engl J Med,2022,386(5):437-448
[23]Hensley ML,Miller A,O'malley DM,et al.Randomized phase III trial of gemcitabine plus docetaxel plus bevacizumab or placebo as first-line treatment for metastatic uterine leiomyosarcoma:an NRG Oncology/Gynecologic Oncology Group study[J].J Clin Oncol,2015,33(10):1180-1185
[24]Colombo N,Dubot C,Lorusso D,et al.Pembrolizumab for persistent,recurrent,or metastatic cervical cancer[J].New Engl J Med,2021,385(20):1856-1867
[25]Peters WA,Liu PY,Barrett RJ,et al.Concurrent chemotherapy and pelvic radiation therapy compared with pelvic radiation therapy alone as adjuvant therapy after radical surgery in high-risk early-stage cancer of the cervix[J].J Clin Oncol,2000,18(8):1606-1613
[26]Mileshkin LR,Moore KN,Barnes EH,et al.Adjuvant chemotherapy following chemoradiotherapy as primary treatment for locally advanced cervical cancer versus chemoradiotherapy alone (OUTBACK):an international,open-label,randomised,phase 3 trial[J].Lancet Oncol,2023,24(5):468-482
[27]Lorusso D,Xiang Y,Hasegawa K,et al.Pembrolizumab or placebo with chemoradiotherapy followed by pembrolizumab or placebo for newly diagnosed,high-risk,locally advanced cervical cancer (ENGOT-cx11/GOG-3047/KEYNOTE-A18):a randomised,double-blind,phase 3 clinical trial[J].Lancet (London,England),2024,403(10434):1341-1350
[28]Wu X,Xia L,Zhang K,et al.Overall survival with camrelizumab plus famitinib versus camrelizumab alone and investigator's choice of chemotherapy for recurrent or metastatic cervical cancer[J].Gynecol Oncol,2024,190:S23-S4
[29]Moore K,Colombo N,Scambia G,et al.Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer[J].New Engl J Med,2018,379(26):2495-2505
[30]Ray-Coquard I,Pautier P,Pignata S,et al.Olaparib plus Bevacizumab as first-line maintenance in ovarian cancer[J].New Engl J Med,2019,381(25):2416-2428
[31]González-Martín A,Pothuri B,Vergote I,et al.Niraparib in patients with newly diagnosed advanced ovarian cancer[J].New Engl J Med,2019,381(25):2391-2402
[32]Li N,Zhu J,Yin R,et al.Treatment with niraparib maintenance therapy in patients with newly diagnosed advanced ovarian cancer:a phase 3 randomized clinical trial[J].JAMA Oncol,2023,9(9):1230-1237
[33]Wu L,Wang J,Li Q,et al.Fuzuloparib with or without apatinib as maintenance therapy in newly diagnosed,advanced ovarian cancer (FZOCUS-1):a multicenter,randomized,double-blind,placebo-controlled phase 3 trial[J].CA Cancer J Clin,2026,76(1):e70042
[34]Wu X,Liu J,Wang J,et al.Senaparib as first-line maintenance therapy in advanced ovarian cancer:a randomized phase 3 trial[J].Nat Med,2024,30(6):1612-1621
[35]Poveda A,Floquet A,Ledermann JA,et al.Olaparib tablets as maintenance therapy in patients with platinum-sensitive relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21):a final analysis of a double-blind,randomised,placebo-controlled,phase 3 trial[J].Lancet Oncol,2021,22(5):620-631
[36]Mirza MR,Monk BJ,Herrstedt J,et al.Niraparib maintenance therapy in platinum-sensitive,recurrent ovarian cancer[J].New Engl J Med,2016,375(22):2154-2164
[37]Wu XH,Zhu JQ,Yin RT,et al.Niraparib maintenance therapy in patients with platinum-sensitive recurrent ovarian cancer using an individualized starting dose (NORA):a randomized,double-blind,placebo-controlled phase III trial[J].Ann Oncol,2021,32(4):512-521
[38]Li N,Zhang Y,Wang J,et al.Fuzuloparib maintenance therapy in patients with platinum-sensitive,recurrent ovarian carcinoma (FZOCUS-2):a multicenter,randomized,double-blind,placebo-controlled,phase III trial[J].J Clin Oncol,2022,40(22):2436-2446
[39]Li N,Bu H,Liu J,et al.An open-label,multicenter,single-arm,phase II study of fluzoparib in patients with germline BRCA1/2 mutation and platinum-sensitive recurrent ovarian cancer[J].Clin Cancer Res,2021,27(9):2452-2458
[40]Wu X,Zhu J,Wang J,et al.Pamiparib monotherapy for patients with germline BRCA1/2-mutated ovarian cancer previously treated with at least two lines of chemotherapy:a multicenter,open-label,phase II study[J].Clin Cancer Res,2022,28(4):653-661
[41]Metcalf RA,Nahirniak S,Guyatt G,et al.Platelet transfusion:2025 AABB and ICTMG international clinical practice guidelines[J].Jama,2025,334(7):606-617
[42]白月婷,苗娅莉,李小平,等.rhTPO治疗妇科恶性肿瘤化疗相关性血小板减少症20例临床分析[J].肿瘤预防与治疗,2009,22(2):142-144,148
[43]陈博,李涛,张军,等.重组人血小板生成素治疗同步放化疗实体瘤患者血小板减少的临床疗效观察[J].癌症进展,2012,10(2):115-119
[44]Tepler I,Elias L,Smith JW,2nd,et al.A randomized placebo-controlled trial of recombinant human interleukin-11 in cancer patients with severe thrombocytopenia due to chemotherapy[J].Blood,1996,87(9):3607-3614
[45]Hatae M,Noda K,Yamamoto K,et al.A clinical study of YM 294 (rhlL-11) in patients with gynecologic cancer[J].Gan To Kagaku Ryoho,2005,32(4):479-487
[46]Al-Samkari H,Munoz C,Geredeli C,et al.Romiplostim versus placebo for chemotherapy-induced thrombocytopenia[J].N Engl J Med,2026,394(11):1061-1073
[47]Ge X,Zhang Q,Zhang H,et al.A phase 2/3 study of romiplostim N01 in chemotherapy-induced thrombocytopenia (CIT)[Z].American Society of Clinical Oncology,2024
[48]Qin S,Wang Y,Yao J,et al.Hetrombopag for the management of chemotherapy-induced thrombocytopenia in patients with advanced solid tumors:a multicenter,randomized,double-blind,placebo-controlled,phase II study[J].Ther Adv Med Oncol,2024,16:17588359241260985
[49]Qin S,Zhang Y,Li H,et al.Hetrombopag for the treatment of chemotherapy-induced thrombocytopenia in advanced solid tumors:a multicenter,randomized,double-blind,placebo-controlled phase III trial[C].American Society of Hematology,2025
[50]Guo Q,An D,Liu T,et al.Efficacy and safety of hetrombopag for PARP inhibitor-induced thrombocytopenia:a phase II open-label,prospective trial[J].HemaSphere,2025,9(S1):PS2247
[51]Xie C,Zhao H,Bao X,et al.Pharmacological characterization of hetrombopag,a novel orally active human thrombopoietin receptor agonist[J].J Cell Mol Med,2018,22(11):5367-5377
[52]Xia X,Zhou H,Zhang H,et al.Hetrombopag plus recombinant human thrombopoietin for chemotherapy-induced thrombocytopenia in patients with solid tumors[J].Res Pract Thromb Haemost,2023,7(7):102231
[53]Cheng Y,Zhai C,Wang Q,et al.Hetrombopag for thrombocytopenia induced by concurrent or sequential chemoradiotherapy in patients with solid tumors:a double-cohort trial[J].BMC Cancer,2025,26(1):55
[54]Kellum A,Jagiello-Gruszfeld A,Bondarenko IN,et al.A randomized,double-blind,placebo-controlled,dose ranging study to assess the efficacy and safety of eltrombopag in patients receiving carboplatin/paclitaxel for advanced solid tumors[J].Curr Med Res Opin,2010,26(10):2339-4236
[55]Winer ES,Safran H,Karaszewska B,et al.Eltrombopag for thrombocytopenia in patients with advanced solid tumors receiving gemcitabine-based chemotherapy:a randomized,placebo-controlled phase 2 study[J].Int J Hematol,2017,106(6):765-776
[56]Al-Samkari H,Kolb-Sielecki J,Safina SZ,et al.Avatrombopag for chemotherapy-induced thrombocytopenia in patients with non-haematological malignancies:an international,randomised,double-blind,placebo-controlled,phase 3 trial[J].Lancet Haematol,2022,9(3):e179-e189
[57]李红梅,余文熙,彭志刚,等.阿伐曲泊帕治疗肿瘤化疗所致血小板减少症的疗效及安全性的回顾性研究[J].肿瘤,2021,41(12):832-839
[58]沈志祥,马军.咖啡酸片治疗肿瘤化疗所致血小板减少症的临床观察[J].中国肿瘤临床,2017,44(17):4
[59]沈阳三生制药有限责任公司.特比澳(重组人血小板生成素注射液)[Z].中国说明书,2025
[60]Xiao Y,Liu J,Huang X E,et al.A clinical study on Juheli (Recombinant Human Interleukin-11) in the second prevention of chemotherapy induced thrombocytopenia[J].APJCP,2016,17(2):485-489
[61]Le Rhun E,Devos P,Houillier C,et al.Romiplostim for temozolomide-induced thrombocytopenia in glioblastoma:the platum trial[J].Neurol,2019,93(19):e1799-e806
[62]Xu Y,Zhu L,Xu Y,et al.Efficacy and safety of hetrombopag for secondary prevention of chemotherapy-induced thrombocytopenia in patients with gynecological malignancies:a prospective,single-center,single-arm study[J].HemaSphere,2024,8(S2):3330
[63]潘博,于雁,胡靖,等.咖啡酸片预防化疗所致血小板减少的临床研究[J].现代肿瘤医学,2013,21(12):3
本文未经《现代妇产科进展》授权禁止转载!
来源:妇产科学进展