
2026年3月,山东大学齐鲁医院刘联教授团队在期刊PLOS One(IF:2.9)在线发表题为:“Patient-derived organoids predict chemotherapy response of locally advanced gastric cancer”的高水平研究论文。
1 论文摘要
局部晚期胃癌(GC)标准辅助化疗的疗效仍不理想,尤其是在印戒细胞癌(SRCC)患者中。亟需可靠的临床前模型来预测治疗反应,而利用患者来源的类器官(PDOs)进行体外药物敏感性检测已成为一种有前景的平台。
本研究建立了来源于局部晚期GC患者的PDOs,并通过下一代测序(NGS)和药物表型分析进行了研究。成功生成了17例GC PDOs,成功率为63%。这些PDOs在组织病理学和遗传特征上高度模拟了其原发肿瘤。药物敏感性测试显示了亚型特异性的反应模式:来源于SRCC的PDOs对表柔比星和紫杉醇敏感,但对5-氟尿嘧啶(5-FU)和奥沙利铂耐药。相比之下,非SRCC PDOs对紫杉醇、表柔比星和奥沙利铂表现出强敏感性。在所有测试药物中,紫杉醇在两种亚型中显示出最高的抑瘤效力。
此外,非SRCC PDOs对5-FU和奥沙利铂的敏感性明显高于SRCC PDOs。PDOs的体外药物表型测试能够准确预测GC患者的临床治疗反应,其敏感性为85.7%,特异性为100%,准确率为90.9%。值得注意的是,体外PDOs对药物敏感的患者,其无病生存期显著长于PDOs耐药的患者(P=0.044)。
这些研究结果强调了GC PDOs作为可靠临床前模型的潜力,能够忠实再现肿瘤的生物学特性和治疗反应,从而为预测个体化治疗结果提供了有价值的工具,推动GC精准肿瘤学的发展。
2 创新点
1. 首次系统验证胃癌患者来源类器官(PDOs)预测局部晚期胃癌化疗反应的临床准确性,敏感性达85.7%,特异性100%,准确率达90.9%。
2. 揭示印戒细胞癌(SRCC)与非印戒细胞癌对化疗药物的差异性反应:SRCC对5-FU和奥沙利铂耐药,但对紫杉醇和表柔比星敏感,为病理亚型特异性治疗提供依据。
3. 建立胃癌PDOs与患者临床结局的直接关联,证实体外药敏结果与患者无病生存期显著相关(P=0.044),为精准医疗提供可靠平台。
4. 通过全外显子测序证实PDOs在组织病理学和基因组特征上忠实再现亲代肿瘤,包括CNV模式、突变谱及TMB/MSI状态,验证其作为临床前模型的可靠性。
5. 提出针对SRCC患者应调整标准化疗方案,支持开展含紫杉醇/表柔比星的辅助化疗随机对照试验,为改善该难治亚型预后提供新策略。
3 科学背景与研究现状
胃癌是全球第五大常见癌症和第四大癌症相关死亡原因,中国约70%患者确诊时已属局部晚期。尽管标准化辅助化疗(如S-1单药或奥沙利铂联合卡培他滨)广泛应用,但疗效仍不理想,3年无病生存率仅50-60%,尤其印戒细胞癌(SRCC)预后更差。现有临床前模型存在明显局限:肿瘤细胞系和3D培养球体因克隆选择丢失遗传异质性;患者来源异种移植瘤(PDX)成本高、成瘤率低且周期长;肿瘤外植体(PDE)和肿瘤碎片(PDTF)虽保留免疫微环境,但传代能力有限,不适合高通量筛选。近年来,患者来源类器官(PDOs)技术取得突破,这类由肿瘤干细胞自组织形成的3D模型能保留亲代肿瘤的形态和遗传特征,具有建立快速、细胞活力高、传代能力强、成本相对较低等优势,且与患者治疗反应高度一致。然而,针对局部晚期胃癌PDOs预测化疗反应的系统性研究仍较缺乏,特别是SRCC等特殊病理亚型的药物敏感性特征尚未明确,亟需建立可靠的个体化治疗预测平台。
4 技术路线与实验方法
1. 样本采集与PDOs建立:2022年9-12月收集27例局部胃癌患者手术切除或活检标本,排除转移性病变,经伦理审批后,将组织分三部分:1/3用于类器官培养,1/3液氮冻存行全外显子测序(WES),1/4%多聚甲醛固定行病理染色。组织经消化酶处理、70μm滤网过滤后,以Matrigel包埋接种于24孔板,使用含Y-27632的胃癌类器官完全培养基培养,每2-3天换液,每2周按1:2-1:3传代。
2. 组织病理学与免疫组化:PDOs及亲代肿瘤经固定、脱水、石蜡包埋后切片,行HE染色及Ki67、CK7、CK20、CDX2免疫组化,验证形态学一致性。
3. 全外显子测序分析:提取基因组DNA进行PE150测序,使用MuTect/Strelka检测SNVs和InDels,Control-FREEC检测CNVs,ANNOVAR注释,MuSiC识别显著突变基因,计算肿瘤突变负荷(TMB)和微卫星不稳定性(MSI)状态。
4. 药物敏感性检测:将PDOs消化为单细胞,以250细胞/孔接种于96孔板,培养4天后加入5-FU、奥沙利铂、SN-38、表柔比星、紫杉醇等临床常用药物,作用4-6天后MTS法检测细胞活力,计算抑制率(IR)和半数抑制浓度(IC50),以IR≥50%判定为敏感。
5. 临床随访与一致性分析:术后每3个月电话随访,记录无病生存期(DFS)和无进展生存期(PFS),对比PDOs药敏结果与患者实际临床反应,计算敏感性、特异性和准确性。
5 结果图
Figure 1展示了研究流程图及胃癌类器官的组织病理学特征。图A示意从患者活检或手术标本到类器官培养、药敏检测及临床反应预测的完整流程;图B显示GC-010类器官在Matrigel中培养9天的动态生长过程,第9天直径达约100μm;图C比较SRCC(GC-014、GC-027)与非SRCC(GC-010、GC-011)类器官的形态学差异,GC-027呈现致密结构;图D的HE染色显示GC-007(SRCC)类器官重现亲代肿瘤的印戒细胞特征(黑箭头),GC-025(非SRCC)类器官呈现囊实性混合结构(蓝箭头);图E的免疫组化证实类器官与亲代肿瘤在Ki67、CK7、CK20和CDX2表达模式上高度一致。
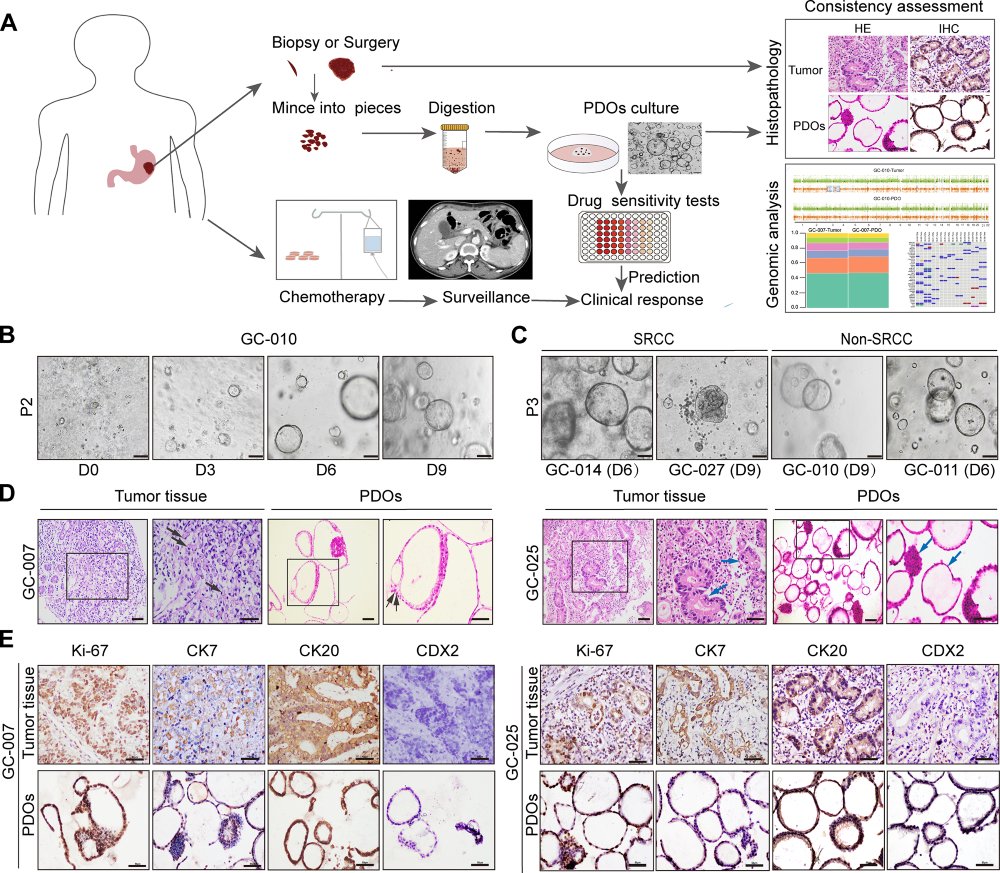
Figure 2展示了胃癌类器官与亲代肿瘤的基因组特征比较。图A热图显示PDOs保留了亲代肿瘤的CNV模式,包括染色体增益(红色)和缺失(蓝色);图B以GC-010和GC-014为例展示全基因组CNV图谱及B等位基因频率分布;图C热图显示PDOs忠实再现亲代肿瘤的常见突变基因(ARID1A、KMT2C、MUC16、BRCA2、TP53等);图D显示PDOs与亲代肿瘤的碱基替换类型分布相似,均以C>T/G>A为主。
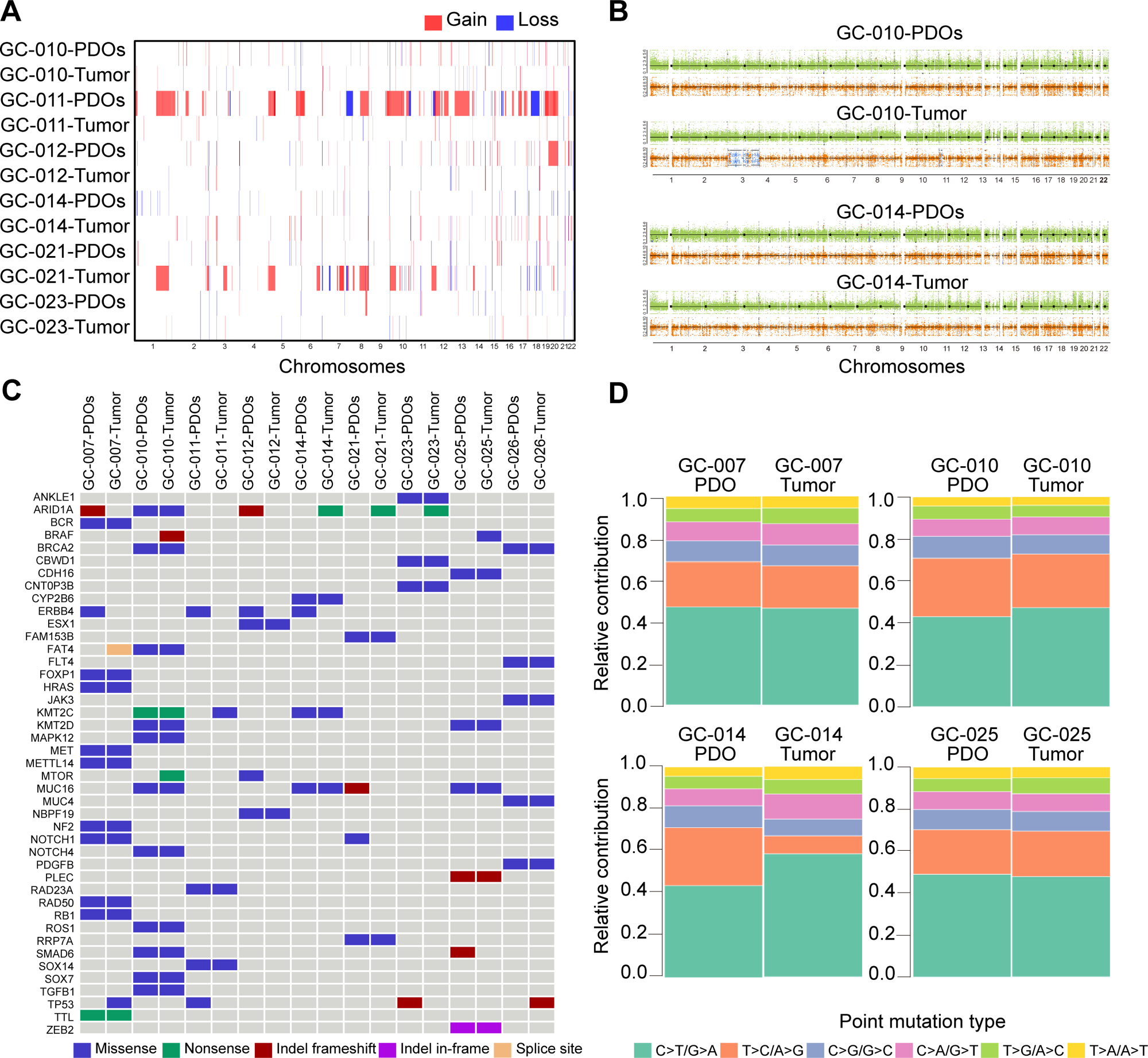
Figure 3展示了胃癌类器官对五种化疗药物的反应。图A-E为13个PDOs的剂量-反应曲线,显示不同类器官对5-FU、奥沙利铂、SN-38、紫杉醇和表柔比星的敏感性存在显著异质性;图F-G的明场图像显示GC-012(非SRCC)对5-FU、奥沙利铂、紫杉醇和表柔比星呈剂量依赖性生长抑制,而GC-014(SRCC)仅对SN-38、紫杉醇和表柔比星敏感,对5-FU和奥沙利铂耐药。
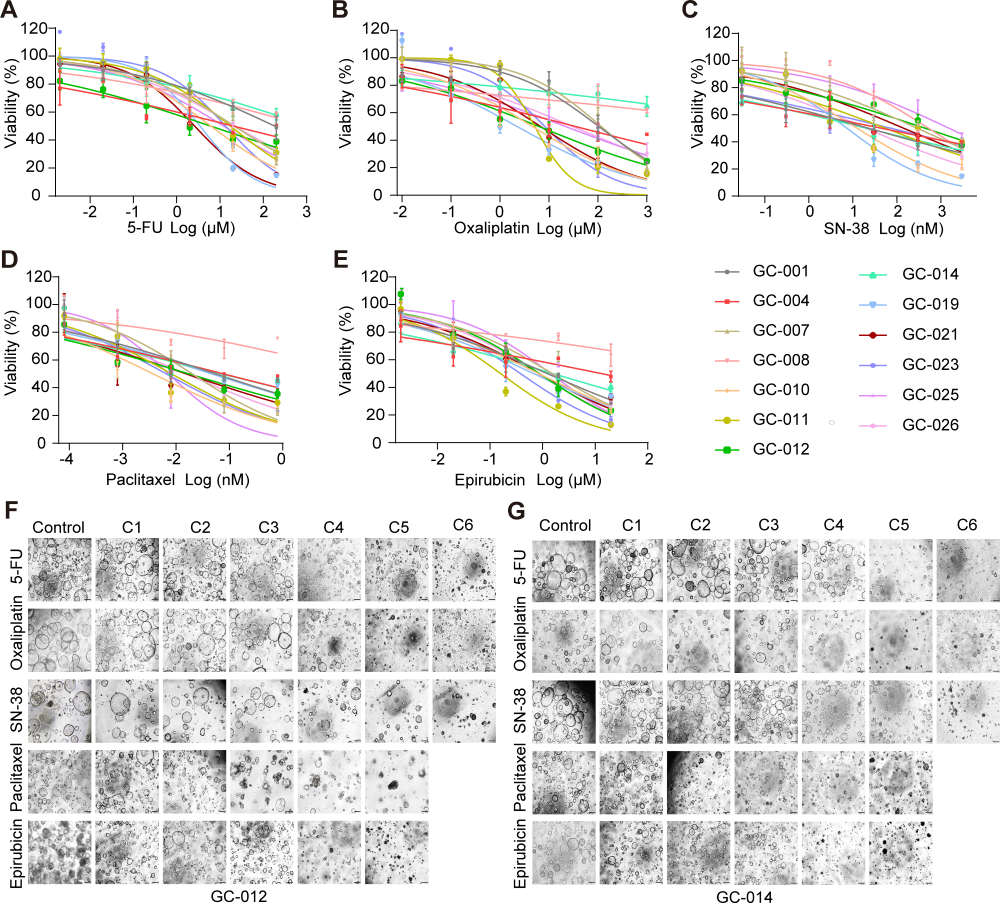
Figure 4展示了药物敏感性定量分析结果。图A热图汇总13个PDOs在稳态血浆浓度下的肿瘤抑制率(IR);图B-C显示SRCC类器官对紫杉醇(59.85%)和表柔比星敏感性最高,显著优于5-FU和奥沙利铂,非SRCC类器官对紫杉醇(59.97%)、奥沙利铂和表柔比星敏感;图D-E显示非SRCC类器官对5-FU(P=0.011)和奥沙利铂(P=0.003)的敏感性显著高于SRCC;图F-H显示两组对SN-38、紫杉醇和表柔比星无显著差异;图I-K的敏感性排序显示紫杉醇和表柔比星在SRCC中排名最优,非SRCC中紫杉醇和表柔比星同样优于5-FU。
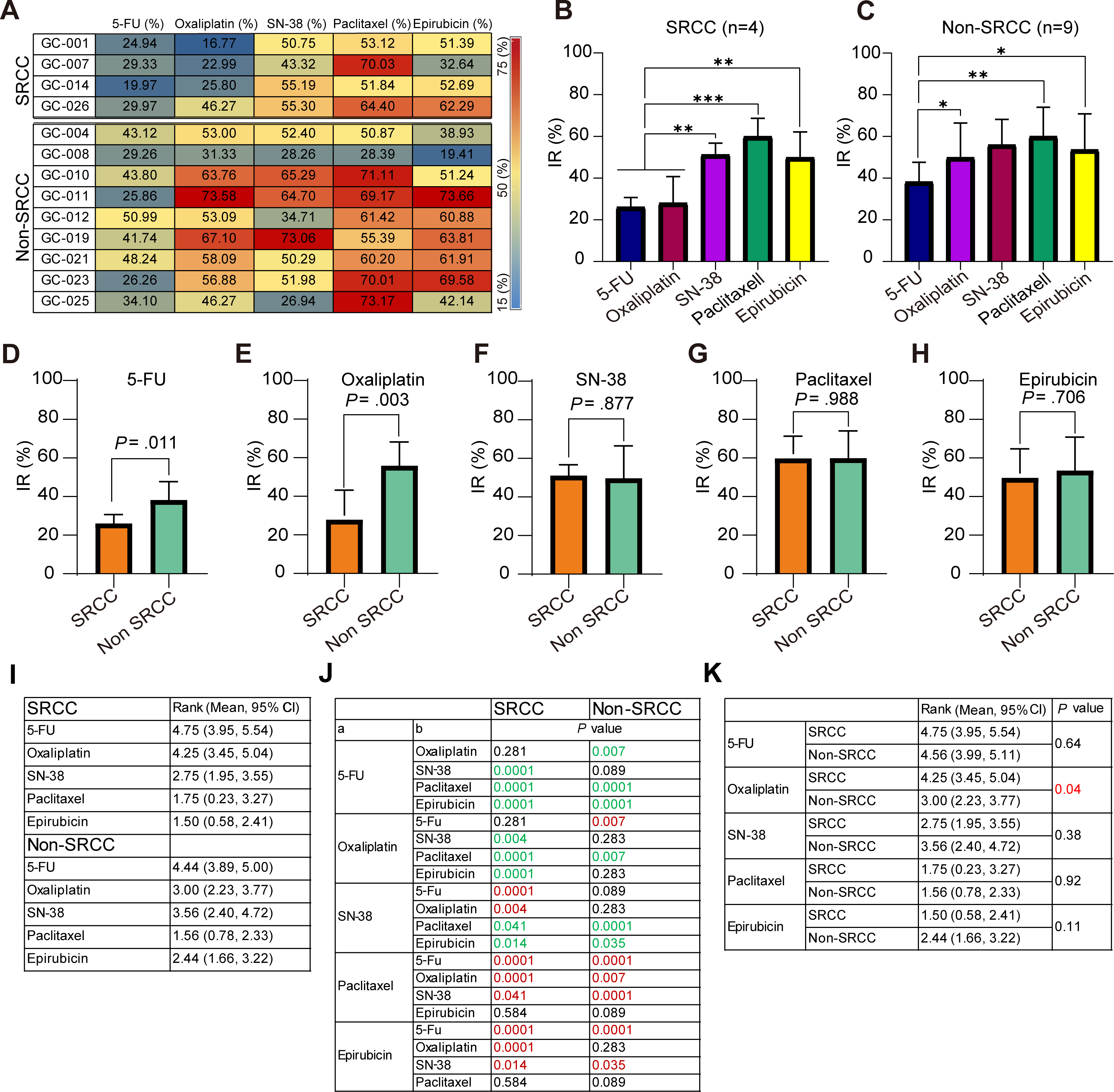
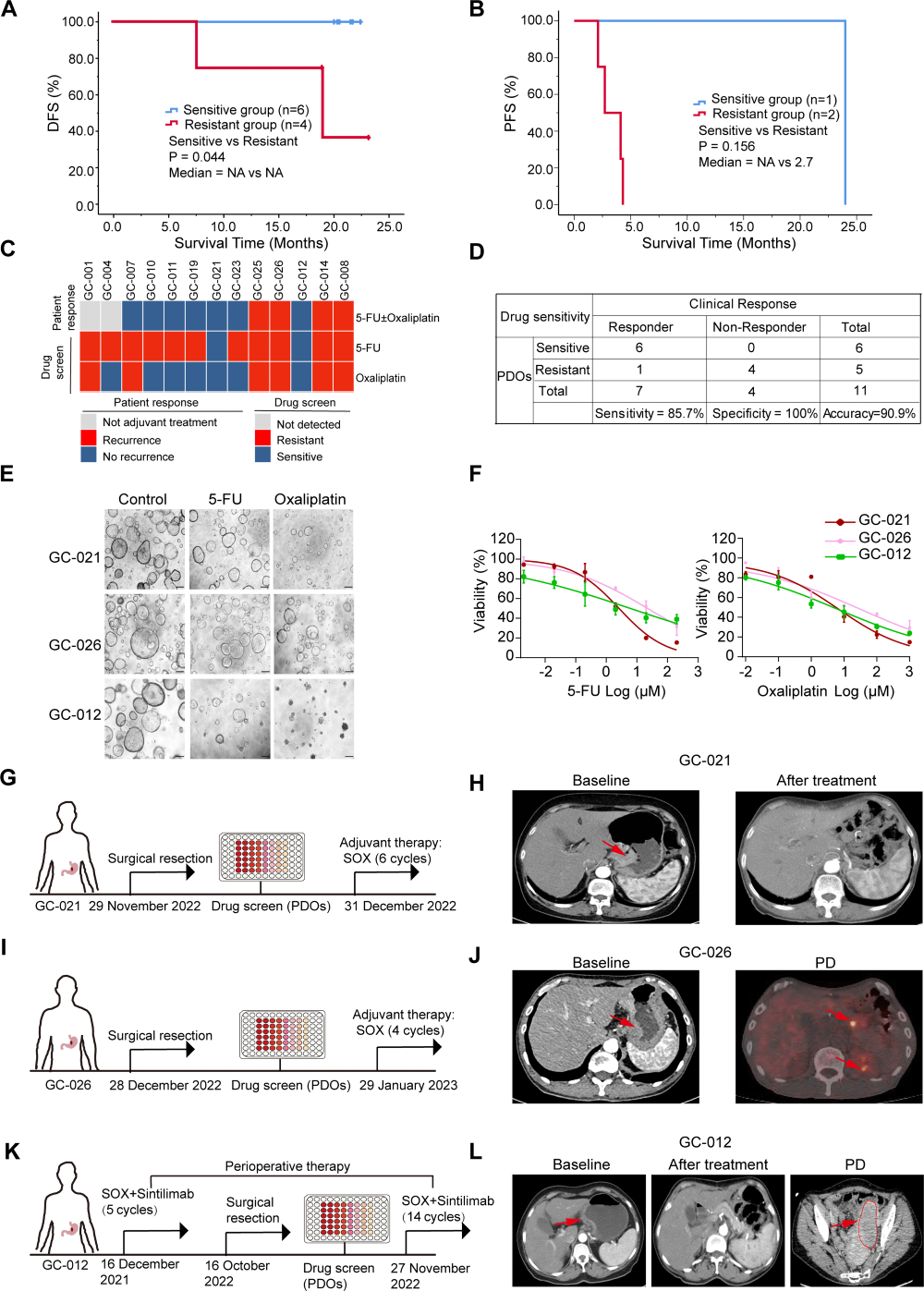
Figure 5展示了PDOs药敏结果与患者临床结局的一致性分析。图A Kaplan-Meier曲线显示PDOs敏感组患者无病生存期显著优于耐药组(P=0.044);图B显示IV期患者中PDOs敏感者无进展生存期达24个月,耐药者仅2.7个月;图C热图汇总13例患者PDOs药敏与临床反应的一致性;图D显示PDOs预测临床反应的敏感性85.7%、特异性100%、准确性90.9%;图E-J展示GC-021(敏感,无复发)、GC-026(耐药,转移)和GC-012(新辅助敏感,PFS 24个月)三个典型病例的治疗时间线、明场图像及CT影像。
专家简介

刘联 教授
山东大学齐鲁医院肿瘤内科主任,教授,博士生导师,主任医师
山东大学齐鲁医学院肿瘤学系副主任
山东省恶性肿瘤精准诊治重点实验室联合PI
山东免疫学会肿瘤分子标志物与靶向治疗专委会主任委员
山东省临床肿瘤学会免疫治疗专委会主任委员
山东省医学伦理学学会肿瘤伦理学分会会长
山东抗癌协会肿瘤心脏病学会主任委员
中华医学会临床流行病学和循证医学分会循证医学学组委员
中国抗癌协会结肠癌专委会内科学组副组长
中国抗癌协会胃癌专委会内科学组委员
CSCO免疫治疗/甲状腺癌/肿瘤营养治疗专家委员会委员
中国人体健康科技促进会肿瘤化疗专委会副主委
中国医药教育学会疑难肿瘤专委会常委
山东抗癌协会、免疫学会、临床肿瘤学会、医药教育学会常务理事
山东省医学会肿瘤学分会兼胃肠肿瘤学组组长/类器官分会副主委
山东医师协会肿瘤科医师分会/化疗医师分会/免疫治疗医师分会副主委
教育部学位中心全国博硕士毕业论文评议专家
山东、浙江、江苏、北京、湖北、深圳科技课题及职称评审外审专家
来源:齐鲁医院肿瘤内科、类器官研究院