
中国医疗保健国际交流促进会肿瘤内科学分会, 中国抗癌协会淋巴瘤专业委员会, 中国医师协会肿瘤医师分会. 中国淋巴瘤诊疗指南(2026版)[J]. 中华肿瘤杂志, 2026, 48(3): 263-309. DOI: 10.3760/cma.j.cn112152-20250605-00260.
淋巴瘤是中国常见的恶性肿瘤之一。淋巴瘤病理类型复杂,异质性强,治疗原则各有不同。近年来,随着对淋巴瘤发生和疾病进展机制的认识不断深入,在诊断和治疗方面取得了诸多新进展,患者生存状况显著改善。为了及时反映淋巴瘤诊断和治疗领域的进展,进一步提高中国淋巴瘤的规范化诊断和治疗水平,中国医疗保健国际交流促进会肿瘤内科学分会、中国抗癌协会淋巴瘤专业委员会和中国医师协会肿瘤医师分会组织专家编写了《中国淋巴瘤诊疗指南(2026版)》,对指南方法学、流行病学数据、临床表现、辅助检查、新药、新治疗方案和新适应证等方面进行了系统、全面地更新,增加了治疗推荐意见和推荐级别,涵盖了淋巴瘤患者诊治过程中常见的临床问题,以便更好地为淋巴瘤患者的规范化诊断和治疗提供借鉴。
【关键词】淋巴瘤;诊断;治疗;指南
淋巴瘤又称恶性淋巴瘤,是一组起源于淋巴造血系统恶性肿瘤的总称,是中国常见恶性肿瘤之一。GLOBOCAN 2022数据显示,2022年全球新发霍奇金淋巴瘤(Hodgkin lymphoma, HL)82409例,居全部恶性肿瘤新发病例排名的第26位,其中男性48753例,女性33656例;死亡22701例,居全部恶性肿瘤死亡病例排名的第28位,其中男性13668例,女性9033例。2022年全球新发非霍奇金淋巴瘤(non-Hodgkin lymphoma, NHL)553010例,居全部恶性肿瘤新发病例排名的第10位,其中男性311157例,女性241853例;死亡250475 例,居全部恶性肿瘤死亡病例排名的第11位,其中男性143624例,女性106851例。2024年中国新发HL 3602例,居全部恶性肿瘤新发病例排名的第28位,其中男性2184例,女性1418例;死亡1331例,居全部恶性肿瘤死亡病例排名的第28位,其中男性858例,女性473例;2024年中国新发NHL 55863例,居全部恶性肿瘤新发病例排名的第14位,其中男性32592例,女性23271例;2022年中国NHL死亡26874例,居全部恶性肿瘤死亡病例排名的第13位,其中男性16994例,女性9880例。
为规范中国淋巴瘤诊疗行为、提高诊疗水平、改善患者预后、保障医疗质量和医疗安全,原国家卫生和计划生育委员会医政医管局委托中国抗癌协会肿瘤临床化疗专业委员会组织专家编写了《中国恶性淋巴瘤诊疗规范(2015年版)》,国家卫生健康委员会医政医管局委托国家癌症中心组织专家编写了《淋巴瘤诊疗规范(2018年版)》。国家卫生健康委员会2022年发布了《淋巴瘤诊疗指南(2022年版)》,后续相关组织还出版了中国抗癌协会《中国肿瘤整合诊治系列指南淋巴瘤分册》《China Anti-Cancer Association (CACA) guidelines for holistic integrative management of lymphoma (version 2022)》《中国淋巴瘤治疗指南(2021年版)》《中国淋巴瘤治疗指南(2023年版)》《中国临床肿瘤协会(CSCO)淋巴瘤诊疗指南2022》《中国临床肿瘤协会(CSCO)淋巴瘤诊疗指南2023》《中国临床肿瘤协会(CSCO)淋巴瘤诊疗指南2024》《中国临床肿瘤协会(CSCO)淋巴瘤诊疗指南2025》《中国肿瘤整合诊治指南(CACA)淋巴瘤(2025年版)》。近年来,人类对淋巴瘤本质认识不断深入,在淋巴瘤诊断和治疗等方面有很多新的研究成果,患者生存得到了显著改善。淋巴瘤是一类以药物治疗为主的疾病,过去十余年中国淋巴瘤治疗药物临床研究取得了长足发展,使中国淋巴瘤患者有了更多的治疗选择。为了及时反映淋巴瘤诊断和治疗领域的进展,进一步提高中国淋巴瘤规范化诊断和治疗水平,中国医疗保健国际交流促进会肿瘤内科学分会、中国抗癌协会淋巴瘤专业委员会和中国医师协会肿瘤医师分会组织专家编写了《中国淋巴瘤诊疗指南(2026版)》。
一 方法学
本指南以“lymphoma”和“malignant lymphoma”作为关键词在 Pubmed、American Association for Cancer Research Annual Meeting、American Society of Clinical Oncology Annual Meeting、European Society for Medical Oncology Congress、American Society of Hematology Annual Meeting、European Hematology Association Congress和International Conference on Malignant Lymphoma Lugano进行检索,筛选了截至2026年3月10日关于淋巴瘤临床研究、荟萃分析、病例报告等文献300余篇,以及2026年3月10日之前获得中国国家药品监督管理局(National Medical Products Administration, NMPA)批准上市的新药、新治疗方案和新适应证。大型随机对照临床研究和严谨的荟萃分析视为高证据级别,小型随机对照临床研究、一般质量的荟萃分析、设计良好的大型回顾性研究和病例对照研究视为稍低证据级别,非对照的单臂临床研究、病例报告和专家观点视为低证据级别。本指南推荐意见由来自肿瘤科、肿瘤内科、血液科、淋巴瘤科、放疗科、病理科、感染科、临床药理中心等科室的专家通过两轮电子邮件审阅后共同决定。75%~100%专家达成共识视为一致推荐,若为高证据级别则为1类推荐,若为稍低证据级别则为2A类推荐;50%~74%专家达成共识视为部分专家推荐,为2B类推荐;<50%专家达成共识视为专家分歧大,为3类推荐。本指南的循证医学推荐级别分类详见表1。本指南供中国肿瘤科、血液科医师和涉及淋巴瘤患者诊疗的相关学科医师参考。

淋巴瘤的诊断主要依靠临床表现、实验室检查、影像学检查、组织病理学和分子病理学检查。组织病理学和分子病理学诊断是决定治疗原则和判断预后的重要依据,是淋巴瘤诊断的金标准。
(一)临床表现
淋巴瘤可表现为局部症状和全身症状。绝大多数HL患者以浅表淋巴结肿大为首发症状。NHL患者大部分以浅表淋巴结肿大为首发症状,部分患者原发于结外淋巴组织或器官。淋巴瘤常见的全身症状有发热、盗汗、体重减轻、皮肤瘙痒和乏力等。以下3种情况中出现任何1种即可诊断为B症状:(1)发热>38.3 ℃,连续3 d以上,排除感染的原因;(2)夜间盗汗;(3)体重于诊断前半年内不明原因下降>10%。
(二)体格检查
体格检查时应注意浅表淋巴结、韦氏环、肝脾的检查以及有无骨骼压痛。淋巴瘤患者肿大的淋巴结多数无痛、表面光滑、质韧饱满,早期大小不等、孤立或散在,后期互相融合、与皮肤粘连、固定或破溃。
(三)辅助检查
推荐意见 1
对于临床表现及影像学检查提示淋巴瘤的患者,应尽早进行肿瘤组织活检以明确病理诊断和分型(1类推荐)。
推荐意见 2
推荐病理诊断为淋巴瘤的患者,进行全身影像学检查,明确累及部位,必要时可结合内镜、超声等检查作为基线(1类推荐)。
1. 实验室检查:患者在治疗前应行血常规、生化常规[包括肝肾功能、乳酸脱氢酶(lactate dehydrogenase, LDH)、碱性磷酸酶、β2-微球蛋白、电解质等]、感染筛查[包括乙型肝炎病毒、丙型肝炎病毒(hepatitis virus C, HCV)、人类免疫缺陷病毒(human immunodeficiency virus, HIV)和梅毒,异常者应进一步检测病毒载量或行确证实验]、红细胞沉降率、免疫球蛋白、爱泼斯坦-巴尔病毒(Epstein-Barr virus, EBV)、巨细胞病毒和骨髓检查等,若存在中枢神经系统(central nervous system, CNS)受累危险因素需行腰椎穿刺,进行脑脊液常规、生化和细胞学检查,必要时可进行脑脊液细胞因子[白细胞介素-6(interleukin-6, IL-6)、IL-10]检查。对于胃淋巴瘤,应行幽门螺杆菌(helicobacter pylori, Hp)检查;对于NK/T细胞淋巴瘤和其他EBV相关淋巴瘤,应行外周血EBV DNA定量检测。
2. 影像学及其他辅助检查:影像学检查包括CT、MRI、正电子发射计算机断层扫描(positron emission tomography-computed tomography, PET-CT)和超声等。其他辅助检查包括心电图、内窥镜和肺功能等。高龄、有心血管系统基础疾病或拟使用蒽环类药物治疗的患者建议行超声心动检查;拟使用博来霉素或既往存在肺基础疾病的患者建议行肺功能检查;病理诊断为NK/T细胞淋巴瘤、黏膜相关淋巴组织淋巴瘤、套细胞淋巴瘤(mantle cell lymphoma, MCL)等胃肠道高受累风险的患者建议行相应内镜检查。采用PET-CT评价疗效时,PET-CT检查结果可能因炎症而出现假阳性,若出现无法解释的局灶性代谢增高,应根据具体情况追加其他检查。怀疑CNS受累的患者,需常规行MRI检查。
3. 病理检查:病理检查是淋巴瘤确诊和分型的金标准。组织活检时,应注意以下几点:(1)淋巴结活检应选择增长迅速、饱满、质韧的肿大淋巴结,尽量完整切除,大肿块或体腔深部病灶可行粗针穿刺活检,避免细针穿刺细胞学检查。(2)尽量选择受炎症干扰较小部位的淋巴结进行活检。如有多个解剖区域的淋巴结病灶,一般宜选择颈部、锁骨上和腋窝淋巴结。(3)术中应避免挤压组织,切取的组织应尽快固定。(4)病理检查应包括形态学、免疫组织化学(immunohistochemistry, IHC),必要时进行荧光原位杂交(fluorescence in situ hybridization, FISH)、流式细胞术、免疫球蛋白(immunoglobulin, Ig)、T细胞受体(T cell receptor, TCR)基因重排和其他分子病理学检测(如二代测序、EBER原位杂交等)。
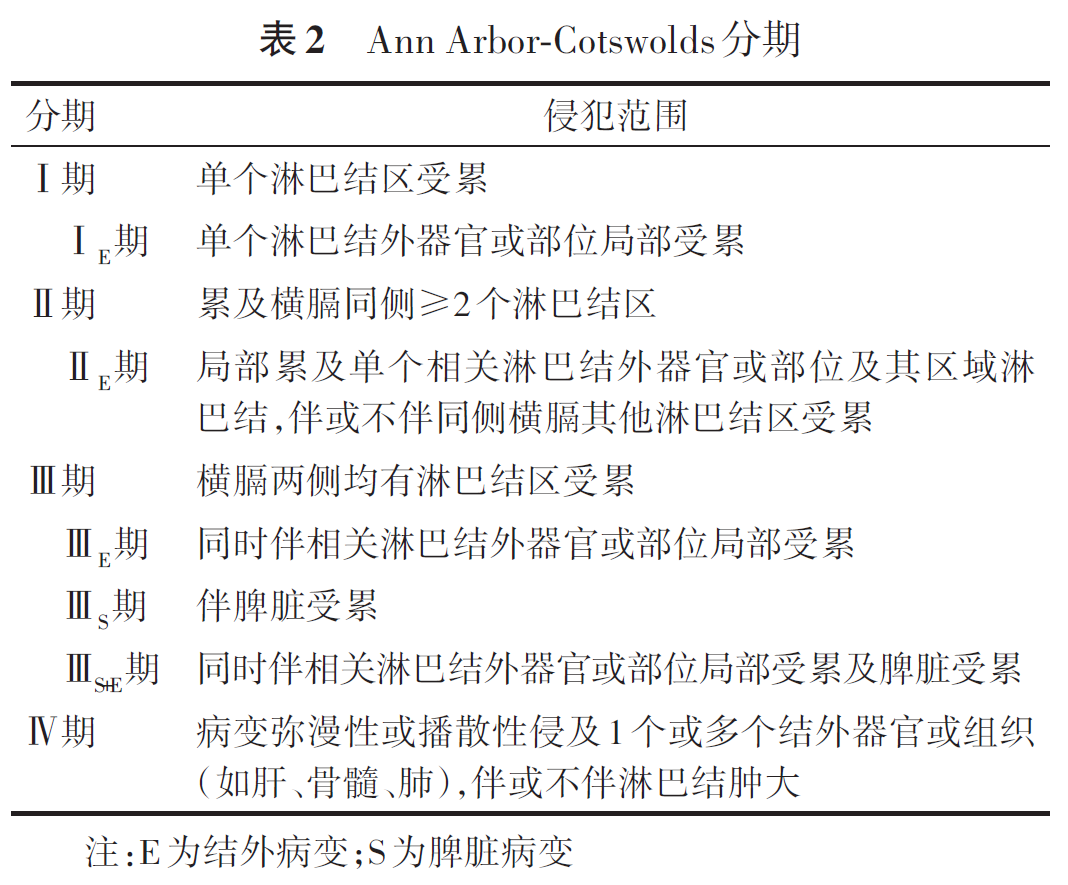
淋巴瘤的临床分期依据疾病侵犯范围采用Ann Arbor-Cotswolds分期系统(表2),同时根据患者的全身症状分为A组(无B症状)和B组(有B症状)。Lugano分期标准对Ann Arbor-Cotswolds分期进行了改良(表3)。某些特殊部位的淋巴瘤采用特定的分期系统,如原发胃肠道淋巴瘤采用Lugano分期系统(表4)。此外,慢性淋巴细胞白血病(chronic lymphocytic leukemia, CLL)采用Binet分期或Rai分期,皮肤蕈样真菌病(mycosis fungoides, MF)和Sézary综合征(Sézary syndrome,SS)采用国际皮肤淋巴瘤协会(International Society for Cutaneous Lymphomas, ISCL)和欧洲癌症研究与治疗组织(The European Organization for Research and Treatment of Cancer, EORTC)皮肤淋巴瘤工作组的TNMB分期,其他原发皮肤淋巴瘤采用ISCL和EORTC皮肤淋巴瘤工作组的TNM分期标准。


四 疗效评价
明确诊断为淋巴瘤的患者,在接受抗淋巴瘤治疗后,应按照计划定期进行疗效评价,根据治疗效果决定后续治疗方案(1类推荐)。
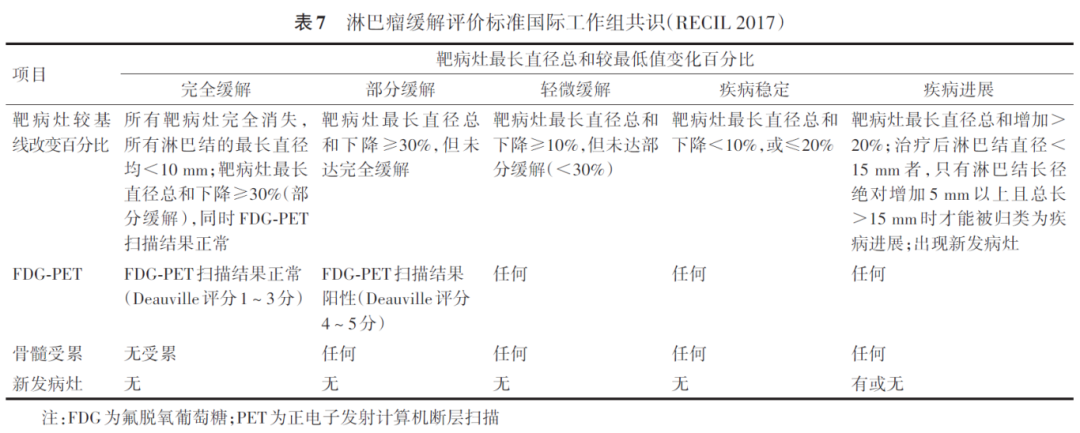
主要采用Lugano淋巴瘤治疗效果评价标准(表5)评价疗效,治疗效果分为基于CT和/或MRI评价的影像学缓解和基于PET-CT评价的代谢缓解,PET-CT评价代谢缓解的依据是多维尔标准的PET 5分法(five-point scale, 5-PS),见表6。淋巴瘤缓解评价标准国际工作组共识(International Working Group consensus response evaluation criteria in lymphoma, RECIL 2017)采用单径测量(表7)。


淋巴瘤病理分类复杂,随着免疫学、分子生物学和临床研究的不断进展,1994年国际淋巴瘤研究组基于大量研究进展,提出了修订的欧美淋巴瘤分类(Revised European-American Lymphoma Classification,REAL),简称“REAL分类”。在REAL分类的基础上,2001年WHO提出了造血和淋巴组织肿瘤分类方案,得到广泛应用和认可,2022年第5版WHO造血淋巴肿瘤分类(5th edition of the WHO Classification of Haematolymphoid Tumours, WHO-HAEM5),与2017年WHO第4修订版造血和淋巴组织肿瘤分类(4th edition of the WHO Classification of Haematolymphoid Tumours,WHO-HAEM4)淋巴瘤部分相比,首次引入瘤样病变概念,结合分子生物学对淋巴瘤分类进一步细化(表8)。





(一)HL
HL发病率占淋巴瘤的5%~10%,男性高于女性。欧美国家HL的发病年龄呈典型的双峰分布,分别为20~30岁和50~70岁。我国HL发病年龄较低,中国医学科学院肿瘤医院回顾性分析结果显示,中位发病年龄为30岁(14~83岁),美国监测、流行病学和最终结果(The Surveillance, Epidemiology, and End Results, SEER)数据库HL中位发病年龄为36岁(14~98岁)。HL病因不详,部分与EBV感染有关。HL分为经典型霍奇金淋巴瘤(classic Hodgkin lymphoma, cHL)和结节性淋巴细胞为主型霍奇金淋巴瘤(nodular lymphocyte predominant Hodgkin lymphoma, NLPHL)。cHL约占HL的90%,可分为4种组织学亚型,即结节硬化型、富于淋巴细胞型、混合细胞型和淋巴细胞消减型。
1. 临床表现
90%的HL以淋巴结肿大为首发症状,颈部淋巴结是最常见的受累部位,多表现为质韧无痛淋巴结肿大。纵隔淋巴结也是常见受累部位,大部分患者以淋巴结肿大压迫引起的症状就诊。随着病情进展可逐渐扩散到其他淋巴结区域,但较少出现淋巴结跳跃性受累。HL可累及脾、肝、骨等,部分患者可伴有B症状、乏力、皮肤瘙痒等症状,血沉增快、贫血、白蛋白降低、血清LDH升高多见于肿瘤负荷较大、肿瘤生长速度较快的患者。
2. 病理诊断
HL有独特的病理特征,在炎症细胞和反应性细胞所构成的微环境中散在分布少量里-施(Reed-Sternberg, R-S)细胞及变异型R-S细胞。典型R-S细胞为双核或多核巨细胞,核仁嗜酸性,大而明显,细胞质丰富;若细胞表现为对称的双核时则称为“镜影细胞”。NLPHL中典型R-S细胞少见,肿瘤细胞因细胞核大、折叠,似“爆米花样”,故又称为“爆米花细胞”或“淋巴细胞性和/或组织细胞性R-S细胞变型细胞”。诊断HL应常规检测的IHC标志物包括:CD45(LCA)、CD20、CD15、CD30、PAX5、CD3、MUM1、Ki-67和EBER。cHL常表现为CD30(+)、CD15(+/-)、PAX5(弱+)、MUM1(+)、CD45(-)、CD20(-/弱+)、CD3(-)、BOB1(-)、OCT2(-/+)、部分患者EBER(+)。NLPHL常表现为CD20(+)、CD79ɑ(+)、BCL6(+)、CD45(+)、CD3(-)、CD15(-)、CD30(-)、BOB1(+)、OCT2(+)、EBV-EBER(-)。在进行鉴别诊断时需要增加相应的标志物检查,以鉴别间变性大细胞淋巴瘤(anaplastic large cell lymphoma, ALCL)或弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma, DLBCL)等。
3. 治疗
(1)一线治疗
推荐意见 4
cHL患者一线治疗2~3周期后需要进行PET-CT检查评价疗效,根据结果调整后续治疗方案和治疗周期(1类推荐)。
①cHL患者的一线治疗
国际上几个权威研究机构对早期cHL的不良预后因素进行了研究(表9),不同研究机构对于早期和晚期cHL的定义有所不同。Ⅰ~Ⅱ期cHL患者推荐化放疗综合治疗,单纯化疗的局部复发率高,但化放疗综合治疗与单纯化疗患者的总生存时间(overall survival, OS)相似。Ⅲ~Ⅳ期cHL患者采用化疗为主的综合治疗。

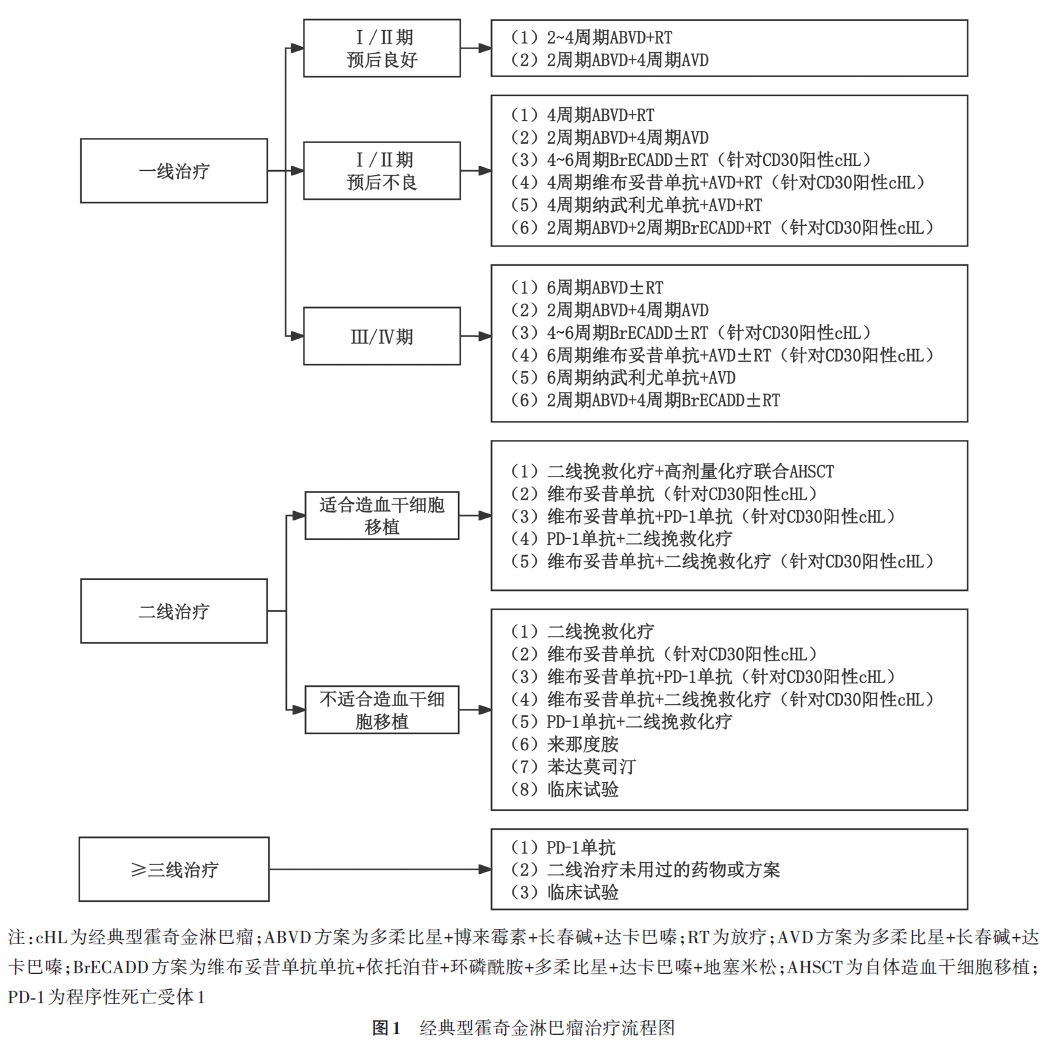
(a)Ⅰ~Ⅱ期cHL患者的治疗:在无PET-CT指导治疗时代,Ⅰ~Ⅱ期预后良好的cHL标准治疗为2~4个周期ABVD方案(多柔比星+博来霉素+长春碱+达卡巴嗪)化疗+20 Gy放疗;Ⅰ~Ⅱ期预后不良的cHL推荐4个周期ABVD方案化疗+30 Gy放疗。建议采用中期PET-CT指导后续治疗,预后良好组:2周期ABVD方案治疗后,PET-CT阴性者,继续行1~2周期ABVD方案治疗后行20 Gy放疗或4周期AVD(多柔比星+长春碱+达卡巴嗪)方案治疗;PET-CT阳性者,行活检或2周期ABVD方案治疗后再次PET-CT评价疗效,若为阴性则行30 Gy放疗,若仍为阳性,则按照难治cHL治疗。预后不良组:2周期ABVD方案治疗后,PET-CT阴性者,继续行2周期ABVD方案治疗后行30 Gy放疗或4周期AVD方案治疗;PET-CT阳性者,行活检或可继续2周期ABVD方案治疗或调整为BrECADD(维布妥昔单抗单抗+依托泊苷+环磷酰胺+多柔比星+达卡巴嗪+地塞米松)方案治疗2周期后再次PET-CT评价疗效,若为阴性,则行30 Gy放疗,若仍为阳性,则按照难治cHL治疗。此外,Ⅰ~Ⅱ期预后不良的cHL患者还可考虑N(纳武利尤单抗)-AVD+RT(放疗)方案、Bv(维布妥昔单抗)+AVD方案治疗。
(b)Ⅲ~Ⅳ期cHL患者的治疗:推荐6个周期ABVD方案化疗,对残留病变给予放疗。也可考虑Bv+AVD方案、N-AVD方案、BrECADD±RT方案治疗。建议采用中期PET-CT指导后续治疗,接受2个周期ABVD方案化疗后PET-CT阴性的患者可继续接受ABVD方案或AVD方案化疗;PET-CT阳性的患者后续需要选择高强度方案化疗,如BrECADD方案。基于ECHELON-1研究结果,美国食品药品监督管理局(Food and Drug Administration, FDA)于2018年3月21日批准Bv+AVD方案用于CD30阳性Ⅳ期HL成人患者的一线治疗(图1)。
②NLPHL患者的一线治疗
NLPHLⅠ~Ⅱ期患者多见,大肿块、纵隔淋巴结受累及B症状少见。90%以上的Ⅰ~Ⅱ期NLPHL患者可长期生存。相较于Ⅰ~Ⅱ期NLPHL,Ⅲ~Ⅳ期患者预后较差,出现大肿块、腹腔受累或脾脏受累的患者,初期或后期转变为大细胞淋巴瘤的风险较高。Ⅲ~Ⅳ期NLPHL采用以化疗±R(利妥昔单抗)为主的综合治疗。
(a)无大肿块的ⅠA或ⅡA期NLPHL患者的治疗:无大肿块的ⅠA或邻近病灶的ⅡA期患者推荐受累部位放疗(involved site radiotherapy, ISRT);孤立淋巴结病变经完整手术切除后的ⅠA期患者可以选择随诊观察;NLPHL行单纯化疗的研究数据较少,除了参加临床试验,不推荐对此类NLPHL患者行单纯化疗;利妥昔单抗单药治疗复发率高,不推荐单独使用。
(b)ⅠA或ⅡA期伴大肿块,ⅠB或ⅡB期,或病灶相距较远的ⅡA 期NLPHL患者的治疗:推荐短程化疗(2~4个月)+利妥昔单抗+ISRT,化疗方案包括:ABVD方案、CHOP方案(环磷酰胺+多柔比星+长春新碱+泼尼松)和CVbP方案(环磷酰胺+长春碱+泼尼松)等。
(c)Ⅲ~Ⅳ期NLPHL患者的治疗:Ⅲ~Ⅳ期NLPHL可选择化疗+利妥昔单抗±ISRT,化疗方案包括ABVD方案、CHOP方案和CVbP方案等;对于不耐受化疗的患者,也可选择利妥昔单抗单药治疗;有症状的局部病灶可选择姑息性放疗;若患者无任何症状,也可以选择随诊观察。
(2)复发或难治HL患者的治疗
推荐意见 5
复发或难治cHL患者,如符合自体造血干细胞移植(autologous hematopoietic stem cell transplantation, AHSCT)条件,可在解救方案治疗后行高剂量化疗联合AHSCT治疗;如不符合AHSCT条件,可行传统二线及后线解救方案治疗(1类推荐)。
①复发或难治cHL患者的治疗:符合AHSCT条件的复发或难治cHL患者,先接受二线解救方案治疗,疗效达完全缓解(complete response, CR)的患者行AHSCT,未达CR患者接受后线系统治疗联合或不联合放疗后再次评价是否可进行AHSCT。移植后高复发风险患者可考虑维布妥昔单抗维持治疗(最多16个周期),维布妥昔单抗维持治疗可以延长患者的无进展生存时间(progression-free survival, PFS)。移植后高复发风险因素包括:一线治疗未达CR、复发时间距初次缓解时间<12个月,或复发时结外受累。ⅠA或ⅡA期患者,若一线治疗未行放疗,复发时间距末次治疗结束≥12个月且原位复发,可考虑单纯放疗。
不适合AHSCT的复发或难治cHL患者进行传统二线解救方案治疗,包括DHAP方案(地塞米松+顺铂+阿糖胞苷)、GDP方案(吉西他滨+顺铂+地塞米松)、GVD方案(吉西他滨+长春瑞滨+脂质体阿霉素)、ICE方案(异环磷酰胺+卡铂+依托泊苷)、IGEV方案(异环磷酰胺+吉西他滨+依托泊苷+泼尼松)、BeGEV方案(苯达莫司汀+吉西他滨+长春瑞滨)、GemOx方案(吉西他滨+奥沙利铂)和MINE方案(依托泊苷+异环磷酰胺+美司钠+米托蒽醌)等。在一些小样本的前瞻性研究中,新药加入二线解救方案的CR率超过60%。这些方案包括维布妥昔单抗+苯达莫司汀、维布妥昔单抗+纳武利尤单抗、维布妥昔单抗+ICE方案、帕博利珠单抗+ICE方案、帕博利珠单抗+GVD方案、纳武利尤单抗序贯ICE方案、信迪利单抗+ICE方案。AHSCT后复发患者预后不佳。美国FDA于2011年8月19日批准维布妥昔单抗用于治疗AHSCT治疗失败的HL或至少应用2种以上化疗方案且不适合进行AHSCT的HL患者。基于CheckMate 039和CheckMate 205研究结果,美国FDA于2016年5月17日,批准纳武利尤单抗用于治疗AHSCT和/或维布妥昔单抗治疗后复发或难治cHL。基于KEYNOTE-087研究结果,美国FDA于2017年3月14日批准帕博利珠单抗用于治疗AHSCT和/或维布妥昔单抗治疗后复发或难治cHL。基于5项关键性注册临床试验,NMPA分别于2018年12月27日、2019年5月29日、2019年12月27日、2021年8月5日和2021年8月30日批准信迪利单抗、卡瑞利珠单抗、替雷利珠单抗、派安普利单抗和赛帕利单抗上市,用于治疗二线系统化疗后复发或难治cHL。此外,在应用帕博利珠单抗或维布妥昔单抗治疗复发或难治HL的KEYNOTE-204研究中,帕博利珠单抗中位PFS显著长于维布妥昔单抗。中国NMPA于2020年5月14日批准维布妥昔单抗用于治疗复发或难治CD30阳性HL或ALCL。
三线治疗失败或者一、二线治疗时已经应用过程序性死亡受体1(programmed cell death-1, PD-1)单抗或者维布妥昔单抗的患者,无标准治疗,可以考虑参加临床试验、对症支持治疗或者其他药物如来那度胺或苯达莫司汀(图1)。
②复发或难治NLPHL患者的治疗:复发或难治NLPHL患者推荐再次进行病灶活检,以排除是否转化为侵袭性淋巴瘤。若没有转化,可根据具体情况,选择随诊观察,或者利妥昔单抗单药治疗,或者利妥昔单抗+二线解救化疗方案±放疗。二线解救化疗方案包括DHAP方案、ICE方案、IGV方案(异环磷酰胺+吉西他滨+长春瑞滨)、ABVD方案(若一线未使用)、CHOP方案(若一线未使用)、CVbP方案(若一线未使用)、苯达莫司汀等。
4. 预后因素和生存
Ⅰ~Ⅱ期cHL的不良预后因素见表9,不同研究机构定义的不良预后因素略有差别。
Ⅲ~Ⅳ期cHL最常用的预后评价系统为国际预后评分,包括7个不良因素,分别为:①白蛋白<40 g/L;②血红蛋白<105 g/L;③男性;④年龄≥45岁;⑤Ⅳ期病变;⑥白细胞增多,白细胞计数≥15×109/L;⑦淋巴细胞减少,占白细胞比例<8%和/或淋巴细胞计数<0.6×109/L。每增加1个不良因素,复发风险增加7%~8%。
中期PET-CT检查:2~3个周期化疗后PET-CT阴性的患者预后明显优于PET-CT阳性的患者。
中国医学科学院肿瘤医院2000—2018年接受标准一线治疗的HL患者的回顾性分析结果显示,10年淋巴瘤特异性生存(lymphoma-specific survival, LSS)率和OS率分别为91.7%和87.1%,在校正预后相关因素后,中国医学科学院肿瘤医院和同期美国SEER数据库HL患者的LSS和OS差异无统计学意义。
(二)DLBCL
DLBCL是所有NHL中最常见的类型,在美国占成人NHL的32.5%,在中国占NHL的36.2%。中国医学科学院肿瘤医院2005—2018年DLBCL患者的回顾性分析结果显示,中位发病年龄为54岁(12~91岁),≤60岁和>60岁患者分别占65.7%和34.3%;同期美国SEER数据库DLBCL患者中位发病年龄为63岁(12~96岁),≤60岁和>60岁患者分别占45.1%和54.9%。
1. 病理诊断及分类
诊断DLBCL常规IHC标志物包括CD19、CD20、PAX5、CD3、CD5、CD79α、CyclinD1、Ki-67等;通常表现为CD19(+)、CD20(+)、PAX5(+)、CD3(-);对具体亚型的诊断应遵循WHO-HAEM5。根据细胞起源的不同将DLBCL分为3类,即生发中心B细胞样(germinal center B-cell like, GCB)、活化B细胞样(activated B-cell-like, ABC)和第3型DLBCL(Type 3 DLBCL)。临床上通常采用Hans分型进行分类,分为GCB型及非生发中心B细胞样(non-germinal center B-cell like, non-GCB)型,其中GCB型的IHC表现为:(1)CD10(+)、不论BCL-6和MUM1表达如何;(2)CD10(-)、BCL-6(+)、MUM1(-)。其他情况均为non-GCB型。明确诊断及分期后,应行FISH检测BCL-2、MYC基因重排,还应行IHC检测以明确BCL-2、MYC的表达情况,这将有助于判断患者预后并选择治疗方案。高级别B细胞淋巴瘤伴MYC和BCL-2基因易位,其遗传学特征为同时存在MYC和BCL-2基因重排;双表达DLBCL指MYC和BCL-2的IHC表达阳性(MYC蛋白表达≥40%,BCL-2蛋白表达≥50%);两者均提示预后不良。二代基因测序检测发现,MYD88和CD79b双突变、TP53突变、NOTCH1突变提示预后不良。较为广泛应用的基因分型方式将DLBCL分为MCD、N1、A53、BN2、ST2、EZB MYC+、EZB MYC-和其他亚型。另外,还有C0-C5分型等多种分型方式。
2. 预后指标
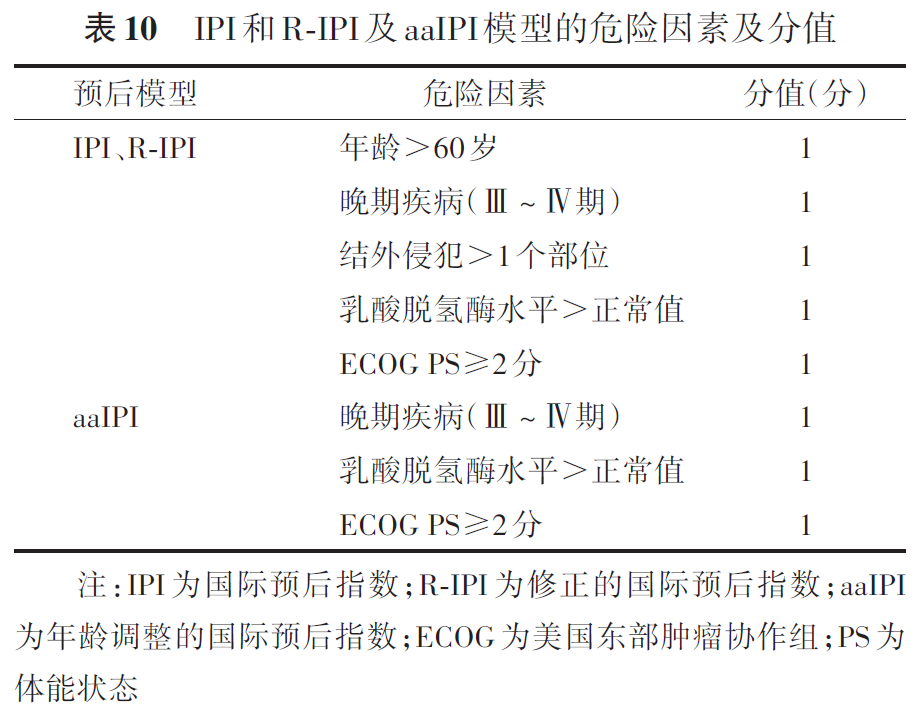
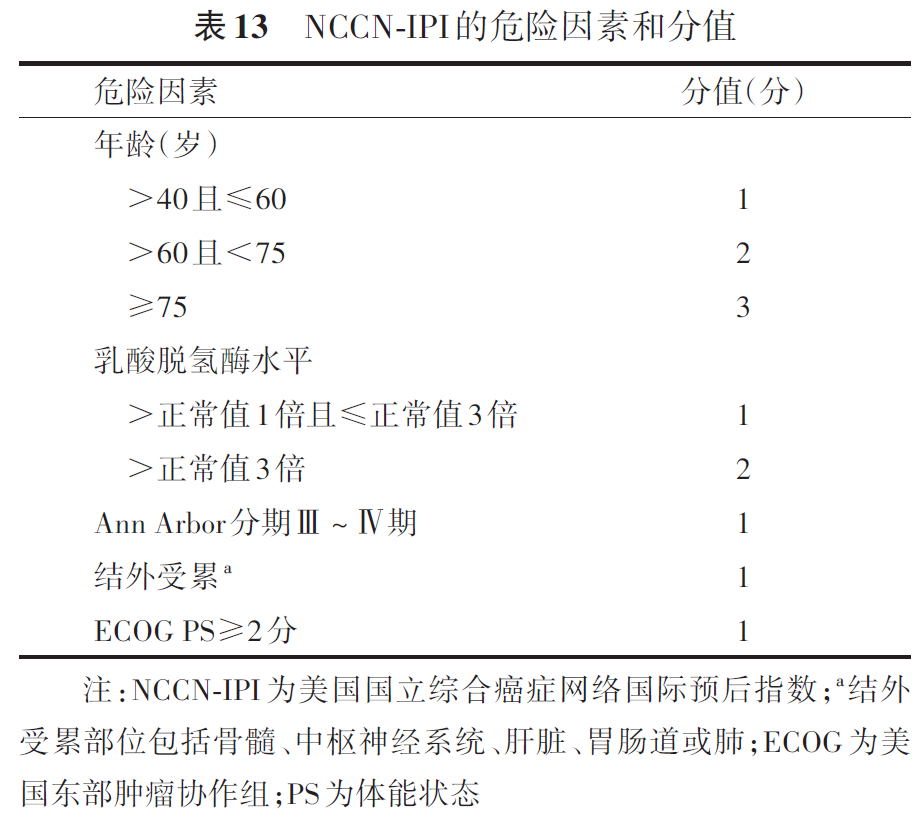
国际预后指数(international prognostic index, IPI)是DLBCL患者预后的经典评价系统,年龄调整的IPI(age adjusted IPI, aaIPI)适合≤60岁的患者。IPI和aaIPI中的每个危险因素计为1分(表10、11)。利妥昔单抗时代形成的修正的IPI(revised international prognostic index,R-IPI)被认为能够更好地预测患者的预后,R-IPI 0分为预后非常好组;R-IPI 1~2分为预后好组;R-IPI 3~5分为预后差组(表12)。在IPI基础上将年龄和LDH进一步分层形成的NCCN-IPI,能更准确地预测患者预后[低危组(0~1分),低中危组(2~3分),中高危组(4~5分),高危组(≥6分),表13]。基于临床因素建立的新的风险预后模型和自身抗体等生物标志物也可以用于DLBCL患者的疗效和预后判断。


3. 治疗
DLBCL的治疗模式是以内科治疗为主的综合治疗。内科治疗包括化疗、靶向治疗及免疫治疗,应综合考虑患者年龄、疾病分期、病理类型和分子遗传学特征等来制定治疗方案。
(1)DLBCL患者的一线治疗
DLBCL患者一线治疗推荐R-CHOP(利妥昔单抗+环磷酰胺+多柔比星+长春新碱+泼尼松)或R-CHOP样方案,对于IPI评分≥2分的患者,可以考虑Pola-R-CHP方案[维泊妥珠单抗(polatuzumab vedotin, pola)+利妥昔单抗+环磷酰胺+多柔比星+泼尼松],必要时联合放疗。
CNS受累风险高的DLBCL患者,建议进行CNS预防治疗。
DLBCL患者的初始治疗应根据年龄、身体状况、疾病分期、病理类型、分子遗传学特征等采取个体化治疗策略。如果有合适的临床试验,建议患者参加。对于肿瘤负荷较高的患者,建议采取预防措施,例如在正式治疗开始前给予泼尼松±长春新碱作为前期治疗,以预防发生肿瘤溶解综合征。此外,应尽量避免由于骨髓抑制导致的治疗药物剂量降低。对于以治愈为目的或年龄>60岁的高危患者可以预防性应用重组人粒细胞刺激因子,以尽可能避免发热性中性粒细胞减少症的发生。聚乙二醇化重组人粒细胞刺激因子每个化疗周期应用1次就可以有效预防化疗导致的中性粒细胞减少症的发生。
①Ⅰ~Ⅱ期DLBCL患者的一线治疗:Ⅰ~Ⅱ期无大肿块(肿块最大径<7.5 cm)的DLBCL患者可选择4个周期R-CHOP方案或化疗后序贯2个周期利妥昔单抗单药治疗,或4~6个周期R-CHOP方案±ISRT。Ⅰ~Ⅱ期伴有大肿块(肿块最大径≥7.5 cm)的DLBCL患者选择6个周期R-CHOP方案±ISRT。Ⅱ期伴广泛肠系膜侵犯者参照Ⅲ~Ⅳ期患者的治疗(图2)。
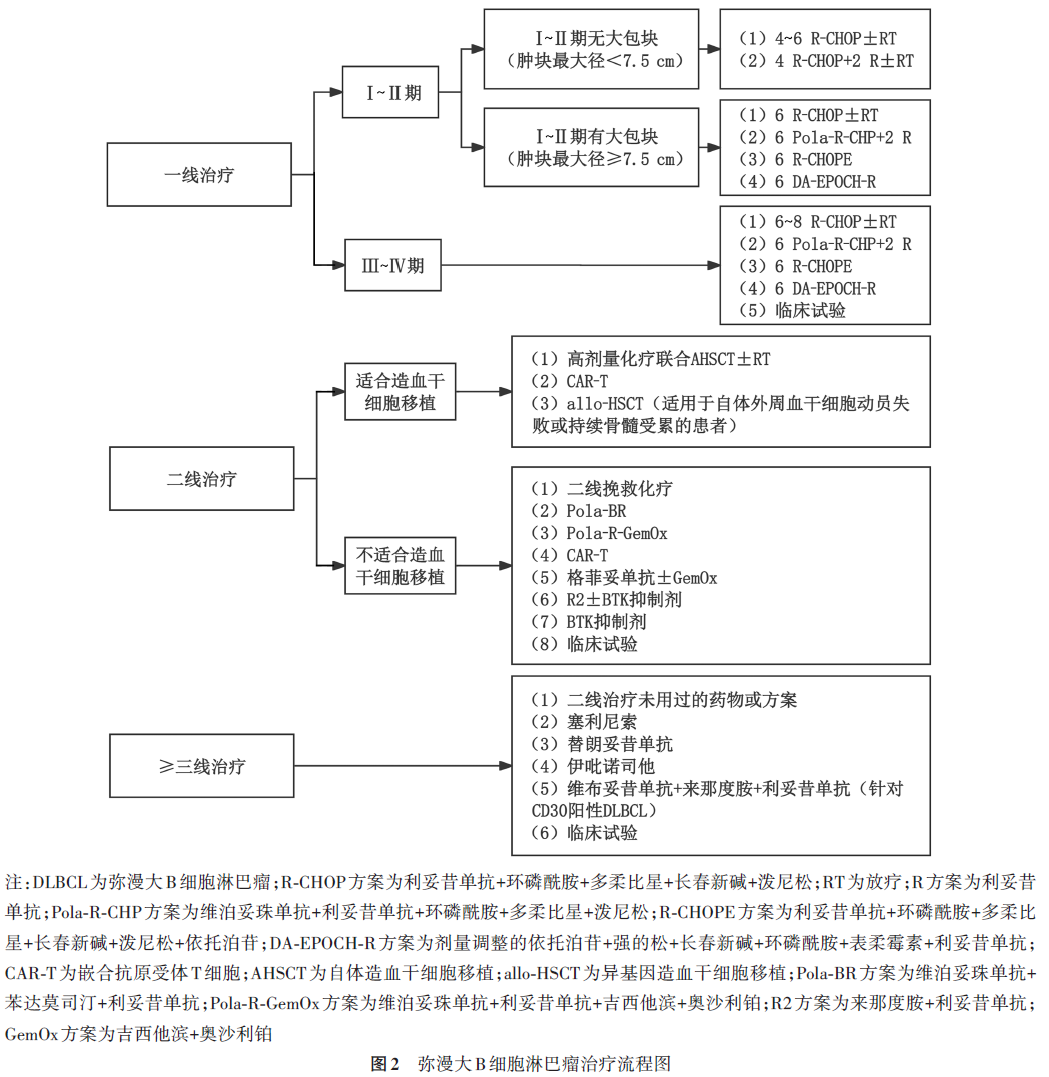
②Ⅲ~Ⅳ期DLBCL患者的一线治疗:对于Ⅲ~Ⅳ期DLBCL患者推荐R-CHOP方案治疗,如有合适的临床试验,建议患者参加。R-CHOP方案治疗2~4个周期后应全面复查确认疗效,若治疗无效,建议再次活检,并参考复发或难治DLBCL患者的治疗方案;若治疗有效,疗效评价为CR或部分缓解(partial response, PR),则继续R-CHOP方案化疗至6个周期。POLARIX研究结果显示,Pola-R-CHP方案较R-CHOP方案可显著提高IPI>1分的初治DLBCL患者的2年PFS率,但两组2年OS率差异无统计学意义。2023年1月13日CD79b的抗体偶联药物维泊妥珠单抗获得中国NMPA批准上市,联合R-CHP方案用于既往未经治疗的DLBCL成人患者。2025年11月25日利妥昔单抗被中国NMPA批准联合维泊妥珠单抗、环磷酰胺、多柔比星和泼尼松用于治疗既往未经治疗的DLBCL成人患者。60~80岁的患者在使用一线R-CHOP方案治疗达到CR或PR后可考虑来那度胺维持治疗(图2)。
③特殊类型DLBCL患者的一线治疗:存在MYC/BCL2双表达的DLBCL患者:一线可选择西达本胺联合R-CHOP方案治疗,治疗有效的患者序贯西达本胺维持治疗24周。对于体力状况较差或年龄>80岁的Ⅰ~Ⅱ期DLBCL患者,可选择R-mini-CHOP方案(利妥昔单抗+减低剂量的CHOP方案)或R-CDOP方案(利妥昔单抗+环磷酰胺+脂质体阿霉素+长春新碱+强的松)等治疗。蒽环类药物不能耐受的患者,可选择R-GCVP方案(利妥昔单抗+吉西他滨+环磷酰胺+长春新碱+泼尼松)或R-CEOP方案(利妥昔单抗+环磷酰胺+依托泊苷+长春新碱+强的松)等。体力状态欠佳且肿瘤负荷高的DLBCL患者,可以在足量化疗开始前给予低剂量的诱导治疗,药物包括泼尼松±长春新碱,以预防肿瘤溶解综合征的发生。对于表面抗原阳性的患者应密切监测外周血乙型肝炎病毒DNA含量,并给予抗乙型肝炎病毒治疗。对于伴有CNS受累的DLBCL患者,若为脑实质受累,需加用静脉高剂量甲氨蝶呤(≥3 g/m2);若为脑膜受累,需行鞘内注射甲氨蝶呤或阿糖胞苷,也可在R-CHOP方案化疗的基础上加用静脉滴注3~3.5 g/m2的甲氨蝶呤,或在R-CHOP+甲氨蝶呤或阿糖胞苷鞘内注射后采用静脉滴注甲氨蝶呤作为巩固治疗。对于CNS受累风险高的DLBCL患者,如CNS-IPI高危[伴有4~6个CNS受累的危险因素:年龄>60岁、LDH升高、Ⅲ~Ⅳ期、美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)体能状态(performance status, PS)>1分、结外病变>1个、肾或肾上腺受累]、HIV相关淋巴瘤、伴MYC和BCL2重排的高级别B细胞淋巴瘤、原发睾丸DLBCL、原发皮肤DLBCL腿型、伴有危险因素(双侧乳腺受累、肿物>5 cm、IPI评分高、LDH升高、ECOG PS评分差)的原发乳腺DLBCL等,应进行CNS预防治疗。预防治疗的方法仍存在争议,可在全身治疗中或治疗后采用鞘内注射4~8次甲氨蝶呤或阿糖胞苷,或者在全身治疗过程中或一线治疗结束后静脉滴注3~3.5 g/m2甲氨蝶呤2~4个周期进行预防性治疗。
即使是Ⅰ期的原发睾丸DLBCL患者,CNS和对侧睾丸复发风险也同样较高。因此,对于原发睾丸DLBCL患者,在完成一线治疗后,推荐使用鞘内注射甲氨蝶呤±阿糖胞苷或高剂量甲氨蝶呤静脉化疗以及对侧睾丸局部放疗(25~30 Gy),分别预防CNS和对侧睾丸复发。原发纵隔大B细胞淋巴瘤患者的最佳一线治疗尚存在争议,推荐利妥昔单抗和蒽环类药物联合方案治疗,可选择的治疗包括DA-EPOCH-R方案(剂量调整的依托泊苷+强的松+长春新碱+环磷酰胺+表柔霉素+利妥昔单抗)、R-CHOP方案±ISRT或R-CHOP续贯R-ICE方案±ISRT等。治疗后残余纵隔肿块常见,推荐化疗结束时采用PET-CT进行评价,PET阴性(5-PS评分1~3分)的患者可以免去放疗进入后续密切随诊观察,PET阳性(5-PS评分4~5分)的患者建议进行局部组织重新活检以除外假阳性如治疗后炎症反应、胸腺增生等。如果PET阳性(5-PS评分4分)但局部组织活检病理阴性,则采取随诊观察;PET阳性(5-PS评分4分)且病理阳性或者PET阳性(5-PS评分5分)病理阴性患者则补充30~40 Gy ISRT;PET阳性(5-PS评分5分)且病理阳性的患者按照难治患者处理。伴MYC和BCL2重排的高级别B细胞淋巴瘤患者常伴有不良预后因素,如LDH增高、骨髓受累、CNS受累和高IPI评分等。伴MYC和BCL2重排的高级别B细胞淋巴瘤患者尚无推荐的标准一线治疗方案,首先推荐参加合适的临床试验,也可采用强化治疗方案,如DA-EPOCH-R方案、R-HyperCVAD/MA方案(利妥昔单抗+环磷酰胺+长春新碱+多柔比星+地塞米松与利妥昔单抗+高剂量甲氨蝶呤+阿糖胞苷交替使用)、R-CODOX-M/R-IVAC方案(利妥昔单抗+环磷酰胺+长春新碱+多柔比星联合甲氨蝶呤与异环磷酰胺+依托泊苷+阿糖胞苷交替使用),但是需要考虑药物不良反应,评价患者的体能状态和合并症。高级别B细胞淋巴瘤患者CNS复发和受累风险较高,推荐进行CNS预防性治疗。原发CNS的DLBCL患者推荐含高剂量甲氨蝶呤(≥3.5 g/m2)的联合方案,包括甲氨蝶呤+利妥昔单抗方案、R-MA方案(利妥昔单抗+甲氨蝶呤+阿糖胞苷)、MATRix方案(甲氨蝶呤+阿糖胞苷+塞替派+利妥昔单抗)、R-MT方案(利妥昔单抗+甲氨蝶呤+替莫唑胺)、BTK抑制剂+甲氨蝶呤±利妥昔单抗方案等。不能耐受高剂量甲氨蝶呤的患者可选用其他方案化疗。对于化疗达CR的年轻患者,进行减量的全脑放疗或AHSCT或高剂量阿糖胞苷±依托泊苷或含高剂量甲氨蝶呤的联合方案进行巩固治疗,老年患者可不行全脑放疗。
(2)复发或难治患者的治疗
复发难治DLBCL患者,如缓解时间>12个月且符合AHSCT条件,可行解救方案治疗后行高剂量化疗联合AHSCT;如缓解时间<12个月或原发难治DLBCL患者可考虑嵌合抗原受体T细胞(chimeric antigen receptor T cell, CAR-T)治疗;如缓解时间>12个月但不符合AHSCT条件的DLBCL患者,可行传统二线及后线解救方案治疗(1类推荐)。
复发或难治DLBCL患者根据获得缓解时间长短(是否>12个月)和是否符合AHSCT条件进行分层治疗,可选择其他与CHOP无交叉耐药的药物或个体化治疗方案。如果患者具备AHSCT条件且达到了CR或PR,则行AHSCT;如果患者不具备AHSCT条件或治疗后仍为疾病稳定(stable disease, SD)或疾病进展(progressive disease, PD),则可考虑其他治疗方案治疗或行最佳支持治疗。在任何情况下,如果条件允许,推荐参加临床试验。
①缓解时间>12个月且符合AHSCT条件的DLBCL患者:如果患者获得缓解时间>12个月且符合AHSCT条件,应首先接受二线治疗,方案包括DHA(地塞米松、阿糖胞苷)+铂类(卡铂、顺铂或奥沙利铂)±R、GDP±R方案、GemOx±R方案、ICE±R方案、ESHAP方案(依托泊苷+甲泼尼龙+顺铂+阿糖胞苷)±R、MINE±R方案等。若达CR,可选择AHSCT±ISRT或参加合适的临床试验,如果患者有接受异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation, allo-HSCT)的适应证,可行allo-HSCT。若为PR,则可选择CD19 CAR-T治疗,或AHSCT±ISRT,或参加临床试验,如果患者有接受allo-HSCT的适应证,可行allo-HSCT。若为SD或PD,则可选择CD19 CAR-T治疗,或参加合适的临床试验,或选择其他治疗方案,或姑息性ISRT,或最佳支持治疗。基于ZUMA-1研究和JULIET研究,美国FDA分别于2017年10月20日和2018年5月1日批准阿基仑赛(Yescarta)和tisagenlecleucel (Kymriah)用于至少接受过二线治疗的复发或难治DLBCL、转化型滤泡淋巴瘤和高级别B细胞淋巴瘤患者的治疗。基于TRANSCEND研究,美国FDA于2021年3月26日批准lisocabtagene mraleucel(Juno Therapeutics)用于至少接受过二线治疗的复发或难治大B细胞淋巴瘤(包括DLBCL和惰性淋巴瘤转化的DLBCL)患者的治疗。2021年6月23日中国NMPA批准阿基仑赛上市,适用于既往接受二线或以上系统性治疗后复发或难治大B细胞淋巴瘤(包括DLBCL非特指型、原发纵隔大B细胞淋巴瘤、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的DLBCL)成人患者的治疗。2021年9月1日中国NMPA批准瑞基奥伦赛(Carteyva)上市,用于经过二线或以上系统性治疗后复发或难治大B细胞淋巴瘤成人患者的治疗。2025年7月30日中国NMPA批准雷尼基奥仑赛上市,用于经过二线及以上系统治疗后的复发或难治大B细胞淋巴瘤成人患者的治疗(图2)。
②缓解时间<12个月或原发难治的DLBCL患者:可考虑接受CAR-T治疗。
③缓解时间>12个月但不符合AHSCT条件的DLBCL患者:若患者不符合AHSCT条件,则可选择参加合适的临床试验、二线治疗、姑息性ISRT,或最佳支持治疗。不符合AHSCT条件的患者经过治疗后疗效评价如为CR,进入临床随诊期;如疗效评价为PR、SD或PD,可选择CD19 CAR-T治疗、参加临床试验、选择其他治疗方案、姑息性ISRT,或最佳支持治疗。二线治疗方案包括GemOx±R方案、Pola±苯达莫司汀±利妥昔单抗、坦昔妥单抗+来那度胺方案、DA-EPOCH±R方案、BeGEV方案(苯达莫司汀+吉西他滨+长春瑞滨)、CEOP±R方案、GDP±R方案、MINE±R方案、利妥昔单抗单药方案。
特殊情况下可选择的治疗包括维布妥昔单抗(适用于CD30阳性的DLBCL)、R2方案(来那度胺±利妥昔单抗,适用于non-GCB型DLBCL)、伊布替尼(适用于non-GCB型DLBCL)、BR方案(苯达莫司汀+利妥昔单抗)、格菲妥单抗、格菲妥单抗+GemOx、伊吡诺司他(双利司他)等。另外,基于GO29365研究,维泊妥珠单抗于2019年6月10日被美国FDA批准上市,于2023年1月13日被中国NMPA批准上市,用于与BR方案联合治疗不适合AHSCT的复发或难治DLBCL成人患者。2025年11月25日利妥昔单抗被中国NMPA批准联合苯达莫司汀和维泊妥珠单抗用于不适合接受造血干细胞移植的复发或难治DLBCL成人患者。2026年3月10日,中国NMPA批准维泊妥珠单抗联合利妥昔单抗、吉西他滨和奥沙利铂方案,用于不适合AHSCT的复发或难治DLBCL成人患者。CD20/CD3 T细胞结合双特异性抗体格菲妥单抗于2023年6月15日被美国FDA批准上市,2023年11月8日被中国NMPA批准上市,用于治疗既往接受过至少两线系统性治疗的复发或难治DLBCL成人患者。基于L-MIND研究,CD19单抗坦昔妥单抗于2020年7月31被美国FDA批准上市,2025年5月22日被中国NMPA批准上市,适应证为与来那度胺联合治疗不适合移植的复发或难治DLBCL成人患者(包括DLBCL非特指型、低级别淋巴瘤转化的DLBCL)。基于LOTIS-2研究,loncastuximab于2021年4月23日被美国FDA批准上市,适应证为二线或以上系统性治疗后复发或难治大B细胞淋巴瘤成人患者(包括DLBCL 非特指型、低级别淋巴瘤转化的DLBCL、高级别B细胞淋巴瘤)。基于SADAL研究,塞利尼索于2022年6月22日被美国FDA批准上市,于2024年7月5日被中国NMPA批准上市,适应证为二线或以上系统性治疗后的复发或难治DLBCL成人患者(包括DLBCL非特指型、滤泡淋巴瘤转化的DLBCL)。2024年12月10日靶向CD19的抗体偶联药物替朗妥昔单抗(曾用名:泰朗妥昔单抗)被中国NMPA批准上市,适应证为二线或多线系统治疗后的复发或难治大B细胞淋巴瘤成年患者。基于ECHELON-3研究,2025年2月11日维布妥昔单抗联合来那度胺和利妥昔单抗方案被美国FDA批准用于二线或以上系统性治疗后,且不符合AHSCT或CAR-T治疗条件的复发或难治DLBCL患者。2025年6月30日靶向HDAC和PIK3CA的伊吡诺司他(双利司他)被中国NMPA批准上市,适应证为二线以上系统性治疗后复发或难治DLBCL患者(图2)。
此外,中国自主研发的CD20单克隆抗体瑞帕妥单抗于2022年8月23日被中国NMPA批准上市,用于治疗IPI为0~2分的初治CD20阳性DLBCL成人患者,应与CHOP方案联合治疗。泽贝妥单抗于2023年5月12日获中国NMPA批准上市,用于与标准CHOP方案联合治疗CD20 阳性非特指性DLBCL成人患者。
4. DLBCL患者的随诊
若患者治疗结束后疗效评价为CR,则进入随诊阶段,此后2年内每3个月复查1次,第3~5年每6个月复查1次,5年后每年复查1次,终身随诊。当临床出现可疑复发征象时应立即检查,对于新出现的病灶应尽量进行活检,以明确病理诊断。
为了解决利妥昔单抗的可及性问题,近年来利妥昔单抗生物类似药的研发成为药物研发的热点之一。中国已经上市了3款利妥昔单抗生物类似药,分别是汉利康®(HLX01)、达伯华®(IBI301)和TQB2303,这些药物的临床研究结果显示,在药代动力学、临床疗效、安全性和免疫原性等方面,生物类似药与原研药物高度相似,临床上可替代使用。
中国医学科学院肿瘤医院2005—2018年接受R-CHOP或R-CHOP样标准一线治疗的DLBCL患者的回顾性研究结果显示,5年PFS率和5年OS率分别为61.7%和70.6%。中国医学科学院肿瘤医院的回顾性研究结果显示,与原发结外DLBCL患者相比,原发结内DLBCL具有更好的预后;在原发小肠DLBCL患者中,与单独使用R-CHOP相比,R-CHOP联合手术治疗具有更好的预后。
(三)滤泡淋巴瘤(follicular lymphoma, FL)
FL是一类较为常见的惰性NHL,在美国占NHL患者的17.1%,在中国占NHL患者的2.9%。中国医学科学院肿瘤医院2008—2018年进展期FL患者的回顾性研究结果显示,中位发病年龄为49岁(18~78岁)。患者主要表现为多发淋巴结肿大,也可累及骨髓、外周血、脾脏、韦氏环、胃肠道和软组织等,原发结外者少见。
1. 病理诊断
FL来源于生发中心的B细胞,形态学上表现为肿瘤细胞部分保留了滤泡生长的模式,WHO根据每个高倍镜视野内中心母细胞数量,将FL进一步分为1~3级。1级FL:每个高倍镜视野内中心母细胞数量为0~5个;2级FL:每个高倍镜视野内中心母细胞数量为6~15个;3级FL:每个高倍镜视野内中心母细胞数量>15个。其中,仍保留少数中心细胞为3a级,中心母细胞呈片状分布、不见中心细胞者为3b级。1~3a级FL患者临床表现为惰性,3b级FL患者的治疗原则按照DLBCL进行。任何分级的FL中出现DLBCL成分,应诊断为DLBCL,并按照DLBCL进行治疗。WHO-HAEM5将FL进一步分为原位滤泡B细胞肿瘤、FL、儿童型FL、十二指肠型FL、原发皮肤滤泡中心淋巴瘤。
FL典型的免疫表型为CD20(+)、CD23(+/-)、CD10(+)、CD43(-)、BCL-2(+)、BCL-6(+)、CD5(-)、CCND1(-),部分病例可以出现BCL-2(-)或CD10(-)。同时应该检查Ki-67指数。FISH检测显示85%的FL存在t(14;18)及其相关的IGH-BCL2融合基因。
2. 治疗
FL患者按照分期进行分层治疗和管理,分期常采用Ann Arbor分期系统。
(1)一线治疗
Ⅰ期和局限Ⅱ期的初治FL患者首先推荐ISRT,非局限Ⅱ期的FL患者,可以选择CD20单抗±化疗+ISRT。Ⅲ~Ⅳ期FL无治疗指征的患者可以考虑观察等待,有治疗指征的患者可以考虑CD20单抗单药或联合化疗或来那度胺治疗(1类推荐)。
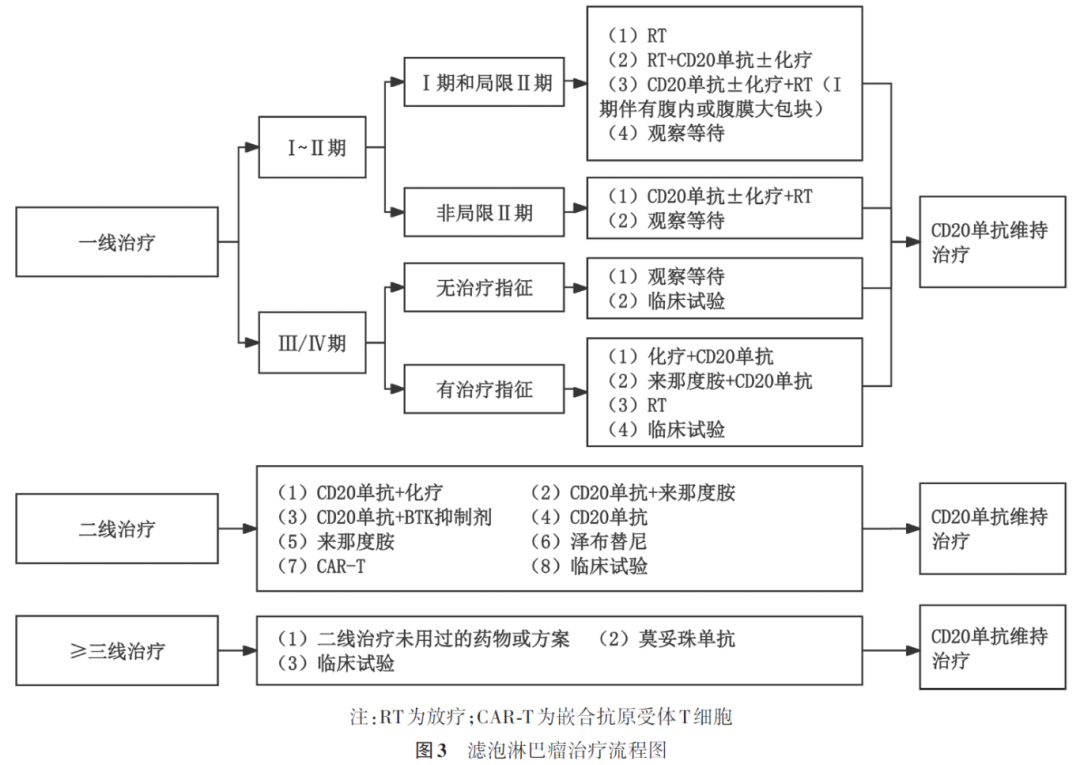
①Ⅰ~Ⅱ期FL患者:Ⅰ期和局限Ⅱ期FL患者首先推荐ISRT,放疗联合全身治疗(CD20单抗单药治疗或者CD20单抗+化疗)组的无失败生存和PFS优于单纯放疗组,但OS差异无统计学意义。对于Ⅰ期伴有腹腔内或腹膜大肿块者,也可考虑CD20单抗±化疗+ISRT。对于非局限Ⅱ期FL患者,可选择CD20单抗±化疗+ISRT,若治疗不良反应大于获益,也可以考虑观察等待(图3)。
②Ⅲ~Ⅳ期FL患者:Ⅲ~Ⅳ期FL患者治疗前需要评价是否具有治疗指征,治疗指征包括出现肿瘤相关症状、器官功能障碍、肿瘤引起的全血细胞减少、肿瘤负荷大(超过3个淋巴结区受累且每个淋巴结区至少存在1个长径≥3 cm的淋巴结,或任何一个淋巴结或结外肿块长径≥7 cm)、疾病持续进展和参加合适的临床试验。观察等待是无治疗指征Ⅲ~Ⅳ期FL患者首先推荐的治疗策略,采取观察等待的患者应每3~6个月复查随诊1次。有治疗指征的Ⅲ~Ⅳ期FL患者,可以选择的治疗方案包括单纯化疗、CD20单抗单药或联合其他药物治疗、参加合适的临床试验或局部放疗。总体治疗原则是根据患者年龄、体能状态、合并症和治疗目标,个体化地选择治疗方案。基于GALLIUM研究结果,美国FDA于2017年11月16日批准奥妥珠单抗联合化疗治疗初治的成人Ⅱ期伴大肿块、Ⅲ~Ⅳ期FL患者。中国NMPA于2021年6月3日批准奥妥珠单抗上市,与化疗联用,随后用奥妥珠单抗维持治疗,用于初治FL患者;或与苯达莫司汀联用,随后用奥妥珠单抗维持治疗,用于利妥昔单抗或含利妥昔单抗方案治疗无缓解、治疗期间或治疗后疾病进展的FL患者。用于治疗FL的多药联合方案主要有利妥昔单抗(R)+苯达莫司汀或奥妥珠单抗(G)+苯达莫司汀、R-CHOP或G-CHOP方案、R-CVP(环磷酰胺+长春新碱+泼尼松)或G-CVP方案、R+来那度胺或G+来那度胺方案等。低肿瘤负荷的患者可考虑利妥昔单抗单药治疗。老年患者、体能状态差且无法耐受较强化疗的患者可选择利妥昔单抗单药、苯丁酸氮芥±利妥昔单抗或环磷酰胺±利妥昔单抗方案。
由于FL具有进展缓慢、反复复发的特点,诱导或解救治疗获得缓解后采用维持治疗会延长缓解时间、降低复发率。推荐用于维持治疗的药物为利妥昔单抗375 mg/m2,每8周1次,维持2年。EORTC 20981研究结果显示,与观察组相比,利妥昔单抗维持治疗能延长复发或难治FL患者的PFS。PRIMA研究结果显示,对于一线免疫化疗后的FL患者,与观察组相比,利妥昔单抗维持治疗能够显著延长PFS。奥妥珠单抗1000 mg 每8周1次,维持2年,也可以作为维持治疗方案。GALLIUM研究结果显示,与接受R-CHOP后R维持的患者相比,接受G-CHOP后G维持的患者PFS显著延长(图3)。
(2)复发或难治患者的治疗
复发或难治FL患者可考虑CD20单抗单药或联合化疗、苯达莫司汀、来那度胺、泽布替尼、莫妥珠单抗等方案。CD20单抗作为巩固和维持治疗方案(1类推荐)。
对于复发或难治FL患者,应重新进行病灶活检,明确是否存在组织学转化。对于病理确认的复发或难治FL患者,需要判断患者是否存在治疗指征,对于无治疗指征的患者,可观察等待。对于具有治疗指征的患者,选择二线治疗方案或者参加合适的临床试验。二线及后线治疗方案需要根据既往治疗方案的疗效、缓解持续时间、患者年龄、体能状态等情况进行综合考虑。可选择的二线治疗方案包括:利妥昔单抗+苯达莫司汀或奥妥珠单抗+苯达莫司汀方案、R-CHOP或G-CHOP方案、R-CVP或G-CVP方案、R2或奥妥珠单抗+来那度胺方案、利妥昔单抗单药、奥妥珠单抗单药、泽布替尼、来那度胺单药或苯达莫司汀单药等。还可选择CAR-T治疗。年老体弱的FL患者可选择的二线治疗方案包括利妥昔单抗、苯丁酸氮芥±利妥昔单抗、环磷酰胺±利妥昔单抗。二线及后线治疗取得缓解的患者,利妥昔单抗维持治疗仍然能给患者带来生存获益。对于应用利妥昔单抗治疗后复发的患者,后续巩固治疗可以选择奥妥珠单抗。二线及后线治疗获得缓解的患者,AHSCT是后续治疗的选择之一。基于C18083/3076临床研究结果,2018年12月17日中国NMPA批准苯达莫司汀上市,适应证是利妥昔单抗或含利妥昔单抗方案治疗过程中或者治疗后病情进展的惰性B细胞NHL。基于一项Ⅱ期临床研究结果,2020年6月18日美国FDA批准EZH2抑制剂他泽司他上市,2025年3月21日中国NMPA批准他泽司他上市,用于既往至少接受过两种系统治疗且伴有EZH2突变的复发或难治FL患者的治疗。然而,2026年3月9日,因在SYMPHONY-1确证性临床试验中观察到继发性血液系统恶性肿瘤的不良事件,该药在中国启动撤市召回,全球上市许可同步撤回。基于一项Ⅱ期临床研究结果,2022年12月22日美国FDA批准CD20/CD3双特异性抗体莫妥珠单抗上市,用于既往至少接受过两种系统治疗的复发或难治成人FL患者的治疗,2024年12月23日中国NMPA批准莫妥珠单抗上市,用于治疗既往接受过至少两种系统性治疗的复发或难治FL成人患者(图3)。
此外,组蛋白去乙酰化酶抑制剂艾贝司他单药在复发或难治FL中显示出较好的疗效和可控的安全性。2025年9月16日,艾贝司他的上市申请已经被中国NMPA受理。
3. 预后因素
FL国际预后指数(follicular lymphoma international prognostic index, FLIPI)有助于评价患者预后和选择治疗方案,FLIPI包括:(1)年龄≥60岁;(2)Ann Arbor分期Ⅲ~Ⅳ期;(3)血红蛋白<120 g/L;(4)血清LDH高于正常;(5)受累淋巴结区≥5个。每项为1分,0~1分为低危组,2分为中危组,≥3分为高危组。低危、中危和高危组患者进展后5年生存率分别为85%、79%和28%。FLIPI2为利妥昔单抗时代FL的预后模型,包括:(1)年龄≥60岁;(2)淋巴结长径>6 cm;(3)骨髓侵犯;(4)β2微球蛋白高于正常;(5)血红蛋白<120 g/L。每项为1分,0分为低危组,1~2分为中危组,≥3分为高危组。低危、中危和高危患者的3年PFS率分别为91%、69%和51%,3年OS率分别为99%、96%和84%。中国医学科学院肿瘤医院2008—2018年158例Ⅱ~Ⅳ期FL患者的回顾性研究结果显示,经标准一线方案治疗缓解后进行利妥昔单抗维持治疗或观察的5年PFS率分别为83.3%和52.7%,5年OS率分别为97.8%和84.1%。生物标志物也可以用于预测接受免疫化疗方案治疗初治FL患者的生存。
(四)边缘区淋巴瘤(marginal zone lymphoma, MZL)
MZL是一组异质性疾病,包括黏膜相关淋巴组织(mucosa-associated lymphoid tissues, MALT)结外边缘区淋巴瘤(简称“MALT淋巴瘤”)、淋巴结MZL及脾边缘区淋巴瘤(splenic marginal zone lymphoma, SMZL)3类亚型,三者在形态学、免疫表型和基因表型方面相似,但其临床表现各异,其中MALT淋巴瘤最常见。在2022版WHO-HAEM5中,原先属于MALT淋巴瘤的原发皮肤边缘区淋巴瘤被单独归为一类。
1. 病因学及临床表现
(1)病因学:MZL与慢性感染或炎症所致的持续免疫刺激有关,胃MALT淋巴瘤与Hp的慢性感染有关,小肠MALT淋巴瘤与空肠弯曲菌感染有关,甲状腺MALT淋巴瘤与桥本氏甲状腺炎有关,腮腺MALT淋巴瘤与干燥综合征有关,部分非胃MALT淋巴瘤、淋巴结MZL和SMZL存在HCV感染。
(2)临床表现:胃肠道是MALT淋巴瘤最常见的原发部位,约占所有MALT淋巴瘤的50%。其他常见部位包括眼附属器、腮腺、肺部、甲状腺和皮肤等,部分患者存在骨髓受累。大部分MALT淋巴瘤为局限性疾病,约有1/3的患者表现为播散性。
2. 病理诊断
MZL的病理诊断更多的是一种排除法,形态学特征包括淋巴结和脾脏的生发中心缩小、边缘区增宽。典型的免疫表型为CD5(-)、CD10(-)、CD20(+)、CD23(-/+)、CD43(-/+)、CyclinD1(-)以及BCL2(-)。T(11;18)、t(1;14))、t(14;18)和t(3;14)是MZL中比较常见的染色体改变。伴有t(11;18)的胃MALT淋巴瘤通常表现为局部晚期病灶,对抗Hp治疗效果差。
3. 分期
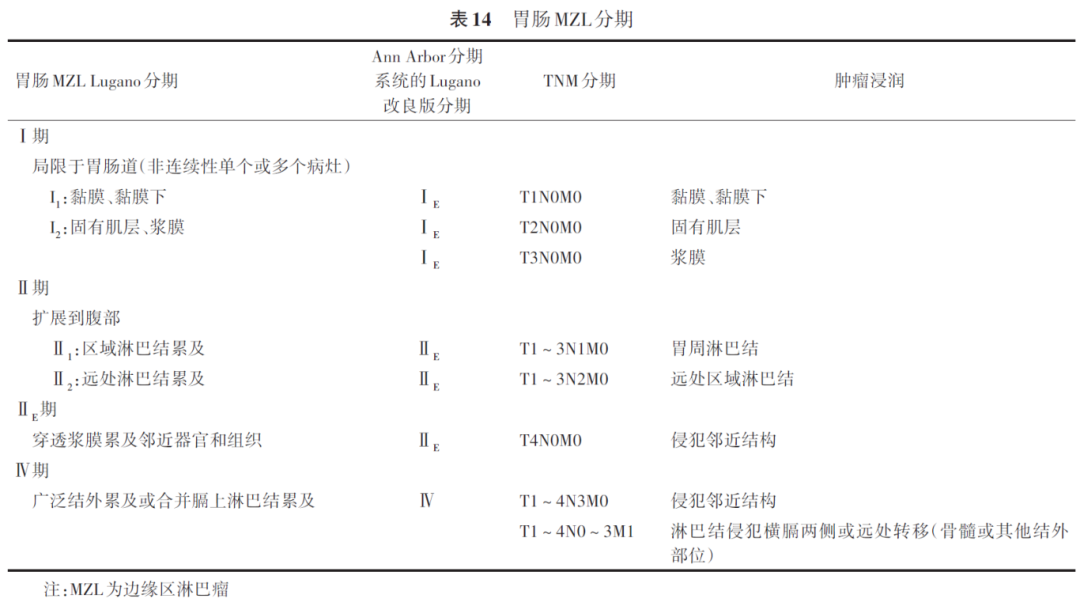
非胃或结内MZL可使用Lugano分期系统,但胃肠MZL常使用胃肠MZL Lugano分期、Ann Arbor分期系统的Lugano改良版分期或欧洲胃肠淋巴瘤研究组制定的胃肠MALT淋巴瘤的TNM分期,见表14。
4. 治疗
MZL需要按照原发部位进行分层治疗。
(1)MALT淋巴瘤
①原发胃MALT淋巴瘤
胃肠MZL Lugano分期Ⅰ~Ⅱ1期的原发胃MALT淋巴瘤Hp阳性患者首选抗Hp治疗,对于抗Hp治疗后失败的患者可选择ISRT治疗;疗前Hp阴性的Ⅰ~Ⅱ1期患者推荐ISRT治疗。ⅡE、Ⅱ2和Ⅳ期患者无治疗指征、无症状的患者可以观察等待;有治疗指征的患者可考虑利妥昔单抗联合化疗(1类推荐)。
(a)胃肠MZL Lugano分期Ⅰ~Ⅱ1期的原发胃MALT淋巴瘤患者:Hp感染在胃MALT淋巴瘤患者的发生、发展过程中发挥着重要作用,因此在治疗前必须进行Hp相关检测,判断Hp感染情况,决定是否进行抗Hp治疗。Hp阳性的Ⅰ~Ⅱ1期患者均应首先进行抗Hp治疗。治疗前Hp阳性、t(11;18)阳性的患者,推荐行抗Hp感染治疗+ISRT,如ISRT有禁忌,也可以联合利妥昔单抗治疗。Hp阳性、t(11;18)状态不明或阴性的患者,推荐首先接受抗Hp治疗。治疗前Hp阴性的患者首先推荐ISRT,如存在ISRT禁忌证,可以选择利妥昔单抗治疗。初治患者在治疗3个月后需要复查胃镜和活检以评价疗效。如果肿瘤无残存并且Hp为阴性,则定期复查;如果肿瘤残存而Hp阴性,无症状的患者可以观察3个月后复查或接受ISRT,有症状的患者应该接受ISRT;对于肿瘤无残存而Hp阳性的患者,应该接受二线抗Hp治疗;如果患者肿瘤残存并且Hp阳性,疾病无进展可以考虑二线抗Hp治疗,疾病较疗前进展,应该考虑二线抗Hp治疗+ISRT。
抗Hp治疗后局部复发的患者推荐行ISRT。抗Hp治疗序贯ISRT后复发的患者需要评价患者是否具有治疗指征,无症状、无治疗指征的患者可以观察,有治疗指征的患者可以接受利妥昔单抗单药或联合化疗。
(b)胃肠MZL Lugano分期Ⅱ2、ⅡE和Ⅳ期的原发胃MALT淋巴瘤患者:无治疗指征、无症状的患者可以观察等待。治疗指征包括影响器官功能、出现淋巴瘤相关症状(如胃肠道出血、腹胀等)、大肿块、疾病持续进展或有合适的临床试验。治疗方案包括利妥昔单抗联合化疗(BR方案、R-CHOP方案、R-CVP方案、R2方案)或姑息性ISRT。针对特定情况,如危及生命的胃肠道出血,可以采取手术治疗。年老体弱患者,可以选择利妥昔单抗单药、苯丁酸氮芥±利妥昔单抗、环磷酰胺±利妥昔单抗方案治疗(图4)。
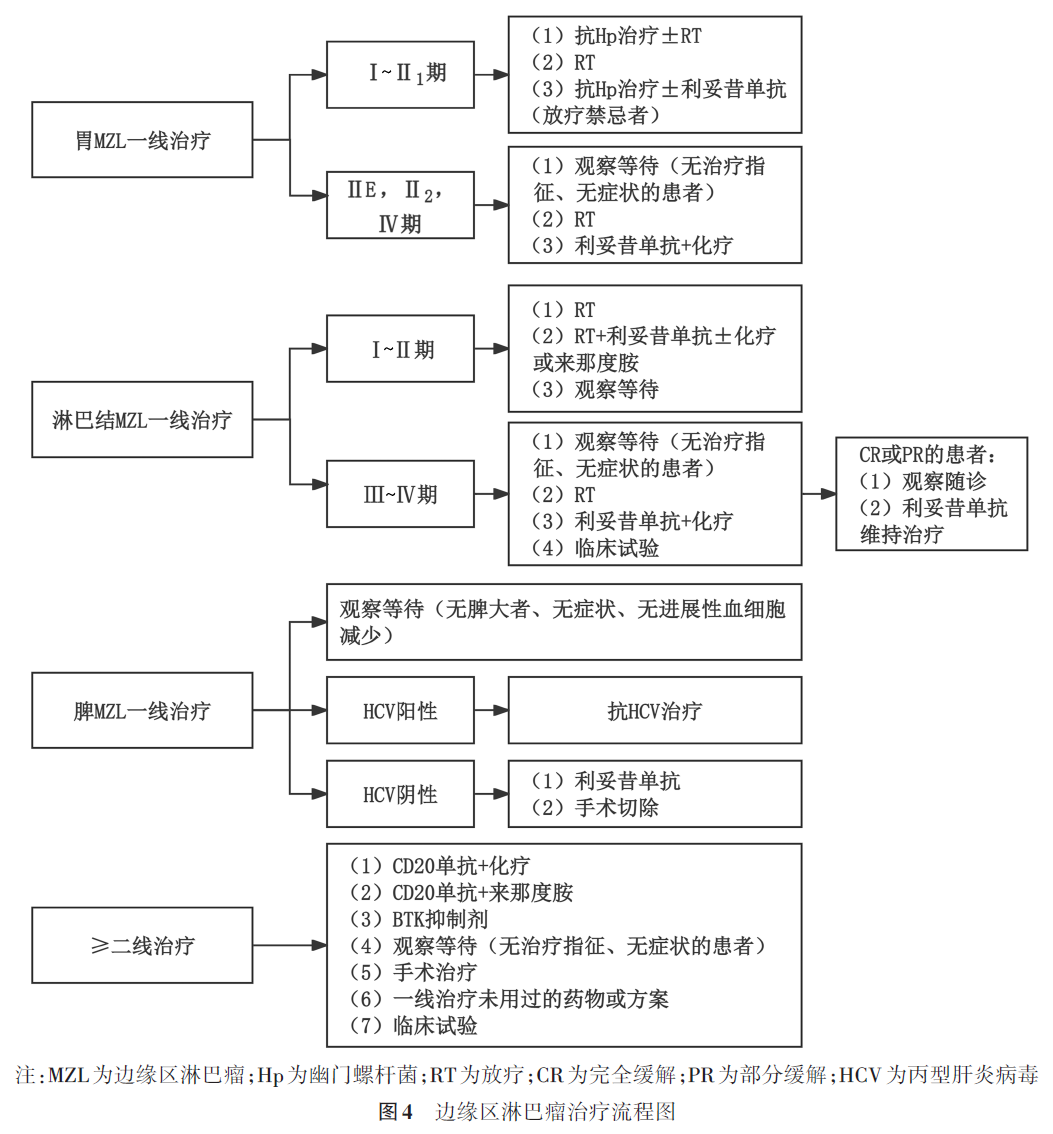
②非胃原发MALT淋巴瘤
Ⅰ期或局限Ⅱ期的非胃MALT淋巴瘤患者,ISRT具有良好疗效;利妥昔单抗可以作为治疗选择;对于某些特定部位的MALT淋巴瘤(如肺、甲状腺、结肠、小肠、乳腺等),可以选择手术切除,切缘阳性的患者术后应该接受局部区域ISRT,切缘阴性的患者可以选择随诊观察。Ⅳ期非胃MALT淋巴瘤患者可以选择ISRT,也可以按照晚期淋巴结MZL治疗。局部复发的患者可以选择ISRT或按照晚期淋巴结MZL治疗;病变范围广泛的复发患者如果无治疗指征可以观察,有治疗指征的患者可以参考淋巴结MZL的二线及后线治疗。
(2)淋巴结MZL
①Ⅰ~Ⅱ期淋巴结MZL患者的一线治疗:Ⅰ期和局限Ⅱ期患者推荐ISRT,也可以考虑ISRT+利妥昔单抗±化疗或来那度胺,Ⅰ期伴有腹腔内或腹膜大肿块者可以考虑利妥昔单抗±化疗或来那度胺;广泛Ⅱ期患者推荐利妥昔单抗±化疗或来那度胺±ISRT,或者可以选择观察等待。
②Ⅲ~Ⅳ期淋巴结MZL患者的一线治疗:无治疗指征的Ⅲ~Ⅳ期患者推荐观察等待;具有治疗指征的患者推荐利妥昔单抗联合其他药物,包括BR方案、R-CHOP方案、R-CVP方案、R2方案等,也可以参加合适的临床试验或进行姑息性ISRT。治疗指征包括出现淋巴瘤相关症状、影响器官功能、继发于淋巴瘤的血细胞减少、大肿块、疾病持续进展或有合适的临床试验。
③一线治疗后的巩固治疗:一线治疗后达到CR或PR的患者可以选择随诊观察或利妥昔单抗维持治疗。
④二线及后线治疗:一线治疗后复发或进展的患者,如果无治疗指征,常常能够再次从观察等待中获益。进展及复发或难治患者的治疗指征和一线治疗指征类似。进展及复发患者需要再次进行肿瘤组织活检,以明确是否出现病理类型转化,尤其是对于出现LDH升高、局部淋巴结持续增大、结外受累和新症状的患者。2023年4月17日中国NMPA批准奥布替尼用于治疗既往接受过一种治疗的成人MZL患者。MZL二线及后线治疗方案参考FL(图4)。
(3)SMZL
①无脾大的SMZL患者的一线治疗:无脾大、无症状或无进展性血细胞减少的SMZL患者可以随诊观察。
②脾大伴HCV阳性的SMZL患者的一线治疗:脾大伴HCV阳性的SMZL患者应评价肝功能,如无禁忌证,应行抗HCV治疗。对于HCV阳性的SMZL患者,合适的抗病毒治疗显示出良好疗效;抗病毒治疗无效或者有禁忌证的HCV阳性SMZL患者应该按照HCV阴性SMZL患者的治疗原则进行治疗。
③脾大伴HCV阴性的SMZL患者的一线治疗:脾大伴HCV阴性的SMZL患者如无症状,可随诊观察。有症状的SMZL患者可以采取利妥昔单抗单药治疗,后续可选择维持或不维持治疗。利妥昔单抗治疗无效的患者可行脾切除。
④复发SMZL患者:复发SMZL患者如果无治疗指征可选择随诊观察。如果有治疗指征可行脾切除、姑息性ISRT、含利妥昔单抗的联合治疗方案或参考淋巴结MZL的二线及后线治疗(图4)。
(五)慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(chronic lymphocytic leukemia/small lymphocytic lymphoma, CLL/SLL)
CLL/SLL在美国占NHL的18.6%,是美国发病率排名第2位的NHL类型。中国CLL/SLL的发病率较低,占NHL的4.1% 。
1. 诊断和分期
CLL和SLL是同一种疾病的不同表现,均属于惰性B细胞淋巴瘤。CLL以骨髓和外周血受累为主要特征,SLL以淋巴结病变为主要特征。
(1)诊断:CLL的诊断标准主要包括:①外周血单克隆B淋巴细胞(CD19+细胞)计数≥5×109/L,且持续至少3个月;②外周血涂片形态学表现为小的、成熟的淋巴细胞显著增多;外周血淋巴细胞中不典型的淋巴细胞及幼稚淋巴细胞≤55%;③典型流式细胞免疫表型为CD19(+)、CD5(+)、CD23(+)、CD200(+)、CD10(-)、FMC7(-)、CD43(+),sIg、CD20及CD79b弱表达。SLL的确诊必须依赖组织病理学和IHC,临床特征包括:①淋巴结和/或肝脾肿大;②无血细胞减少;③外周血单克隆B淋巴细胞计数<5×109/L。推荐进行FISH检测:+12、del(11q)、del(13q)和del(17p)。推荐检测TP53、IGHV基因突变状态和CpG寡核苷酸刺激核型。这些检测有助于预后判断和治疗决策。
(2)分期:由于CLL患者普遍存在骨髓和外周血受累,多采用Binet分期或Rai分期(表15),SLL采取Lugano分期(表3)。

2. 治疗
Lugano分期为Ⅰ期的SLL患者可以选择20~30 Gy放疗。Rai分期为0~Ⅱ期的CLL或Lugano分期为Ⅱ~Ⅳ期的SLL患者,如果无治疗指征可以观察等待;有治疗指征时按照FISH检测del(17p)、TP53突变、CpG寡核苷酸刺激核型及IGHV基因突变检测结果、患者一般状态和合并症情况,选择相应的治疗方案。Rai分期为Ⅲ~Ⅳ期的CLL患者如果有进行性血细胞减少,根据FISH检测del(17p)、TP53突变、CpG寡核苷酸刺激核型及IGHV基因突变检测结果、患者一般状态和合并症情况,选择相应的治疗方案。
(1)治疗指征
有合适的临床试验;出现明显的疾病相关症状,如严重乏力、盗汗、无明确原因体重下降(6个月内下降≥10%)和非感染性发热;脏器功能受损;持续增大的大肿块,如脾大超过左肋缘下6 cm、淋巴结长径>10 cm;进行性贫血或进行性血小板下降;类固醇难治的自身免疫性血细胞减少。
(2)一线治疗
BTK抑制剂为CLL/SLL治疗的首选药物之一,使用前需进行心血管系统功能评价(1类推荐)。
①无del(17p)/TP53突变的CLL/SLL患者:一线治疗可选择泽布替尼、伊布替尼、奥布替尼、伊布替尼+CD20单抗、苯达莫司汀+CD20单抗、高剂量甲强龙+CD20单抗、伊布替尼+维奈克拉、维奈克拉+奥妥珠单抗、奥妥珠单抗、阿可替尼±奥妥珠单抗、苯丁酸氮芥+奥妥珠单抗等。
②具有del(17p)或TP53突变的CLL/SLL患者:一线治疗可选择泽布替尼、高剂量甲强龙+CD20单抗、伊布替尼、奥布替尼、阿可替尼±奥妥珠单抗、维奈克拉+奥妥珠单抗、伊布替尼+维奈克拉等。
基于RESONATE-2研究结果,伊布替尼于2016年3月4日被美国FDA批准用于CLL患者的一线治疗。基于CLL14研究结果和ELEVATE-TN研究结果,美国FDA分别于2019年5月15日和2019年11月21日批准维奈克拉+奥妥珠单抗方案和阿可替尼单药用于一线治疗CLL/SLL成人患者。2023年3月22日中国NMPA批准阿可替尼上市,用于治疗至少接受过1种治疗的CLL/SLL成人患者,2025年3月18日中国NMPA批准阿可替尼一线治疗既往未接受过治疗的CLL/SLL。基于ALPINE和SEQUOIA研究,2023年1月20日美国FDA批准泽布替尼用于治疗CLL/SLL成人患者。
(3)BTK抑制剂和维奈克拉为基础的方案治疗后复发或难治CLL/SLL患者的治疗
复发或难治CLL/SLL患者推荐的治疗方案包括:BTK抑制剂、维奈克拉±利妥昔单抗、伊布替尼+维奈克拉、苯达莫司汀+利妥昔单抗、来那度胺±利妥昔单抗、高剂量甲强龙+CD20单抗、奥妥珠单抗等。非共价结合BTK抑制剂匹妥布替尼用于既往共价结合BTK抑制剂治疗后耐药或不耐受的患者(图5)。
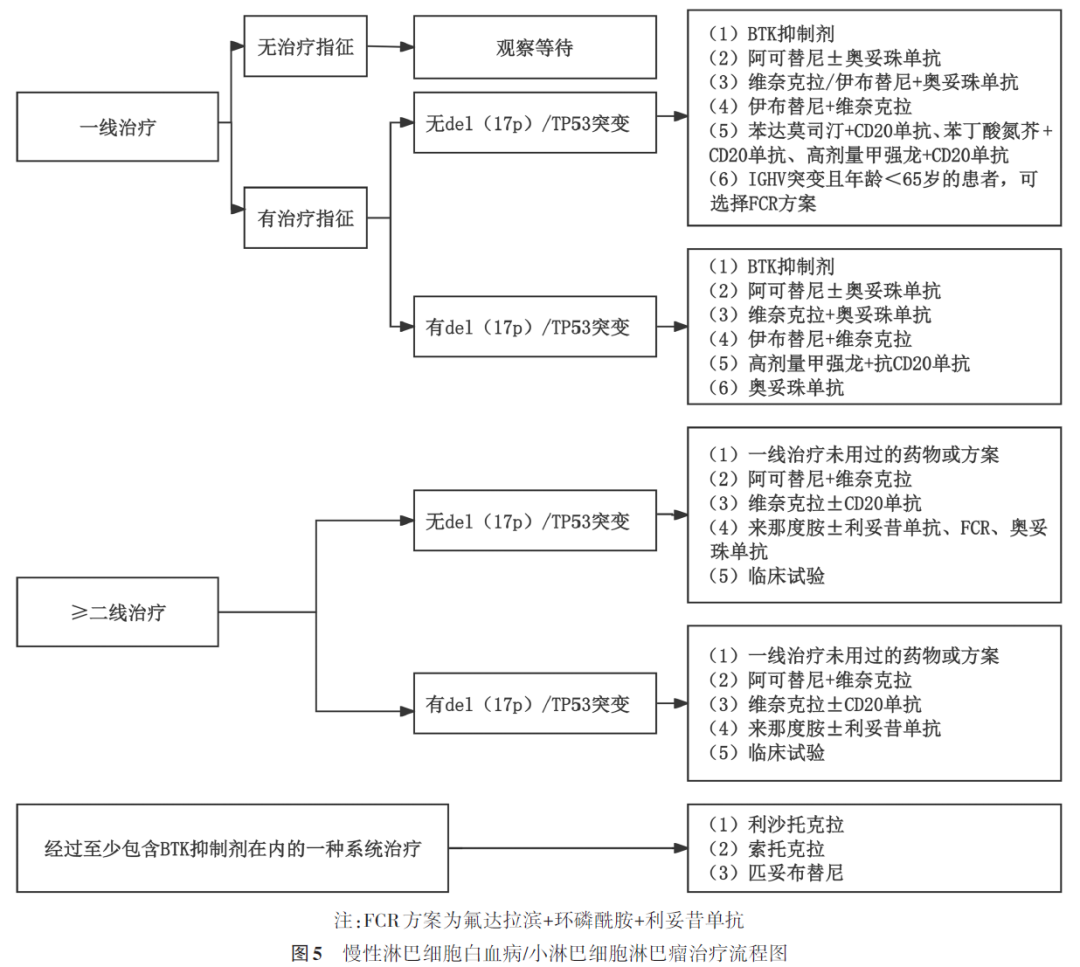
伊布替尼于2014年2月12日被美国FDA批准用于治疗既往接受过至少1次治疗的CLL,于2017年8月30日被中国NMPA批准上市,用于既往至少接受过1种治疗的CLL/SLL。基于一项Ⅱ期临床研究结果,泽布替尼于2020年6月3日被中国NMPA批准用于既往至少接受过1种方案治疗的CLL/SLL患者。奥布替尼于2020年12月25日被中国NMPA批准上市,用于既往至少接受过1种方案治疗的成人CLL/SLL患者。2018年6月8日美国FDA批准维奈克拉与利妥昔单抗联合用于既往至少接受过1种方案治疗、伴或不伴del(17p)的CLL/SLL患者的治疗。2023年12月1日美国FDA批准匹妥布替尼用于治疗经过至少2种治疗方案(包括1种BTK抑制剂和1种BCL-2抑制剂)的CLL/SLL成人患者。2026年2月11日,中国NMPA批准匹妥布替尼用于治疗既往经过至少包含BTK抑制剂在内的1种系统治疗的成人CLL/SLL患者。2025年7月8日中国NMPA批准新一代BCL-2抑制剂利沙托克拉用于既往经过至少包含BTK抑制剂在内的一种系统治疗的成人CLL/SLL患者。2026年1月6日中国NMPA批准新一代BCL-2抑制剂索托克拉治疗既往接受过至少包含BTK抑制剂在内的一种系统治疗的CLL/SLL成人患者。
3. 预后
CLL/SLL患者中位生存时间约10年,但患者预后具有异质性。临床、实验室指标以及分子生物学标志物可以作为预后因素,常用慢性淋巴细胞白血病国际预后指数(chronic lymphocytic leukemia international prognostic index, CLL-IPI)评价预后(表16):0~1分为低危,2~3分为中危,4~6分为高危,7~10分为极高危。CLL-IPI低危、中危、高危、极高危患者的5年OS率分别为93.2%、79.3%、63.3%和23.3%。对于中国CLL/SLL患者,CLL-IPI低危、中危、高危、极高危患者的5年OS率分别为97.6%、83.7%、67.8%和55.2%。微小残留病灶与CLL/SLL患者的治疗反应和预后密切相关,有望成为疗效监测和指导治疗的重要生物学指标。

(六)MCL
MCL在美国占成人NHL的4.1%,在中国占所有NHL的2.7%,是一类兼具惰性和侵袭性淋巴瘤特征的NHL 。
1. 病理特征
MCL需要结合组织学形态和分子表型进行诊断,其典型的免疫表型为CD5(+)、CD19(+)、CD20(+),CD23(-)或弱(+)、Cyclin D1(+)、CD43(+),强表达sIgM或IgD,但通常CD10(-)、CD11c(-)、BCL-6(-)。病理特征是t(11;14)(q13;q32)和CyclinD1过度表达。分子遗传学改变包括CCND1、SOX11等基因突变。在接受传统治疗的MCL患者中,TP53基因突变与更差的预后相关,进行TP53基因检测有助于判断患者预后。WHO-HAEM5将MCL分为经典型MCL、白血病样非淋巴结性MCL和原位套细胞瘤变3种亚型。
2. 治疗
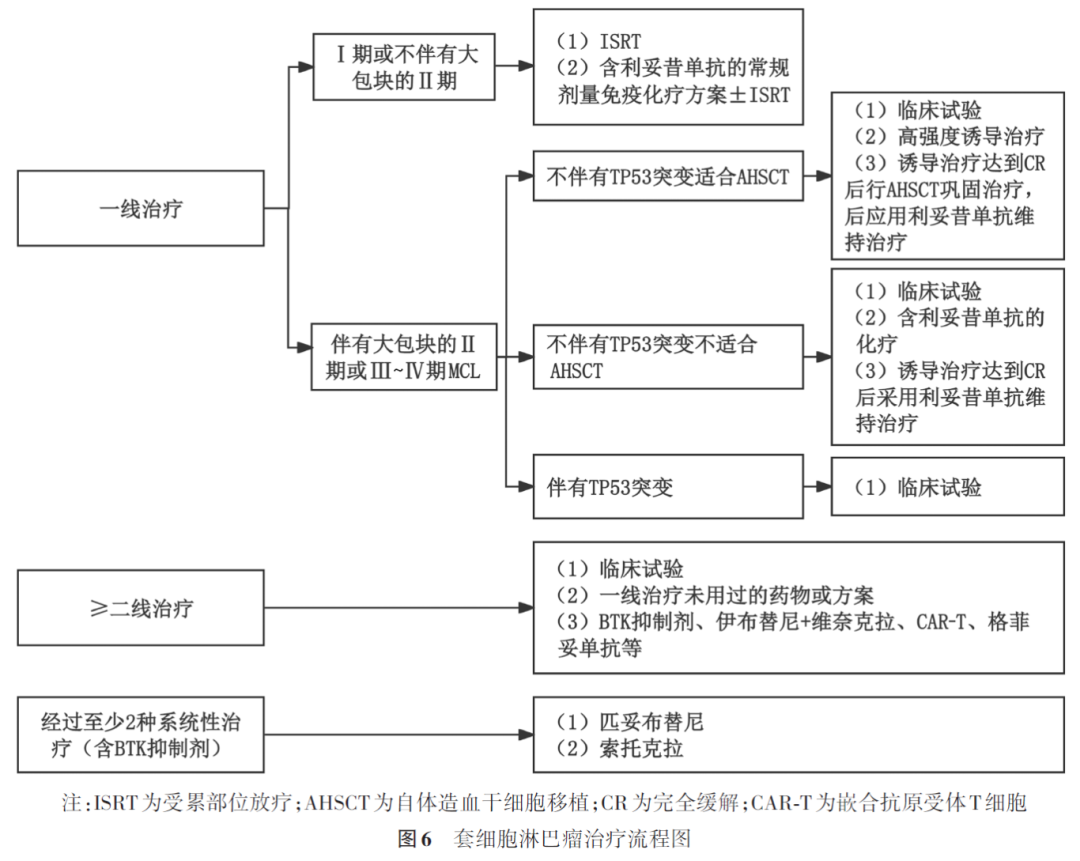
Ⅰ期和不伴有大肿块的局限Ⅱ期MCL患者,推荐采用ISRT,或含利妥昔单抗的常规剂量免疫化疗方案±ISRT。伴有大肿块的Ⅱ期或Ⅲ~Ⅳ期MCL患者需根据病理及临床特征、是否有TP53突变,采取不同的治疗策略(2A类推荐)。
(1)MCL患者的一线治疗
①Ⅰ期或不伴有大肿块的Ⅱ期MCL患者:Ⅰ期和不伴有大肿块的局限Ⅱ期MCL患者,推荐采用ISRT,或含利妥昔单抗的常规剂量免疫化疗方案±ISRT。不伴有大肿块的非局限Ⅱ期MCL患者,推荐含利妥昔单抗的常规剂量免疫化疗方案。含利妥昔单抗的常规剂量免疫化疗方案包括R-CHOP、利妥昔单抗+苯达莫司汀、R2、VR-CAP(硼替佐米+利妥昔单抗+环磷酰胺+阿霉素+泼尼松)等。
②伴有大肿块的Ⅱ期或Ⅲ~Ⅳ期MCL患者:需根据病理及临床特征、是否有TP53突变,采取不同的治疗策略。
不伴有TP53突变的经典型MCL患者需判断是否适合AHSCT。(a)不适合AHSCT的患者:首先推荐参加合适的临床试验,或选择利妥昔单抗+苯达莫司汀方案、利妥昔单抗+苯达莫司汀+伊布替尼方案、利妥昔单抗+苯达莫司汀+阿可替尼方案、R-CHOP方案、VR-CAP方案、R2方案、RBAC500方案(利妥昔单抗+苯达莫司汀+阿糖胞苷)。对于上述治疗有效的患者采用利妥昔单抗或利妥昔单抗+BTK抑制剂维持治疗。(b)适合AHSCT的患者:推荐参加合适的临床试验或采用高强度诱导治疗方案。高强度诱导治疗方案包括R-DHA+铂类(卡铂、顺铂或奥沙利铂)方案、R-CHOP与R-DHAP交替方案+BTK抑制剂方案后利妥昔单抗+BTK抑制剂维持治疗、NORDIC方案(高剂量R-CHOP与利妥昔单抗+高剂量阿糖胞苷交替)、R-HyperCVAD方案、利妥昔单抗+苯达莫司汀序贯利妥昔单抗+高剂量阿糖胞苷、利妥昔单抗+苯达莫司汀方案等。诱导治疗达到CR后行AHSCT巩固治疗,之后应用利妥昔单抗维持治疗3年。
伴TP53突变的经典型MCL患者对传统细胞毒药物联合治疗方案疗效欠佳,强烈推荐参加临床试验,如果没有合适的临床试验,可以考虑泽布替尼+奥妥珠单抗+维奈克拉治疗。
无症状或无治疗指征的惰性MCL患者可以随诊观察。需要治疗的患者,参考经典型MCL患者的治疗策略。
(2)复发或难治MCL患者的治疗
可选择BTK抑制剂、来那度胺±利妥昔单抗、BR方案、硼替佐米±利妥昔单抗、R-DHA+铂类(卡铂、顺铂或奥沙利铂)方案、R-GemOx方案、伊布替尼+来那度胺+利妥昔单抗、伊布替尼+维奈克拉、CAR-T治疗等。基于一项Ⅱ期临床研究结果,美国FDA于2013年11月13日批准伊布替尼用于一线治疗失败的MCL患者的治疗。2017年8月30日,中国NMPA批准伊布替尼上市,用于既往至少接受过1种方案治疗的MCL患者的治疗。2023年4月6日,在验证性临床试验中,伊布替尼未显示出OS优势,美国FDA认为不足以支持伊布替尼在MCL中的全面批准,制造商在与美国FDA协商后自愿撤市。美国FDA和中国NMPA分别于2019年11月15日和2020年6月3日批准泽布替尼上市,用于既往接受过至少1种方案治疗的成人MCL患者的治疗。2020年12月25日,奥布替尼被中国NMPA批准上市,适应证为既往至少接受过1种方案治疗的MCL患者的治疗。二线治疗后可采用allo-HSCT巩固治疗。2020年7月24日,美国FDA批准CD19 CAR-T产品tecartus(brexucabtagene autoleucel)用于治疗复发或难治MCL。2023年3月22日,中国NMPA批准阿可替尼上市,用于治疗既往至少接受过1种治疗的成人MCL患者。对于免疫化疗及共价BTK抑制剂治疗后复发或难治MCL患者,可以考虑非共价BTK抑制剂匹妥布替尼或者格菲妥单抗治疗。2023年1月27日美国FDA批准匹妥布替尼上市,适用于治疗经过至少2种系统性治疗(含BTK抑制剂)的复发或难治MCL成人患者。2024年10月22日中国NMPA批准匹妥布替尼上市,单药适用于既往接受过至少2种系统性治疗(含BTK抑制剂)的复发或难治MCL成人患者。2026年1月6日中国NMPA批准新一代BCL-2抑制剂索托克拉治疗既往接受过至少两种系统性治疗(含BTK抑制剂)的复发或难治MCL成人患者(图6)。
3. 预后因素
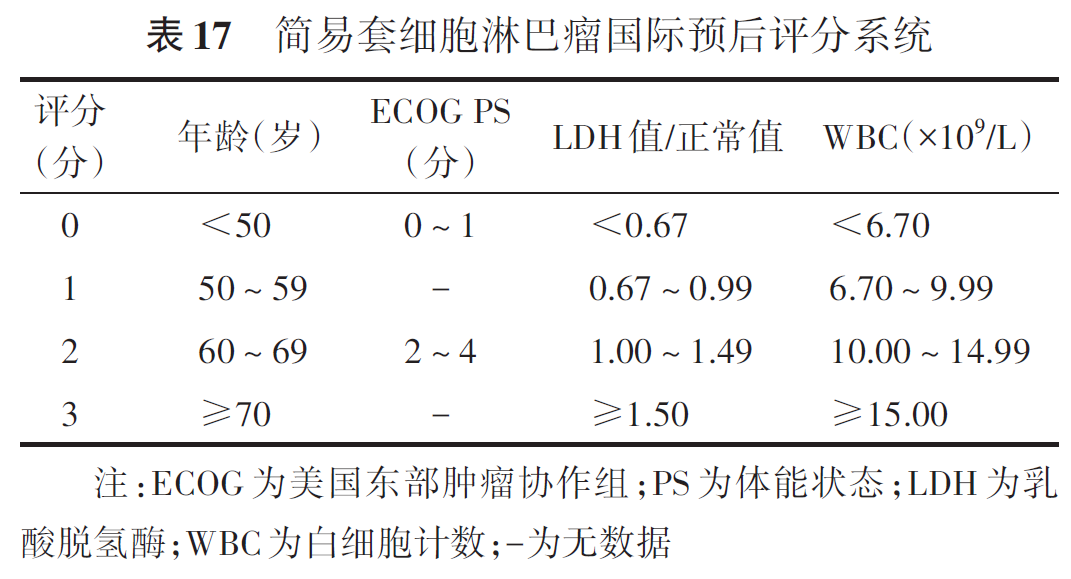
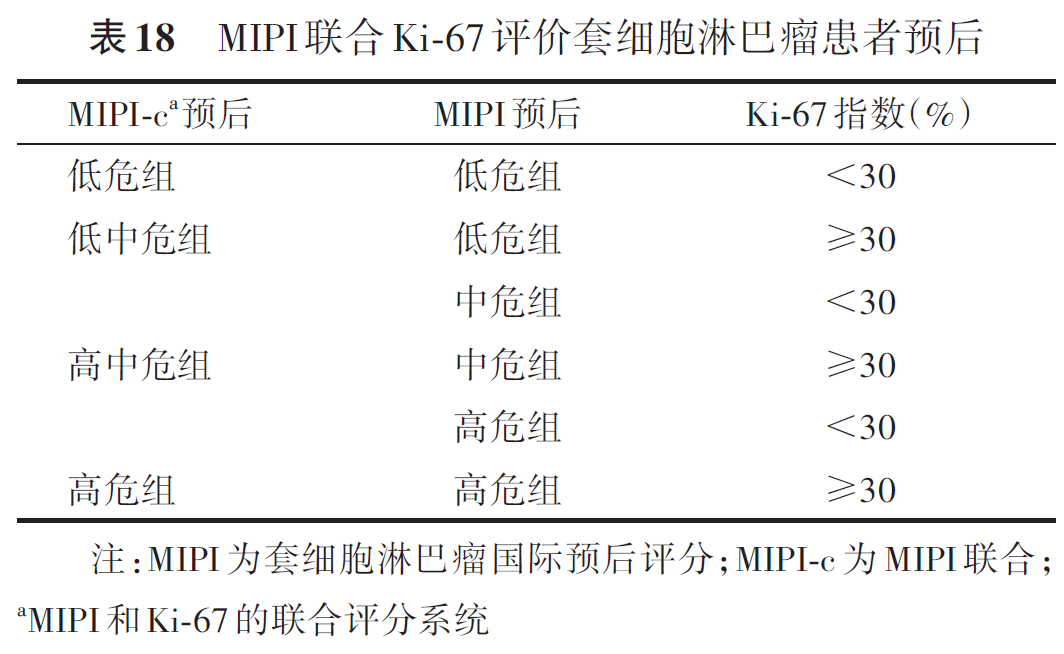
MCL不良预后因素包括TP53突变或缺失、Ki-67>30%、母细胞样和多形性细胞样转化等。相比IPI,简易套细胞淋巴瘤国际预后评分系统(mantle cell lymphoma international prognostic index,MIPI)对MCL的预后分层效果更好,被广泛应用(表17)。结合MIPI和Ki-67的联合评分系统被认为能够更好地预测MCL患者的预后,其中0~3分为低危组,4~5分为中危组,6~11分为高危组(表18)。
(七)伯基特淋巴瘤(Burkitt lymphoma, BL)
BL占所有中国NHL的1.1%,占欧洲和美国所有成人淋巴瘤的1%~2%。BL是高度侵袭性NHL,约占儿童NHL的40%,可分为地方流行型、散发型和免疫缺陷相关型3个变异型。散发型BL主要见于发达国家,占成人NHL的1%~5%,占儿童淋巴瘤的30%,主要发生在儿童和青年,男女比例为3∶1~2∶1,EBV阳性率<30%;地区型BL主要见于赤道附近的非洲国家,约占该地区儿童肿瘤的30%~50%,与EBV及地方性疟疾感染高度相关,EBV阳性率>95%;免疫缺陷相关型BL主要见于HIV感染人群或器官移植的患者。
1. 临床特点
地方型BL最常出现下颌骨病灶,可以累及远端回肠、肾、乳腺和长骨等结外组织和器官。散发型成人BL以腹腔大肿块,特别是回盲部肿块为常见临床表现,面部特别是下颌骨受累罕见。BL是细胞倍增周期最短的肿瘤,生长迅速。BL结外受累常见,头颈、腹部、骨髓和CNS等是其常见的受累部位。
2. 病理诊断
经典型BL形态学表现为较均一的中等大小肿瘤性B细胞弥漫增生,核分裂象及凋亡很明显,常见星空现象。肿瘤细胞起源于生发中心,免疫表型常表现为sIgM(+)、单一轻链(+)、CD19(+)、CD20(+)、CD22(+)、c-Myc(+)、CD10(+)、BCL-6(+)、BCL-2(-)、CD5(-)、CD23(-)、MUM-1(-)和TdT(-)。增殖指数非常高,Ki-67阳性率近100%。即使形态学、免疫表型都为典型的BL,也要采用FISH进行MYC检测,其中t(8;14)约占80%,t(2;8)和t(8;22)占15%;鉴别诊断包括伴MYC和BCL-2重排的高级别B细胞淋巴瘤和BL伴11q异常。EBV-EBER检测对BL是必须的,约100%的地区型BL、30%的散发型BL及40%的免疫缺陷型BL存在EBV感染。
2016年WHO造血与淋巴系统肿瘤分类新提出“伴11q异常BL”,其基因表达谱和临床特点与经典BL类似,但无MYC基因异常,而是具有11q染色体改变。2022年WHO-HAEM5将“伴11q异常BL”更名为“高级别B细胞淋巴瘤伴11q异常”,并建议对EBV阳性BL和EBV阴性BL这两种亚型进行区分,与EBV阴性BL相比,EBV阳性BL的体细胞超突变水平更高。
3. 治疗
BL患者的一线治疗以化疗为主(1类推荐)。
(1)BL患者的一线治疗:BL患者的一线治疗以化疗为主,一般不推荐放疗,即使是局限性患者也应采取全身治疗的策略,诊断后应尽早开始治疗,采用短疗程高强度的多药联合化疗方案。联合利妥昔单抗可以改善患者长期生存,特别是>60岁的患者获益更大。应进行CNS预防性治疗,并充分预防肿瘤溶解综合征的发生。LDH正常、Ⅰ期且腹腔肿块完全切除或单个腹腔外肿块长径<10 cm的患者为低危患者,此外均为高危患者。无论低危或高危患者,均可参加合适的临床试验。<60岁的低危患者可选择的诱导治疗方案包括CODOX-M-R方案(环磷酰胺+长春新碱+阿霉素+高剂量甲氨蝶呤+利妥昔单抗),或DA-EPOCH-R方案,或R-HyperCVAD/MA方案;<60岁的高危患者,可选择CODOX-M-R与R-IVAC(利妥昔单抗+依托泊苷+异环磷酰胺+阿糖胞苷)交替方案或R-HyperCVAD/MA方案,不能耐受强化疗方案的患者可选择DA-EPOCH-R方案,治疗起始合并症状性CNS受累的患者治疗方案中应包含能透过血脑屏障的药物。≥60岁的低危和高危患者推荐DA-EPOCH-R方案治疗。
(2)复发或难治BL患者的治疗:若BL患者一线治疗后6个月以上疾病复发,则推荐参加合适的临床试验,或接受二线方案治疗,或进行最佳支持治疗。二线化疗可采用DA-EPOCH方案、R-ICE方案、R-GDP方案、R-IVAC方案、高剂量阿糖胞苷+利妥昔单抗等方案。二线治疗后若患者达CR,可考虑AHSCT±ISRT,或考虑allo-HSCT±ISRT;若患者达PR,则继续进行二线方案治疗、AHSCT±ISRT或allo-HSCT±ISRT;若患者为SD或PD,则推荐参加合适的临床试验或包括姑息性ISRT在内的最佳支持治疗。若患者一线治疗后6个月内复发,则考虑参加合适的临床试验或最佳支持治疗。BL患者可能从CAR-T治疗、免疫检查点抑制剂、双特异性抗体和抗体偶联药物治疗中获益。
4. 预后因素
成人BL患者总体预后差于儿童和青少年BL患者,90%以上的儿童及青少年BL患者在高剂量化疗下可以得到治愈,75%~85%的成人BL患者可以得到长期缓解。成人BL-IPI包括了4个独立不良预后因素:(1)年龄≥40岁;(2)ECOG PS评分≥2分;(3)LDH水平>3倍正常上限值;(4)CNS受累。该评分系统将成人BL患者分为低风险组(0个危险因素)、中风险组(1个危险因素)和高风险组(≥2个危险因素),不同风险组患者的3年PFS率分别为92%、72%和53%,3年OS率分别为96%、76%和59%。
(八)外周T细胞淋巴瘤,非特指型(peripheral T-cell lymphoma,not otherwise specified, PTCL-NOS)
PTCL是起源于胸腺后成熟T细胞和NK细胞的一组异质性肿瘤。WHO-HAEM4中提出PTCL包括白血病型或播散型、淋巴结型、结外型和皮肤型。美国PTCL-NOS占NHL的1.7%,我国占NHL的4.3%。在欧美人群中,PTCL亚型发病率由高到低依次为PTCL-NOS、血管免疫母细胞性T细胞淋巴瘤(angioimmunoblastic T-cell lymphoma, AITL)、结外NK/T细胞淋巴瘤,鼻型(extranodal NK/T-cell lymphoma, nasal type, ENKTL)、成人T细胞白血病/淋巴瘤、间变性淋巴瘤激酶(anaplastic lymphoma kinase, ALK)阳性ALCL和ALK阴性ALCL,占T细胞淋巴瘤比例分别为25.9%、18.5%、10.4%、9.6%、6.6%和5.5%,其他类型PTCL相对少见。在中国,ENKTL是最常见的PTCL亚型,其次为PTCL-NOS、AITL、ALK阳性及阴性ALCL,占T细胞淋巴瘤比例分别为28.16%、19.88%、13.84%、7.34%和4.21%。与WHO-HAEM4相比,WHO-HAEM5加入了T细胞为主的肿瘤样病变概念,包括菊池病(Kikuchi-Fujimoto病)、惰性 T 淋巴细胞增殖和自身免疫性淋巴增生综合征。
1. 临床表现
PTCL-NOS常见于中老年,中国医学科学院肿瘤医院2006—2017年240例PTCL(不包括ENKTL)患者的回顾性分析结果显示,中位发病年龄为51岁(12~84岁),无明显性别差异,PTCL-NOS约占PTCL患者的42.5%。PTCL-NOS多表现为浅表淋巴结肿大,半数患者伴有B症状。结外常累及皮肤及皮下组织、肝脾、消化道、甲状腺和骨髓等。初诊时多为Ⅲ~Ⅳ期。
2. 病理诊断
PTCL-NOS由于其在形态学、免疫学、遗传学和临床表现上均无特异性,所以只有在排除其他独立分型的T细胞淋巴瘤后,方能做出PTCL-NOS的诊断。组织病理学表现为异型的淋巴细胞分布于副皮质区或弥漫分布。肿瘤细胞通常会丢失一种或多种成熟T细胞抗原(CD5或CD7),表达TCR(多为α或β型),一般不表达B细胞相关抗原。PTCL-NOS的TCR基因常表现为克隆性重排。PTCL-NOS包括2种亚型,分别为PTCL-GATA3和PTCL-TBX21,PTCL-GATA3具有统一的分子遗传谱,具有2型辅助性T细胞的转录特征,而PTCL-TBX21是异质性的,可能伴随细胞毒(GNLY,PRF,GZM-K,-H-M,LYZ)/细胞因子(CXCR3, CXCL12,和CCL-2,-3,-6,-11)基因的表达和侵袭性行为,具有1型辅助性T细胞的转录特征。进行IHC检测CD10、PD-1、BCL-6、CXCL13、ICOS鉴别滤泡辅助T细胞来源的淋巴瘤,有条件的可以进行RHOA、TET2、DNMT3A、IDH2基因突变检测。当DLBCL的细胞多形性明显时酷似T细胞特点,也需要进行鉴别,所以B细胞标志物(如CD20和PAX5等)的检查不可或缺。在伴有多量浆细胞增生时,注意浆细胞的克隆性。
3. 治疗
PTCL-NOS推荐参加合适的临床试验。若无合适的临床试验,对IPI低危或低中危的Ⅰ~Ⅱ期患者给予4~6个周期化疗±局部放疗±AHSCT。对于IPI高危或中高危的Ⅰ~Ⅳ期患者,给予6~8个周期化疗±局部放疗±AHSCT。对于复发或难治PTCL-NOS患者,推荐参加合适的临床试验,或应用二线方案治疗,或行姑息性放疗(2A类推荐)。
(1)PTCL-NOS患者的一线治疗:一线推荐方案包括CHOEP方案(环磷酰胺+长春新碱+多柔比星+依托泊苷+泼尼松)、CHOP方案、DA-EPOCH方案、维布妥昔单抗+CHP方案(适用于CD30阳性的患者);其他推荐方案包括CHOP方案序贯IVE方案(异环磷酰胺+依托泊苷+表柔比星)、HyperCVAD方案以及含吉西他滨的方案。一线治疗达到CR的患者可随诊观察或进行AHSCT。AHSCT能否改善患者生存尚缺乏前瞻性临床研究证实。但基于单臂的前瞻性或回顾性临床研究结果,推荐患者进行AHSCT,尤其是IPI评分比较高的患者。部分PTCL(如肝脾T细胞淋巴瘤、单形性嗜上皮性肠道T细胞淋巴瘤)预后极差,可以选择一线allo-HSCT进行巩固治疗,但缺乏大样本量研究数据支持。对于局限期诱导化疗达CR的患者,可以考虑进行巩固放疗。一线化疗未达CR的患者,参照复发或难治PTCL-NOS患者的治疗原则(图7)。
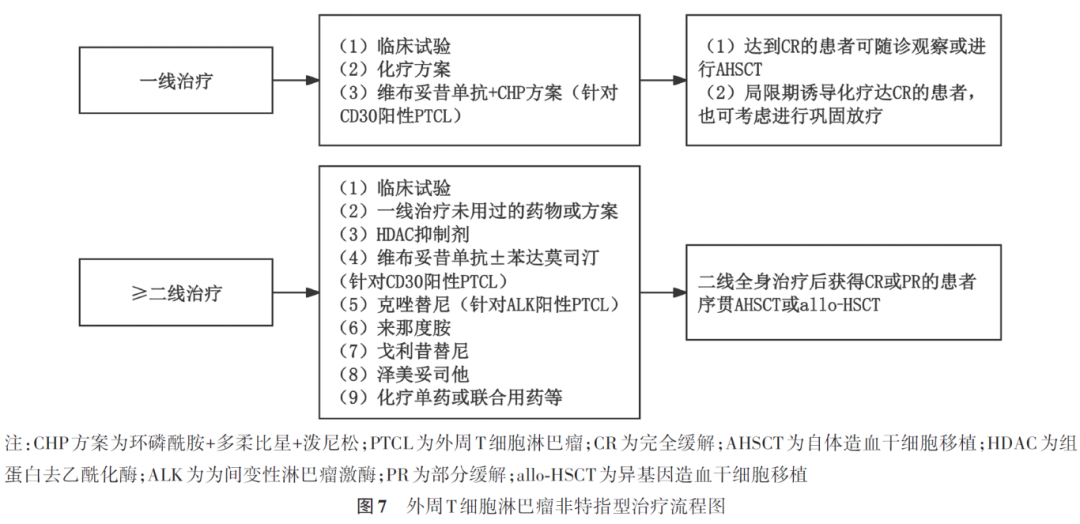
(2)复发或难治PTCL-NOS患者的治疗:首先推荐参加合适的临床试验,否则接受二线治疗(包括局部放疗)。二线治疗方案的选择要结合是否计划进行AHSCT或allo-HSCT、患者体能状态和药物不良反应等因素综合考虑。二线全身治疗后获得CR或PR的患者序贯AHSCT或allo-HSCT。二线治疗的单药方案包括西达本胺、普拉曲沙、维布妥昔单抗(针对CD30阳性PTCL)±苯达莫司汀、克唑替尼(针对ALK阳性PTCL)、吉西他滨、苯达莫司汀、来那度胺、硼替佐米、米托蒽醌脂质体、戈利昔替尼等;可供选择的联合化疗方案包括DHA+卡铂或顺铂或奥沙利铂方案、ESHA+顺铂或奥沙利铂方案、GDP方案、GVD方案、ICE方案等。基于关键性注册Ⅱ期临床研究(CHIPEL研究)结果,中国NMPA于2014年12月23日批准西达本胺上市,用于既往至少接受过1次全身化疗的复发或难治PTCL患者的治疗。基于一项Ⅱ期临床研究结果,2020年8月28日中国NMPA批准普拉曲沙上市,用于复发或难治PTCL患者的治疗。基于前期临床研究结果,2022年1月7日,米托蒽醌脂质体被中国NMPA批准上市,用于既往至少经过一线标准治疗的复发或难治PTCL成人患者的治疗。戈利昔替尼是一种JAK1抑制剂,2024年6月24日被中国NMPA批准上市,用于既往至少接受过一线系统性治疗的复发或难治的PTCL成人患者。2025年8月26日中国NMPA批准EZH2抑制剂泽美妥司他用于既往接受过至少一线系统性治疗的复发或难治PTCL成人患者。针对中国患者AITL以外的其他复发或难治PTCL患者,包括ENKTL患者,PD-1单抗单药Ⅱ期临床试验结果显示了初步的有效性,生物标志物预测PD-1单抗治疗PTCL患者的疗效正在研究中。
4. 预后
PTCL-NOS总体预后差于侵袭性B细胞淋巴瘤,国外数据显示PTCL-NOS患者的5年OS率约为30%。中国医学科学院肿瘤医院2006—2017年240例接受标准一线治疗的PTCL(不包括ENKTL)患者的5年PFS率和OS率分别为30.4%和48.8%。中国医学科学院肿瘤医院PTCL患者一线接受CHOP、CHOPE和GDP方案治疗的中位PFS分别为6.0、15.3和9.7个月,1年OS率分别为65.0%、83.3%和100%。
PTCL预后评分系统包括IPI和PTCL-NOS预后指数(prognostic index for PTCL-NOS,PIT),PIT的危险因素包括:(1)年龄>60岁,(2)LDH升高,(3)ECOG PS 2~4分,(4)骨髓受累。具有1个、2个、3个和4个危险因素的患者5年OS率分别为62.3%、52.9%、32.9%和18.3%。
(九)ENKTL
ENKTL是EBV相关淋巴瘤,90%以上的患者肿瘤组织中EBV呈阳性。ENKTL在亚洲和南美洲较常见,欧美极少见,绝大部分原发于结外。
1. 临床表现
ENKTL多见于男性,发病年龄较轻,B症状常见。肿瘤常局限于鼻腔或直接侵犯邻近结构或组织,邻近器官或结构受累以同侧上颌窦和筛窦最常见,其他依次为鼻咽、局部皮肤、硬腭、软腭、眼球和口咽等,较少有远处淋巴结受累或结外器官受累。Ⅰ~Ⅱ期患者占70%~90%,Ⅲ~Ⅳ期患者占10%~30%,Ⅲ~Ⅳ期患者常出现皮肤、胃肠道、睾丸受累和肝脾肿大。
2. 病理诊断
ENKTL病理学特征为弥漫性淋巴瘤细胞浸润,呈血管中心性、血管破坏性生长,导致组织缺血坏死及黏膜溃疡。组织坏死很常见,是导致ENKTL漏诊的主要原因。ENKTL诊断所需IHC标志物包括CD3、CD56、CD2、CD4、CD5、CD7、CD8、CD45RO、CD20、PAX5、TIA-1、granzyme B、Ki-67及EBV-EBER等。典型的ENKTL免疫表型为CD2(+)、CD3(+)、CD56(+)、TIA-1(+)、granzyme B(+)和EBV-EBER(+)。EBV-EBER阴性时诊断要谨慎,如果CD56(+)、CD3(+)、细胞毒标志物均表达可以诊断ENKTL,如果CD3(-)、CD56(-),则诊断PTCL-NOS。多数ENKTL无TCR基因重排。ENKTL还需注意与未分化癌相鉴别,应增加CK、EMA等上皮标志物检测。
3. 治疗
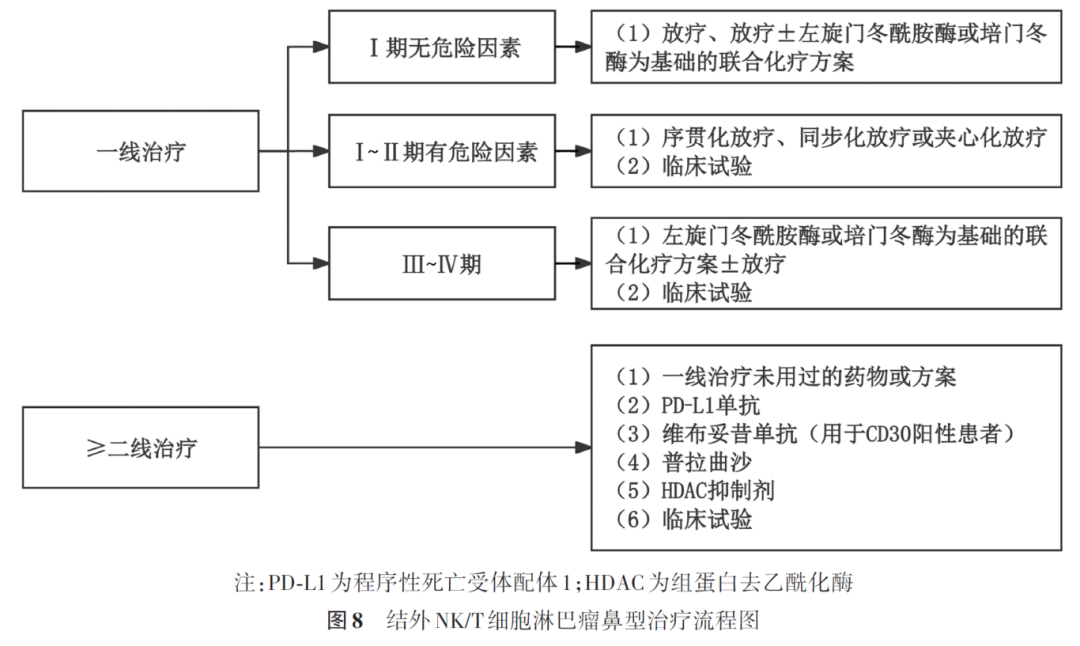
(1)ENKTL患者的一线治疗:任何期别ENKTL患者参加合适的临床试验都是最佳选择。无危险因素的Ⅰ期ENKTL患者(年龄<60岁、ECOG PS 0~1分、LDH正常、Ⅰ期无原发肿瘤局部广泛侵犯)可接受单纯放疗。有危险因素的Ⅰ期及Ⅱ期患者可采用序贯化放疗、同步化放疗或夹心化放疗。由于ENKTL对含蒽环类药物的方案疗效不佳,推荐含左旋门冬酰胺酶或培门冬酶为基础的化疗方案,包括P-GemOx方案(吉西他滨+培门冬酶+奥沙利铂)、DDGP方案(顺铂+地塞米松+吉西他滨+培门冬酶)、剂量调整的SMILE方案(甲氨蝶呤+亚叶酸钙+异环磷酰胺+美司钠+地塞米松+依托泊苷+左旋门冬酰胺酶)和AspaMetDex方案(培门冬酶+高剂量甲氨蝶呤+地塞米松)等。
Ⅲ期或Ⅳ期鼻型ENKTL和任何期别的鼻外型ENKTL患者可以采用左旋门冬酰胺酶或培门冬酶为基础的联合化疗方案±放疗。小样本前瞻性研究结果显示,应用PD-1单抗联合P-GemOx方案治疗晚期NK/T细胞淋巴瘤具有潜在疗效。对于Ⅲ期或Ⅳ期ENKTL,单纯化疗预后差,尽管AHSCT的确切价值仍存在争议,但多个回顾性研究结果表明,晚期患者化疗获得完全缓解后,可以从AHSCT获益。
(2)复发或难治ENKTL患者的治疗:首先推荐参加合适的临床试验。其他推荐方案包括单药或多药联合方案治疗。单药包括西达本胺、维布妥昔单抗(用于CD30阳性的患者)、普拉曲沙、PD-1/PD-L1单抗、戈利昔替尼、米托蒽醌脂质体等。多药联合方案包括含门冬酰胺酶的联合化疗方案(若一线未使用)、DHAP方案、DHAX方案(地塞米松、阿糖胞苷、奥沙利铂)、ESHAP方案、GDP方案、GemOx方案和ICE方案,PD-1单抗与西达本胺联合,有可能提高疗效。对于敏感复发的患者,若体能状态允许,在上述治疗获得缓解后可行AHSCT,有合适供者的患者可考虑allo-HSCT。对于化疗后局部进展或复发的患者可以考虑放疗(图8)。
4. 预后因素
ENKTL的预后模型包括NKTL预后模型(prognostic index for natural killer cell lymphoma,PINK)、PINK-E模型、诺莫图修正风险指数(nomogram-revised risk index, NRI),PINK模型包括:(1)年龄>60岁、(2)远处淋巴结侵犯、(3)Ⅲ~Ⅳ期、(4)鼻外原发。在PINK模型的基础上增加外周血EBV-DNA水平,形成了PINK-E模型。NRI指数包括5个危险因素:(1)年龄>60岁(1分);(2)Ann Arbor Ⅱ期(1分)Ann Arbor Ⅲ或Ⅳ期(2分);(3)ECOG评分≥2分(1分);(4)LDH升高(1分);(5)原发肿瘤侵犯(1分),低危(0分)、低中危(1分)、中高危(2分)、高危(3分)和很高危(≥4分)患者5年OS率分别为85.4%、78.7%、68.4%、52.5%和33.2%。
(十)MF和SS
MF和SS是最常见的皮肤T细胞淋巴瘤(cutaneous T cell lymphoma, CTCL)。MF约占CTCL的50%,SS约占CTCL的5%。中国的回顾性分析结果显示,与早期相比,晚期MF/SS患者面临较高经济负担及生活质量下降等问题。
1. 临床表现
MF临床表现为多发性皮肤红斑、斑块和瘤样结节,全身皮肤均可发生,常伴皮肤瘙痒。病程呈反复性进展,病变可局限于皮肤数月、数年、甚至数十年,在疾病晚期可发生淋巴结和内脏受累。约10%MF患者的皮肤损害是广泛性红皮病。SS为一种独特的红皮病型CTCL,伴外周血受累,循环血中异常细胞占淋巴细胞比例>5%,在受累的皮肤组织、淋巴结和外周血中可见到Sézary细胞。SS可能由斑片或斑块或红皮病型MF进展而来,也可能表现为典型的新发皮肤、血液系统和淋巴结受累。
2. 病理诊断
MF的诊断比较困难,可能需要经过数年观察、多次活检才能确诊。小的、多形核淋巴细胞聚集在表皮或表皮真皮交界处,向表皮浸润,形成Pautrier微脓肿是其特点。MF和SS典型的免疫表型为CD2(+)、CD3(+)、CD5(+)、CD4(+)、CD8(-)、CCR4(+)、TCRβ(+)和CD45RO(+),无CD7和CD26表达。一些MF亚型为CD8(+)或CD4和CD8双阴性。TCR克隆性重排对MF和SS的诊断有重要意义,流式细胞术对分期和与其他累及皮肤的淋巴瘤的鉴别诊断有重要价值。
3. 分期
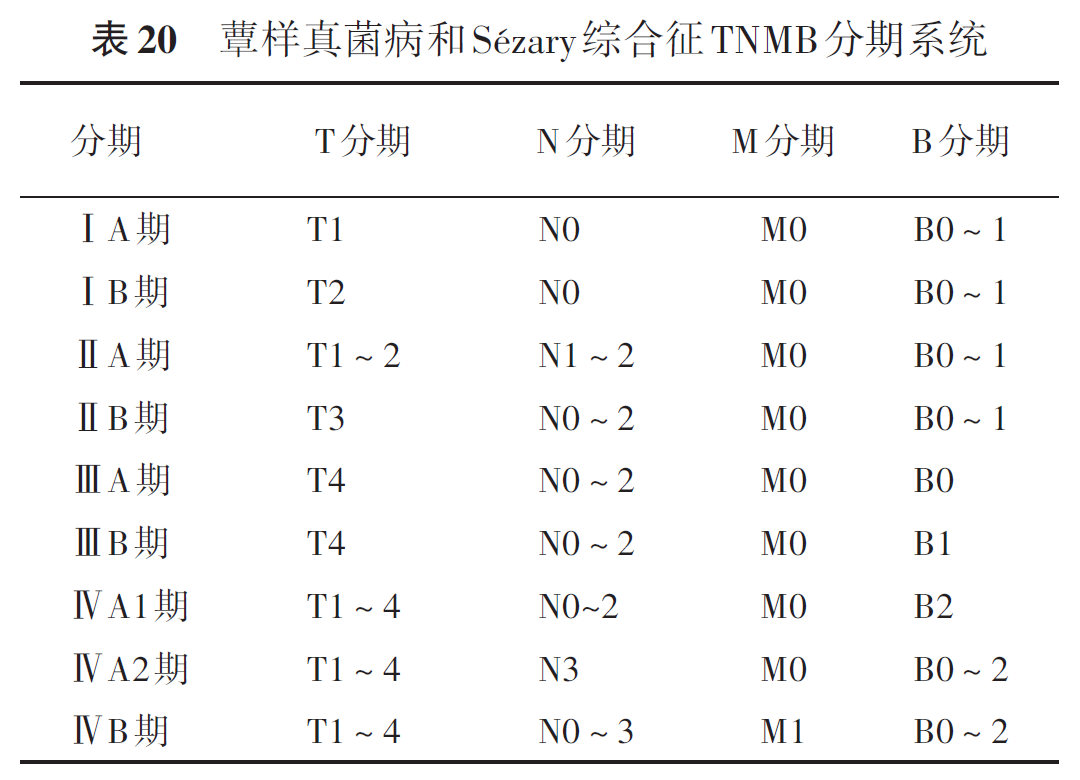
MF和SS的分期见EORT的TNMB分期系统(表19、20)。

4. 治疗
MF和SS尚无根治性治疗方法,疾病分期是确定治疗方案的主要依据。早期病变(ⅠA期和ⅡA期)采用皮肤定向疗法,当ⅠB期和ⅡA期斑块性病变的范围比较广泛或皮肤定向疗法疗效不佳时,可结合全身治疗。ⅡB期、Ⅲ期、Ⅳ期和难治性病变采用以系统治疗为主的综合治疗或参加合适的临床试验。皮肤定向疗法包括患处局部应用皮质类固醇、化疗[氮芥(HN2)或卡莫司汀]、维A酸、咪喹莫特、放疗(X射线或电子束)、光照疗法(中波紫外线或补骨脂素联合长波紫外线);全身治疗方法包括全皮肤电子束治疗(total skin electron beam therapy, TSEBT),全身性生物疗法包括小剂量甲氨蝶呤、维A酸类药物、干扰素、组蛋白去乙酰化酶抑制剂、维布妥昔单抗(CD30阳性的患者)、帕博利珠单抗、吉西他滨、脂质体阿霉素、环磷酰胺、硼替佐米、来那度胺、普拉曲沙、体外光分离置换疗法和ASHCT等。
(1)早期MF和SS患者的治疗:ⅠA期MF患者可以局部应用皮质类固醇治疗。对于斑块较薄且自然病程较为惰性的ⅠB期或ⅡA期患者,可以局部应用皮质类固醇、HN2、卡莫司汀或窄谱中波紫外线。局限的难治性病变可以局部应用贝沙罗汀、咪喹莫特或局部放疗。对于症状非常明显的泛发性厚斑块并需要迅速获得缓解的患者,建议采用TSEBT治疗或皮肤定向治疗联合全身性生物疗法。若皮肤定向治疗无效、皮肤病变广泛、症状严重或患者存在较差的预后特征,则使用全身性生物疗法。
(2)晚期或难治性MF和SS患者的治疗:晚期MF或SS通常是一种呈复发病程的慢性或持续性疾病。治疗的主要目标是尽可能长期控制疾病、迅速缓解症状以及管理危及生命的侵袭性疾病。长期控制疾病策略包括针对疾病类型和部位(如斑片或斑块、肿瘤、红皮病、皮肤外病变)的连续治疗,全身性治疗优先选择对免疫功能影响小的药物(以下全身性治疗指该类药物)。皮肤肿瘤累及体表面积较小(通常<10%体表面积)的患者,建议采用针对肿瘤的局部放疗,按需加用皮肤定向治疗。对于广泛性皮肤病变(>10%体表面积)的患者,可选择TSEBT或全身性治疗,TSEBT治疗后可进行其他皮肤定向治疗或全身性治疗,以延长疗效持续时间。对于血液系统未受累的大多数泛发性红皮病患者(≥80%体表面积),可同时采用皮肤定向治疗(如外用类固醇)和全身性治疗。对于伴有血液系统受累的患者,推荐使用全身性治疗。有临床侵袭性疾病的患者使用标准方案治疗获得长期疾病控制的可能性较小,需要更积极的治疗。对于具有侵袭性临床特征的患者,推荐使用起效较快且缓解率较高的药物。治疗选择包括伏立诺他、贝沙罗汀、维布妥昔单抗(CD30阳性患者)、莫格利珠单抗、帕博利珠单抗、单药化疗或联合化疗。对于病情难以控制的患者,可考虑allo-HSCT。基于MAVORIC研究结果,CCR4单抗莫格利珠单抗于2022年10月27日被中国NMPA批准上市,用于治疗既往接受过系统性治疗的复发或难治MF和SS患者。
5. 预后
MF患者预后较好,5年OS率约为82.2%;SS患者预后通常不佳,5年OS率为42.3%。国际皮肤淋巴瘤联合会的回顾性研究结果显示,MF和SS患者独立不良预后危险因素包括:(1)Ⅳ期病变,(2)年龄>60岁,(3)LDH升高,(4)皮肤大细胞转化。低危(0~1个危险因素)、中危(2个危险因素)和高危组(3~4个危险因素)的5年OS率分别为68%、44%和28%。
淋巴瘤是一类异质性很强的恶性肿瘤,近年来,对于淋巴瘤的一些特殊情况,如淋巴瘤相关噬血细胞综合征等临床问题的认识也逐渐深入,在诊疗过程中需要多学科协作,结合患者的个体特征来制定治疗方案,从而提高诊断和治疗水平,改善患者预后。
由于临床实践中患者的具体情况存在较大的个体差异以及我们的水平有限,本指南仅供参考,不具有法律效力。
参考文献略。
纸质版期刊订阅:中国邮政网上营业厅(https://11185.cn/)检索“中华肿瘤杂志”在出版前订购;或中华医学期刊网-期刊服务-期刊商城订购过刊。
专家组顾问
孙燕(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
专家组组长
石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,航天中心医院肿瘤中心)
专家组成员(按姓氏汉语拼音字母排序)
白鸥(吉林大学第一医院血液科)
蔡清清(中山大学肿瘤防治中心肿瘤内科)
曹军宁(复旦大学附属肿瘤医院肿瘤内科)
岑洪(广西医科大学第一附属医院肿瘤内科)
崔杰(甘肃省肿瘤医院肿瘤内科)
冯晓莉(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院病理科)
高玉环(河北医科大学第四医院血液科)
顾康生(安徽医科大学第一附属医院肿瘤内科)
桂琳(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
韩晓红(中国医学科学院北京协和医院临床药理中心 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
何娟(中国医科大学附属第一医院血液内科)
何小慧(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
胡建达(福建医科大学附属第二医院血液科)
金洁(浙江大学医学院附属第一医院血液科)
姜时雨(复旦大学附属肿瘤医院肿瘤内科)
景红梅(北京大学第三医院血液内科)
克晓燕(北京大学第三医院血液科)
廖爱军(中国医科大学附属盛京医院血液内科)
刘代红(解放军总医院血液病医学部)
刘辉(北京医院血液内科)
刘海生(河北医科大学第四医院)
李建勇(江苏省人民医院血液科)
李文瑜(广东省人民医院淋巴瘤科)
李小秋(复旦大学附属肿瘤医院病理科)
李晓玲(辽宁省肿瘤医院肿瘤内科)
李玉富(河南省肿瘤医院血液科)
李增军(山东省肿瘤医院淋巴血液科)
李志铭(中山大学肿瘤防治中心肿瘤内科)
刘鹏(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
刘瑛(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院PET⁃CT中心)
林华(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院病案室)
卢学春(解放军总医院第二医学中心血液科)
彭志刚(广西医科大学第一附属医院血液内科)
钱文斌(浙江大学医学院附属第二医院血液科)
秦燕(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
苏航(解放军总医院第五医学中心)
孙秀华(大连医科大学附属第二医院肿瘤内科)
石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,航天中心医院肿瘤中心)
双跃荣(江西省肿瘤医院肿瘤内科)
宋永平(河南省肿瘤医院血液科)
苏丽萍(山西省肿瘤医院血液科)
孙燕(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
陶云霞(徐州医科大学附属医院肿瘤内科)
王华庆(南开大学天津市人民医院肿瘤内科)
王章桂(航天中心医院肿瘤中心)
王昭(首都医科大学附属北京友谊医院血液科)
吴剑秋(江苏省肿瘤医院肿瘤内科)
吴晓雄(解放军总医院第一附属医院血液科)
邢晓静(辽宁省肿瘤医院肿瘤内科)
徐兵(厦门大学附属第一医院血液内科)
颜晓菁(中国医科大学附属第一医院血液科)
杨海燕(浙江省肿瘤医院肿瘤内科)
杨顺娥(新疆维吾尔自治区肿瘤医院肿瘤内科)
杨瑜(福建省肿瘤医院淋巴瘤内科及头颈肿瘤内科)
杨建良(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
杨晟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
杨向红(中国医科大学附属盛京医院病理科)
薛宏伟(青岛大学附属医院淋巴瘤科)
薛学敏(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院病理科)
徐小红(江苏省南通肿瘤医院肿瘤内科)
许景艳(南京鼓楼医院血液科)
张长弓(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
张会来(天津医科大学附属肿瘤医院肿瘤内科)
张利玲(华中科技大学同济医学院附属协和医院肿瘤中心)
张清媛(哈尔滨医科大学附属肿瘤医院肿瘤内科)
张明智(郑州大学第一附属医院肿瘤内科)
张伟京(首都医科大学附属北京世纪坛医院肿瘤内科)
张雯杰(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院PET⁃CT中心)
赵征(陕西省肿瘤医院肿瘤内科)
周辉(湖南省肿瘤医院淋巴瘤血液内科)
周生余(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
周泽平(昆明医科大学第二附属医院血液科)
钟巧凤(福建医科大学肿瘤临床医学院 福建省肿瘤医院肿瘤内科)
邹立群(四川大学华西医院血液科)
学术秘书(按姓氏汉语拼音字母排序)
陈馨蕊(解放军总医院第二医学中心肿瘤科)
高茹云(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
黄莉玲(中日友好医院血液科)
唐乐(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
谢祖成(浙江省肿瘤医院淋巴瘤科)
杨梦薇(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
朱豪华(航天中心医院肿瘤中心)
志谢
感谢高玉环(河北医科大学第四医院血液科)、胡建达(福建医科大学附属第二医院血液科)、克晓燕(北京大学第三医院血液科)、李增军(山东省肿瘤医院淋巴血液科)、刘海生(河北医科大学第四医院)、孙秀华(大连医科大学附属第二医院肿瘤内科)、王昭(首都医科大学附属北京友谊医院血液科)、杨建良(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、杨晟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、张雯杰(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院PET⁃CT中心)、周辉(湖南省肿瘤医院淋巴瘤血液内科)、钟巧凤(福建医科大学肿瘤临床医学院 福建省肿瘤医院肿瘤内科)在指南撰写过程中提出的宝贵意见和建议
来源:中华肿瘤杂志