春风送暖,芳华绽放。在3・8国际妇女节这个专属女性的美好节日里,我们致敬每一位独立、坚韧、闪耀的她。
今天,我们聚焦威胁女性健康的“头号杀手”——乳腺癌。作为全球女性最常见恶性肿瘤、女性癌症死亡首要原因,乳腺癌始终是女性健康的核心挑战。
近日,浙江省肿瘤医院陈天辉教授团队发表在MedComm(中科院一区)的一篇重磅综述“Breast Cancer: Molecular Pathogenesis, Targeted Therapy, Screening, and Prevention”,融合临床前沿进展,为临床医生、科研人员及广大女性朋友,系统梳理乳腺癌分子发病机制、靶向治疗、筛查和预防的最新进展,用科学守护“她”健康。

一、全球防控现状: 直面“粉红杀手”,精准医疗成破局关键 最新数据显示,2022年全球乳腺癌新发病例达230万,死亡病例67万,占女性新发癌症的25%、癌症死亡的15.5%;预计到2050年,发病率将上升38%,死亡率上升68%,中低收入国家成为重灾区。 乳腺癌并非单一疾病,而是高度异质性的恶性肿瘤,临床通常基于ER、PR、HER2、Ki-67将乳腺癌分为Luminal A、Luminal B、HER2富集型、三阴性乳腺癌(TNBC)四大亚型,不同亚型的预后、治疗方案天差地别。而多组学、单细胞测序、AI技术的突破,正让乳腺癌从“一刀切”的传统治疗,迈向分型而治、精准施策的全新时代。 二、解码发病根源: 从分子层面看懂乳腺癌的发生 乳腺癌的发生是遗传、表观遗传、信号通路、肿瘤微环境共同作用的结果,这也是精准治疗的核心理论基础: 遗传突变:BRCA1/2是遗传性乳腺癌最主要致病基因,终身患病风险超60%。TP53、PIK3CA、ESR1等体细胞突变,直接驱动肿瘤恶变,也是关键治疗靶点。 表观调控:DNA甲基化、组蛋白修饰、非编码RNA可在不改变DNA序列的情况下调控基因表达,成为早期筛查与新药研发的新方向。 核心信号通路:PI3K/AKT/mTOR、ER、MAPK、CDK4/6-Rb等通路异常活化,是肿瘤增殖、耐药的核心机制。 肿瘤微环境(TME):免疫抑制细胞(TAMs、Tregs、MDSCs)、癌症相关成纤维细胞(CAFs)构建“免疫逃逸”微环境,成为免疫治疗的关键靶点。 图1 解读:乳腺癌发生发展的关键分子机制 该图系统总结了驱动乳腺癌的四大机制:(A)遗传与基因组改变(如BRCA1/2, PIK3CA, ESR1);(B)表观遗传与转录调控(如DNA甲基化、ncRNA);(C)关键致癌信号通路(PI3K/AKT/mTOR, CDK4/6-Rb, ER通路);(D)肿瘤微环境与免疫逃逸(Treg, TAMs, CAF的作用)。这为后续的靶向治疗提供了理论基石。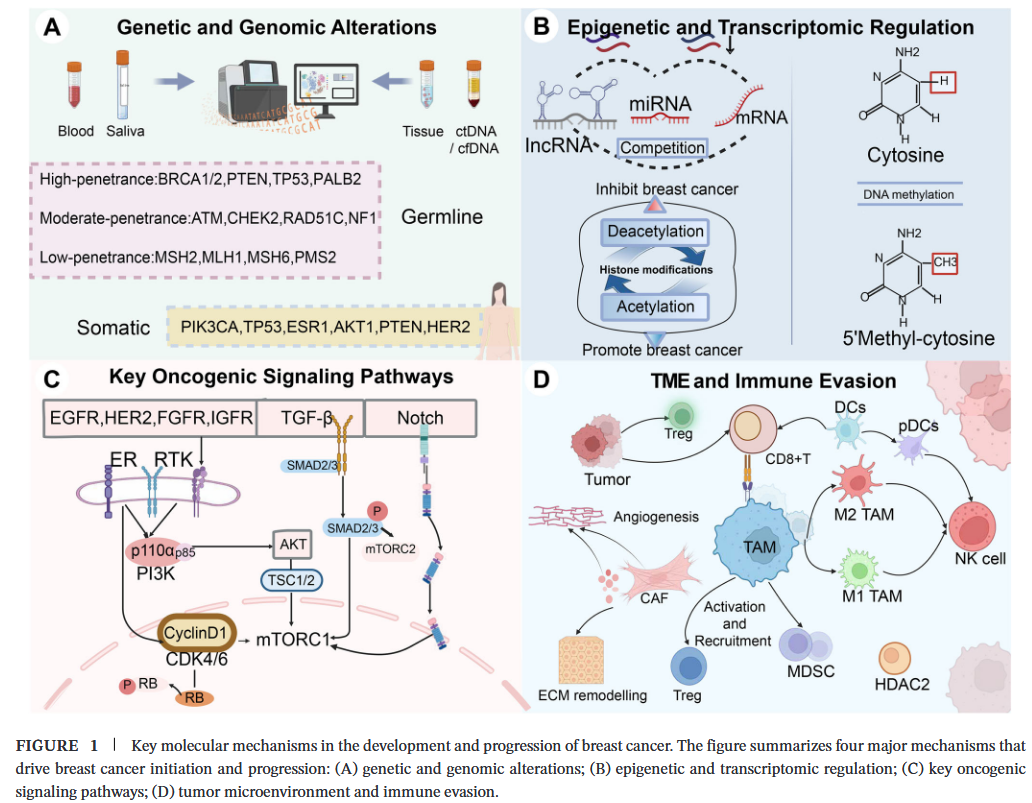
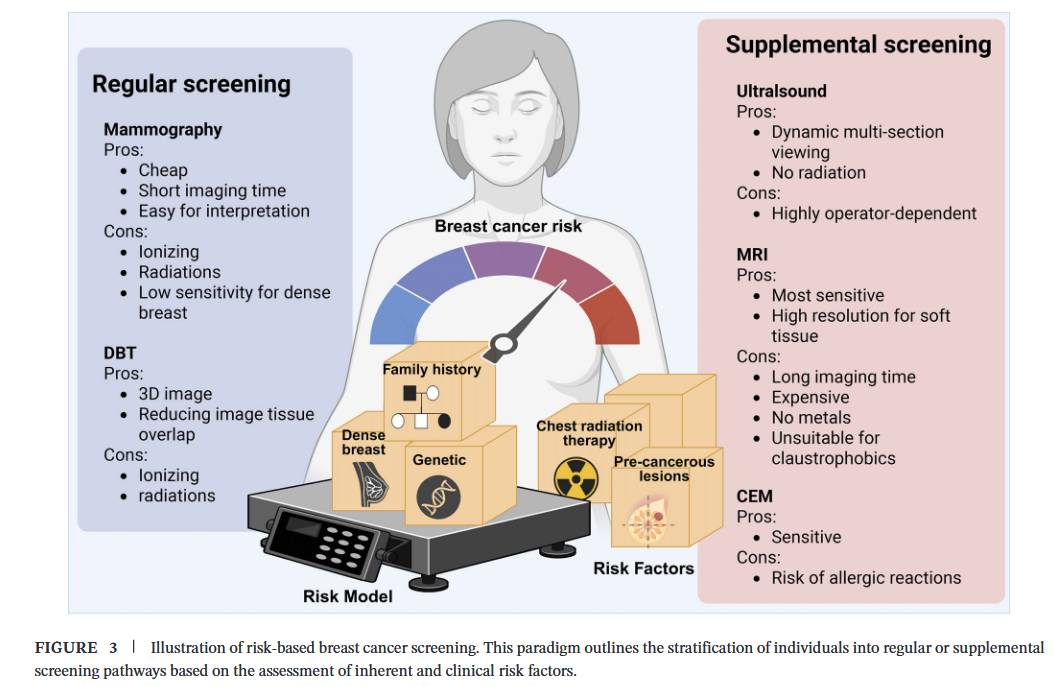
三、靶向治疗: 百花齐放的“黄金时代” 近五十年来,乳腺癌靶向治疗取得长足进展。从1970年代他莫昔芬获批至今,全球已有至少35种靶向药物应用于临床,乳腺癌治疗已全面进入精准医学时代。综述重点囊括了截至2025/2026年的最新临床试验数据(如INAVO120, CAPItello-291, VERITAC-2等),解析了目前靶向治疗的高光进展和痛点与挑战。 图2 解读:乳腺癌靶向药物获批时间轴清晰展示了五十年来的药物进化史。从1970年代的他莫昔芬,到2020年前后爆发的ADC药物(T-DXd, SG)及新型口服SERD、AKT抑制剂等,见证了乳腺癌治疗的极速变革。 内分泌治疗:激素受体阳性乳腺癌的基石 对于占乳腺癌大部分的激素受体阳性患者,内分泌治疗是核心手段。这类药物通过阻断雌激素对癌细胞的刺激作用来抑制肿瘤生长。 他莫昔芬作为经典药物,既能治疗乳腺癌,也可用于高危女性的预防。最新研究发现,低剂量他莫昔芬可显著降低非浸润性癌复发风险,且副作用更小。 口服SERD药物是近年来的重大突破。Elacestrant是目前唯一获批用于ESRI突变患者的口服SERD药物,为内分泌治疗耐药患者带来新选择。最新公布的SERENA-6试验数据显示,新一代口服SERD药物Camizestrant联合CDK4/6抑制剂一线治疗可使中位无进展生存期(PFS)从9.2个月延长至16.0个月。 HER2靶向治疗:从预后最差到治疗典范 HER2阳性乳腺癌曾经预后极差,但现已成为靶向治疗最成功的亚型。 曲妥珠单抗的临床应用是乳腺癌治疗史上的里程碑。随后,帕妥珠单抗与曲妥珠单抗的联合应用进一步提高了疗效。对于发生脑转移的患者,拉帕替尼和图卡替尼等小分子TKI药物能有效穿过血脑屏障,展现独特治疗优势。 抗体药物偶联物(ADC)的问世带来了革命性突破。T-DXd不仅对HER2阳性乳腺癌有效,还扩展至HER2低表达甚至超低表达患者,重新定义了HER2的治疗边界。最新研究证实,T-DXd对乳腺癌脑转移具有显著且持久的疗效。 细胞周期和DNA修复靶向治疗 CDK4/6抑制剂联合内分泌治疗已成为激素受体阳性/HER2阴性晚期乳腺癌的一线或二线标准方案。Ribociclib联合来曲唑可延长总生存期(OS)超过12个月,Dalpiciclib在DAWNA-2试验中也展现出显著疗效。 PARP抑制剂为BRCA1/2突变患者带来精准治疗选择。奥拉帕利在OlympiA试验中被证实可改善gBRCA突变早期乳腺癌的OS。 PI3K/AKT/mTOR通路抑制剂 该信号通路在乳腺癌中频繁异常激活,与内分泌治疗和CDK4/6抑制剂耐药密切相关。 Alpelisib是首个口服α选择性PI3K抑制剂,用于PIKCA突变患者。最新获批的Inavolisib联合治疗显著延长PFS和OS。Capivasertib作为AKT抑制剂,在CAPItello-291研究中显示出一致的PFS获益。 Trop-2 ADC的双星闪耀 三阴性与HR+乳腺癌的全覆盖抗体偶联药物(ADC)正在重塑晚期乳腺癌的治疗格局,其中靶向Trop-2的ADC药物表现尤为抢眼:Sacituzumab Govitecan不仅是三阴性乳腺癌的有力武器,更在HR+/HER2-晚期乳腺癌中确立了地位。Sacituzumab Tirumotecan (SKB264):国产创新药在三阴性乳腺癌后线治疗中展现出潜力。 免疫治疗:为三阴性乳腺癌带来突破 三阴性乳腺癌曾被视为侵袭性强、治疗选择有限的亚型,免疫治疗的出现改变了这一局面。 帕博利珠单抗联合化疗在KEYNOTE-355试验中显著延长了PD-L1阳性转移性三阴性乳腺癌患者的PFS和OS。在早期阶段,KEYNOTE-522试验证实新辅助化疗联合帕博利珠单抗并继续辅助治疗,可显著改善无事件生存期(EFS)和OS。 四、乳腺癌风险分层: 从“大众化”走向“个性化” 风险因素 遗传因素:BRCA1/2基因突变是最常见的高外显率遗传风险因素。BRCA1突变携带者至80岁时患乳腺癌风险约为72%,BRCA2携带者约为69%。其他相关基因包括PALB2、PTEN、TP53、ATM和CHEK2等。 家族史:一级亲属患乳腺癌人数越多,个体风险越高。 个人病史:曾患乳腺非典型增生、小叶原位癌或导管原位癌者风险显著增加。 放射线暴露:童年或青春期接受胸部放疗者,终身风险可增加8倍。 乳腺密度:致密型乳腺女性患病风险是脂肪型女性的4-6倍。 生活方式因素:肥胖、缺乏运动、饮酒、夜班工作等。 风险评估模型 传统模型如GAIL模型基于易测风险因素,但未纳入BRCA突变信息。BOADICEA和IBIS模型则整合了遗传和非遗传因素,预测性能更优。 多基因风险评分是当前研究热点,通过整合多个SNP位点,可更精确评估个体遗传易感性。但需注意的是,目前大多数研究基于欧洲人群,在非欧洲人群中的应用需谨慎验证。 五、筛查技术: 从“金标准”到多元化,把癌症拦在早期 筛查不再是简单的“每年一次钼靶”,而是基于风险的精准决策。 金标准 乳腺钼靶:优势与局限 钼靶筛查可降低50-70岁女性乳腺癌死亡率约20%。但在致密型乳腺女性中,敏感性下降10-20%,年轻女性尤其明显。召回率在不同国家差异显著(2%-27%),过度诊断问题一直存在争议。 技术革新 数字乳腺断层合成:3D技术的突破 DBT通过重建三维图像,有效解决了传统二维钼靶的组织重叠问题。大型队列研究显示,DBT可使检出率从每千名女性4.5例提高到5.3例,同时降低召回率。但设备成本和解读时间增加是其推广应用的主要障碍。 超声:致密乳腺的重要补充 超声检查无辐射,对致密乳腺尤其有价值。J-START试验显示,超声联合钼靶可将敏感性从77.0%提高到91.1%。但特异性相应降低,假阳性率和不必活检增加,且检查结果高度依赖操作者经验。 磁共振:高危女性的优选方案 MRI具有最高敏感性,尤其适用于BRCA突变等高危女性。但成本高、检查时间长、假阳性率高限制了其广泛应用。MRI简化序列可大幅缩短扫描时间,同时保持诊断性能,为改善可及性带来希望。 对比增强钼靶(CEM):折衷方案 CEM结合了钼靶的可及性和MRI的对比增强特性。研究显示,与标准MRI相比,CEM可降低假阳性召回和活检率,采集和解读时间更短。但其癌症检出率和敏感性仍低于MRI。 新兴技术:无创检测的探索 呼气分析通过检测癌细胞特异性代谢产生的挥发性有机化合物,实现完全无创筛查。早期临床研究显示,其敏感性和特异性分别达到89.2%和87.7%。 基于DNA甲基化的液体活检展现出巨大潜力。从宫颈或口腔拭子中检测DNA甲基化改变,可有效识别乳腺癌高危女性,为整合到常规妇科或牙科实践提供了可能。 图3 解读:基于风险的乳腺癌筛查新范式 图示强调了根据个体风险因素(遗传、致密型乳腺、家族史等)选择筛查路径。普通风险人群推荐钼靶;致密型乳腺推荐联合DBT或超声;高危人群(如BRCA突变携带者)则必须纳入MRI。
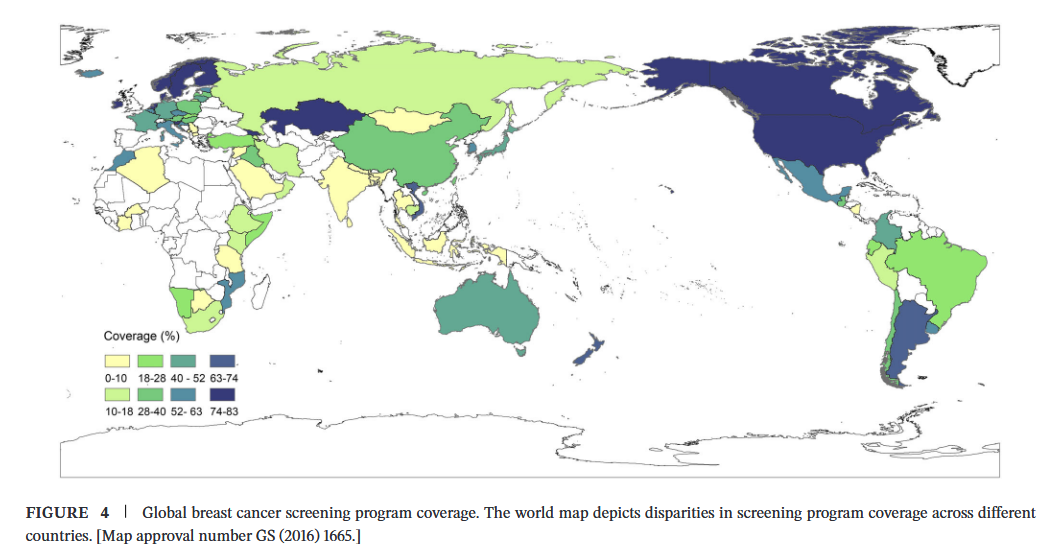
六、风险干预手段 1. 可控危险因素:控制体重、每周≥150分钟中等强度运动、限制酒精摄入、避免熬夜、远离胸部辐射; 2. 不可控危险因素:携带高外显率遗传突变等,需定期检测与强化筛查。 精准预防:高风险女性的选择 药物预防 多项随机试验证实,选择性雌激素受体调节剂(他莫昔芬、雷洛昔芬)和芳香化酶抑制剂(阿那曲唑、依西美坦)可显著降低乳腺癌风险。荟萃分析显示,与安慰剂相比,他莫昔芬风险比0.69,雷洛昔芬0.44,AIs 0.45。 STAR试验显示,他莫昔芬在降低长期乳腺癌风险方面优于雷洛昔芬,但雷洛昔芬不良事件更少(子宫内膜癌RR=0.55,子宫增生RR=0.19,血栓事件RR=0.75)。 尽管临床获益明确,药物预防仍未被充分利用,主要障碍是女性对副作用的担忧(血栓事件、子宫内膜癌、白内障、血管舒缩症状和肌肉骨骼不适)。 预防性手术 降低风险乳房切除术可使乳腺癌风险降低90%。BRCA1/2携带者或30岁前胸部放疗者获益最大。 对于BRCA1/2携带者,完成生育后建议同时行降低风险输卵管卵巢切除术,可显著降低BRCA相关癌症风险。但雌激素和孕激素水平下降会导致更年期症状、骨质疏松、心血管疾病等问题。激素替代治疗可缓解症状,且不会削弱RRSO的保护效应。 七、乳腺癌防治的局限与挑战: 未完成的拼图 尽管进展喜人,综述也冷静地列出了当前面临的严峻挑战,这些也是未来的科研突破口: 耐药机制的复杂性:尽管有新型SERD和PI3K抑制剂,但肿瘤仍会通过旁路激活、表型转化(如转为ER阴性)产生再次耐药。如何克服ADC药物的耐药(如抗原丢失、内吞障碍)仍是未解之谜。 毒性管理:ADC药物带来的间质性肺病仍是致死性风险;PI3K抑制剂的高血糖问题虽有改善(如Inavolisib),但仍需精细化管理。 新兴技术的临床效用:ctDNA虽然能监测微小残留病灶(MRD),但其指导治疗调整能否最终转化为OS获益,仍需更多前瞻性数据支持。 筛查的过度诊断:尤其是针对老年女性(>75岁)和年轻女性(40-49岁),以及筛查的频率如何设置,如何在提高检出率的同时避免过度治疗,尚无完美答案。 种族与数据偏差:现有的基因组数据库(如TCGA)和PRS(多基因风险评分)模型多基于欧洲人群,对亚洲、非洲人群的适用性存疑。 全球资源不平等:截至2021年,63%的WHO成员国报告了国家筛查策略,覆盖率从丹麦的83%到北马其顿的0.25%不等,高收入国家通常拥有成熟的组织化项目,而许多中低收入国家面临资源限制。中国筛查参与率从2014年的20%上升到2022年的50%以上,但区域差异显著,北京超过80%,中西部省份低于40%。 图4 解读:全球乳腺癌筛查率地图展示了全球筛查覆盖率的巨大差异。 八、未来展望:多组学融合与AI赋能 单细胞RNA测序可在单细胞水平解析转录组,揭示治疗耐药和克隆演化机制。空间转录组学更进一步,保留了细胞在组织中的空间位置信息,为深入理解肿瘤微环境提供全新视角。 人工智能在多模态数据整合中展现出巨大潜力。基于深度学习的Mirai模型仅凭单次筛查钼靶即可预测5年乳腺癌风险,性能与传统模型相当甚至更优。AI还能预测患者特异性治疗反应,加速新药设计和筛选。 乳腺癌的诊疗正在从“循证医学”向“数据驱动的精准医学”跨越。随着多维组学(multi-omics)整合与AI的深度融合,我们终将实现对每一位患者的“量体裁衣”。 结语 乳腺癌管理正在从“一刀切”向高度个体化转变,精准预防、精准筛查、精准治疗的理念贯穿始终。精准医疗已不再是口号,而是触手可及的现实。但治疗耐药、药物毒性、成本效益和全球可及性不平等仍是待解决的挑战。 多组学技术、空间生物学和人工智能的融合,有望进一步拓宽乳腺癌研究和临床照护的可能性。但技术创新的最终目标是服务于患者,在推动精准医学发展的同时,保持技术创新与以患者为中心的照护之间的平衡。 愿每一位女性都能被温柔以待,更能拥有守护健康的底气。乳腺癌不再是“不治之症”,精准治疗让晚期患者实现长期生存,早筛早防让健康隐患无处遁形。 在这个专属女性的节日里,愿我们都能重视乳腺健康,定期筛查、科学预防;也愿临床与科研的每一步突破,都能为“她”撑起健康保护伞,让芳华无惧,美丽长存! *温馨提示:本文基于Lei等发表于MedComm 2026的综述整理,仅供临床参考与科普学习,具体诊疗方案请遵医嘱。 第一作者和通讯作者简介: 第一作者:雷慧君 博士 澳门大学与中国科学院杭州医学研究所首届联合培养博士研究生,研究方向为乳腺癌的遗传学及分子流行病学研究。以第一作者/共同作者在国际知名期刊Seminars in Cancer Biology, MedComm, Human Genomics, Journal of Translational Medicine, Neoplasia等发表论文16篇,获授权国家发明专利1项,深度参与多项国家重点研发计划重点专项项目,参编专著/译著5部。 通讯作者:陈天辉 教授 浙江省万人计划科技创新领军人才,研究员/教授、肿瘤学及生物学博士研究生导师、浙江大学医学博士学位(2006年),曾在欧洲学习和工作十年(其中德国国家癌症研究中心DKFZ七年)。现任浙江省肿瘤医院防治科副主任&中国科学院杭州医学所双聘PI。兼任中国抗癌协会6个专委会常务委员(肿瘤流行病学、环境肿瘤学、恶性间皮瘤、肿瘤基因诊断等),国家科技奖励评审专家库成员、国家科技专家库成员、浙江省科技厅A级专家等。 “肿瘤流行病学与预防”课题组PI、分子流行病学专业,团队聚焦三个主攻方向:①石棉暴露所致癌症的人群防控研究;②癌症早筛综合效果评估:周期法提供及时准确的癌症5年相对生存率;③乳腺癌等遗传性肿瘤的分子遗传流行病学及筛查研究。作为课题负责人主持国家重点研发计划“政府间国际科技创新合作”重点专项项目、十五五“四大慢病”国家科技重大专项课题、十四五国家重点研发计划“常见多发病防治研究”重点专项课题等。主编/主译出版专著5部、副主编“十四五”普通高等教育研究生规划教材1部;获授权国家发明专利1项、软件著作权5项;累计发表SCI论文115篇,其中70篇为通讯/第一作者包括4篇JAMA子刊。