2026年3月4日,北京大学未来技术学院、北京大学-清华大学生命科学联合中心何爱彬团队,联合北京大学第三医院血液内科景红梅团队、中国人民解放军总医院血液病医学部窦立萍团队和上海交通大学医学院基础医学院郑俊克团队在国际权威期刊Nature(《自然》)上,在线发表了题为“Cell-free chromatin state tracing reveals disease origin and therapy responses”(游离DNA染色质状态检测技术揭示疾病起源与治疗应答)的文章。
该研究开发了一项名为cf-EpiTracing(cell-free EpiTracing)的创新液体活检技术平台,通过检测血浆中游离染色质的多组蛋白修饰信息,结合机器学习算法,实现了对疾病受累组织和细胞类型的高灵敏度无创识别,在淋巴瘤诊治的临床应用中展现出巨大潜力。

临床痛点亟待破解,技术创新应运而生
淋巴瘤是最常见的血液系统恶性肿瘤之一,其中B细胞淋巴瘤占比超过 85%。弥漫大B细胞淋巴瘤(DLBCL)、滤泡性淋巴瘤(FL)和套细胞淋巴瘤(MCL)是最主要的亚型,不同亚型在治疗策略和预后上存在显著差异——例如FL预后相对良好,而DLBCL侵袭性强、预后较差,MCL则以复发率高为主要特征。然而,目前淋巴瘤的精确分型和预后评估仍高度依赖有创组织活检和传统临床指标,不仅给患者带来身体痛苦和风险,还存在取样局限、无法动态监测等弊端,亟需更加便捷、精准的无创检测手段。
为此,研究团队另辟蹊径,开发了cf-EpiTracing技术。其核心创新在于,突破了传统液体活检主要依赖DNA突变或甲基化信息的局限,聚焦血浆游离核小体上的组蛋白修饰可反映其起源组织器官的原理——细胞凋亡或坏死释放的游离染色质携带了来源组织的特异性表观遗传印记,而组蛋白修饰作为表观遗传调控的关键形式,能够精准表征细胞的功能状态和组织特性。
研究团队通过大量实验验证发现,仅需不到100微升血浆,通过自动化高通量检测少至三种关键组蛋白修饰(H3K9ac、H3K27ac和 H3K4me3),结合多变量隐马尔可夫模型(ChromHMM),即可构建 18种整合染色质状态(ICS),从而无偏倚地识别疾病来源的组织和细胞类型。与既往基于转录组的方法不同,cf-EpiTracing直接解读染色质的整合表观遗传状态,溯源病变器官与细胞,信息维度更丰富,检测灵敏度更高。
三大临床突破,重塑淋巴瘤诊疗模式
突破1:无创实现淋巴瘤精准分型
研究团队对309例B细胞淋巴瘤患者(含DLBCL、FL、MCL等主要亚型)的血浆样本分析发现,不同亚型具有独特的整合染色质状态(ICS)图谱。依托细胞类型特异性表观遗传信号,该技术可有效鉴别不同细胞起源的淋巴瘤亚型,多分类AUC达0.823。针对DLBCL的细胞起源(COO)分型,可精准区分生发中心B细胞型(GCB)和活化B细胞型(ABC),性能优于传统RNA-seq方法。
更具临床价值的是,该技术能够动态捕捉疾病亚型转化。通过对6例FL向DLBCL转化患者的纵向监测,cf-EpiTracing清晰呈现了这一过程中的表观遗传动态变化,识别出26个关键转化相关标志物及BCL6、MYC等驱动转录因子的异常激活,为及时调整治疗策略提供了分子预警。此外,该技术还显著提升了套细胞淋巴瘤特征性染色体易位t(11;14)的检出效能,解决了传统外周血检测灵敏度不足的难题。
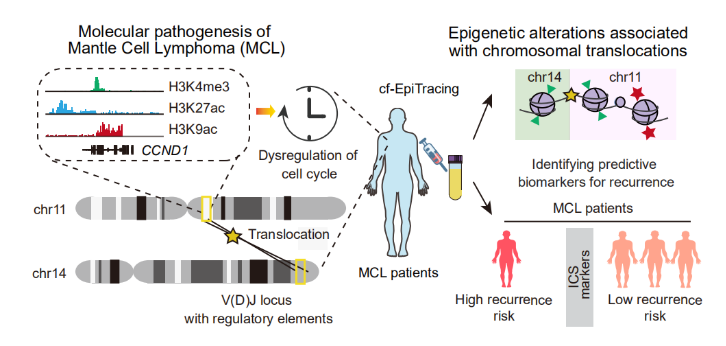
cf-EpiTracing检测技术可于外周血发现套细胞淋巴瘤染色体易位
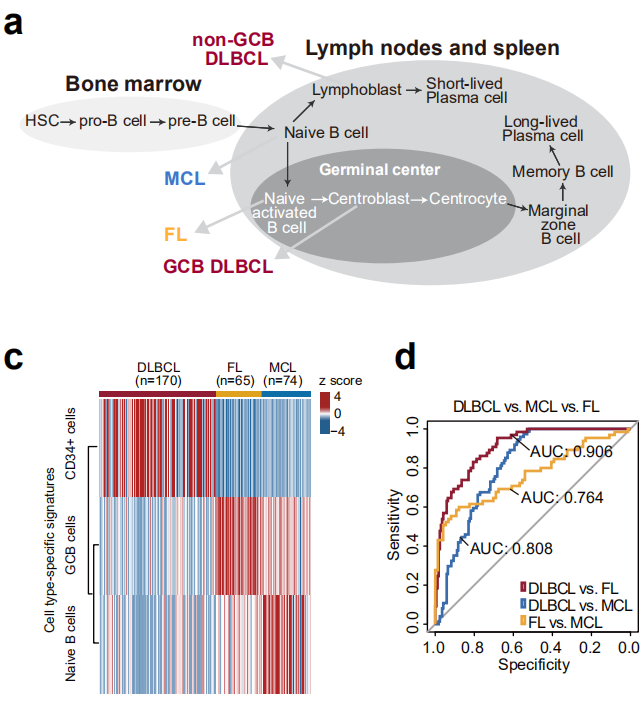
cf-EpiTracing检测技术可对不同细胞起源的淋巴瘤亚型进行有效区分
突破2:预后预测优于传统临床指标
精准的预后评估是制定个体化治疗方案的关键,但现有临床指标(如R-IPI、β2-微球蛋白等)对淋巴瘤预后的预测效能有限。cf-EpiTracing定义的表观遗传特征展现出更卓越的预后预测能力,为患者风险分层提供了新的分子依据。
在DLBCL患者中,基于ICS的表观遗传标志物能够有效预测患者的治疗反应和生存结局,其预测效能显著优于目前临床常用的修订版国际预后指数(R-IPI)。这一发现在研究队列和大规模公共数据集中获得一致结果,充分证明该方法的稳健性和临床转化潜力。在MCL患者中,研究团队识别出18个与高复发风险显著相关的ICS标志物,其预测复发事件的能力明显优于β2-微球蛋白、LDH水平和年龄等传统临床指标,为MCL患者的风险分层和个体化治疗决策提供了新的分子依据。
突破3:捕捉疾病早期转化与衰老相关风险
疾病早期干预和风险预警是改善淋巴瘤预后的关键,cf-EpiTracing技术在疾病早期检测和发病机制探索方面取得重要进展。
该技术能够在临床症状出现前捕获早期表观遗传异常。团队通过系统追踪 FL向DLBCL的恶性转化过程,揭示了转化过程中增强子区域染色质重塑、细胞增殖通路表观激活等关键分子事件,为理解淋巴瘤恶性进展机制提供了全新视角,也为开发早期干预靶点创造了条件。
同时,研究发现MCL的发病与衰老相关表观遗传异常密切相关。健康人群中部分ICS信号随年龄增长呈现规律性变化,而MCL患者中这些衰老相关特征更为显著,涉及信号转导、细胞黏附等通路失调。进一步研究证实,WASF1、PRKN、NEDD4L和CREBBP等与细胞增殖和周期调控相关的转录因子在MCL患者中显著高表达,而在健康老年人中未见此现象,这一发现为解析淋巴瘤发病的年龄相关机制提供了重要线索,也为制定针对性预防策略提供了潜在靶点。
结语:
迈向一体化的无创表观遗传组学时代
cf-EpiTracing技术的问世,是液体活检领域从“基因”维度迈向“表观遗传组”维度的一次重要飞跃。它以自动化、微量化、多维度的优势,成功地将血浆中游离染色质所蕴含的丰富信息转化为可直接指导临床决策的精准工具,实现了从早期筛查、精准分型、预后评估到疗效监测的淋巴瘤全周期无创管理。这一创新平台的应用前景远不止于血液肿瘤,其在结直肠癌、冠心病乃至炎性疾病中展现出的组织溯源能力,预示着它有望成为一种普适性的、能够揭示全身组织器官病理状态的“全景式”无创检测技术。
北京大学未来技术学院陈旭斌、北京大学-清华生命科学联合中心孟晓萱、北京大学第三医院血液内科张伟龙、中国人民解放军医学院血液病医学部张夏威为共同第一作者;何爱彬、景红梅、窦立萍、郑俊克为共同通讯作者。
共同第一作者

张伟龙
血液内科主治医师
副研究员、硕士生导师
主要研究方向:
淋巴瘤的分子分型及精准治疗
共同通讯作者

景红梅
北医三院血液内科主任
主任医师、教授、博士生导师
主要研究方向:淋巴瘤相关基础及临床研究
了解更多:https://www.puh3.net.cn/xynk/info/1461/1511.htm
来源:北京大学第三医院