2026年2月24日,东南大学附属中大医院滕皋军院士团队在Journal of Clinical Oncology发表了CHANCE2005/CARES-005随机II期临床试验结果,题为“Transarterial Chemoembolization Combined With Camrelizumab and Rivoceranib for Unresectable Hepatocellular Carcinoma (CHANCE2005/CARES-005): A Randomized Phase II Trial”。该研究探索了经动脉化疗栓塞(TACE)联合卡瑞利珠单抗和阿帕替尼对比单纯TACE治疗不可切除肝细胞癌的疗效与安全性。研究证实,联合方案显著延长患者的复合标准无进展生存期,疾病进展风险降低66%,且安全性可控。该研究为TACE联合靶向免疫治疗在不可切除肝细胞癌(尤其是伴大血管侵犯/高肿瘤负荷的高危人群)中的应用提供了高质量循证证据。

研究背景
肝细胞癌(HCC)是全球高发的消化道恶性肿瘤,对于不可切除的HCC,经动脉化疗栓塞(TACE)是中晚期患者的标准治疗方案,且在无肝外转移的晚期患者中也被广泛应用。但TACE单药治疗后肿瘤复发或进展难以避免,5年生存率仅26%-35%,亟需更有效的治疗策略。
TACE可诱导肿瘤坏死,释放肿瘤相关新抗原并激活抗肿瘤免疫,但同时会形成肿瘤缺氧微环境,促进血管新生并上调血管内皮生长因子(VEGF)表达。而程序性死亡受体1(PD-1)抑制剂可解除免疫抑制,血管内皮生长因子受体2(VEGFR2)抑制剂能正常化肿瘤血管、改善免疫微环境,二者联合TACE存在协同抗肿瘤的理论基础。
卡瑞利珠单抗(camrelizumab)是人源化抗PD-1单克隆抗体,阿帕替尼(rivoceranib)是靶向VEGFR2的酪氨酸激酶抑制剂(TKI),二者联合已在III期CARES-310研究中证实可改善晚期HCC患者总生存期(OS),并获中国及ESMO指南推荐。回顾性研究也显示该联合方案与TACE联用可行,且较单纯TACE显著延长OS,在此基础上,滕皋军院士团队开展了这项随机II期研究,进一步验证该三联方案的临床价值。
研究设计
CHANCE2005/CARES-005研究是中国22家中心开展的多中心、随机、开放标签II期临床试验(NCT04559607)。
入组标准:
经病理/影像学确诊的HCC
CNLC分期Ib-IIIa期(对应BCLC分期A-C期,但无肝外转移)
不可切除或拒绝手术
至少一个可测量病灶(RECICL 5标准)
Child-Pugh A级肝功能
ECOG PS 0-1分
关键排除标准:门静脉主干完全闭塞、既往接受过免疫治疗或肝动脉灌注化疗、6个月内显著出血史等。
分组:按1:1随机分配至TACE-C-R组(TACE+卡瑞利珠单抗+阿帕替尼)或TACE组,分层因素包括大血管侵犯、既往TKI治疗史、既往TACE次数。
治疗方案:
TACE组:采用含表柔比星(≤40 mg/次)的常规TACE,首次在随机后1周内进行,后续根据增强影像学提示的肿瘤残存情况按需行TACE。
TACE-C-R组:首次TACE后2周内开始静脉卡瑞利珠单抗200mg q3w+口服阿帕替尼250mg qd,直至进展、不可耐受毒性或研究者决定,仅阿帕替尼可因不良反应调整剂量,且允许疾病进展后从单纯TACE组交叉至联合组。
主要终点:复合标准定义的无进展生存期(PFS)(包括RECICL 5进展、TACE后1周内Child-Pugh C级恶化、或TACE失败/抵抗);
次要终点:改良实体瘤疗效评价标准(mRECIST)的PFS、TACE不可治性进展时间(TTUP)、OS、客观缓解率(ORR)、疾病控制率(DCR)、缓解持续时间(DOR)及安全性。
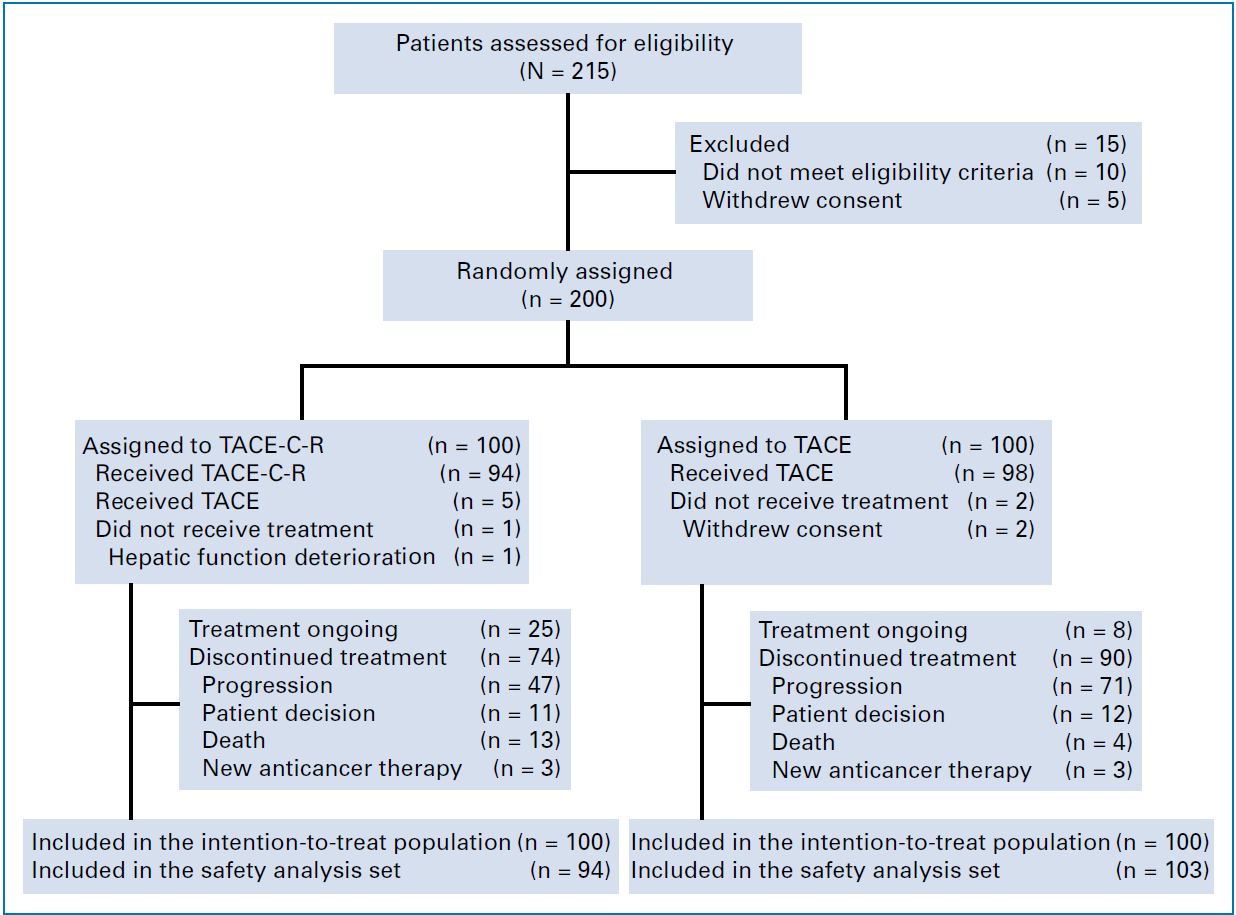
CONSORT图
研究结果
2020年12月28日-2023年10月29日,共纳入200例不可切除HCC患者(每组100例),其中89.5%肿瘤负荷≥7.0 cm,43%因血管侵犯(其中27%为Vp3-4型门静脉癌栓)属于晚期,入组人群更贴合临床中高危不可切除HCC的实际情况。截至2024年10月16日,中位随访14.3个月。
基线特征
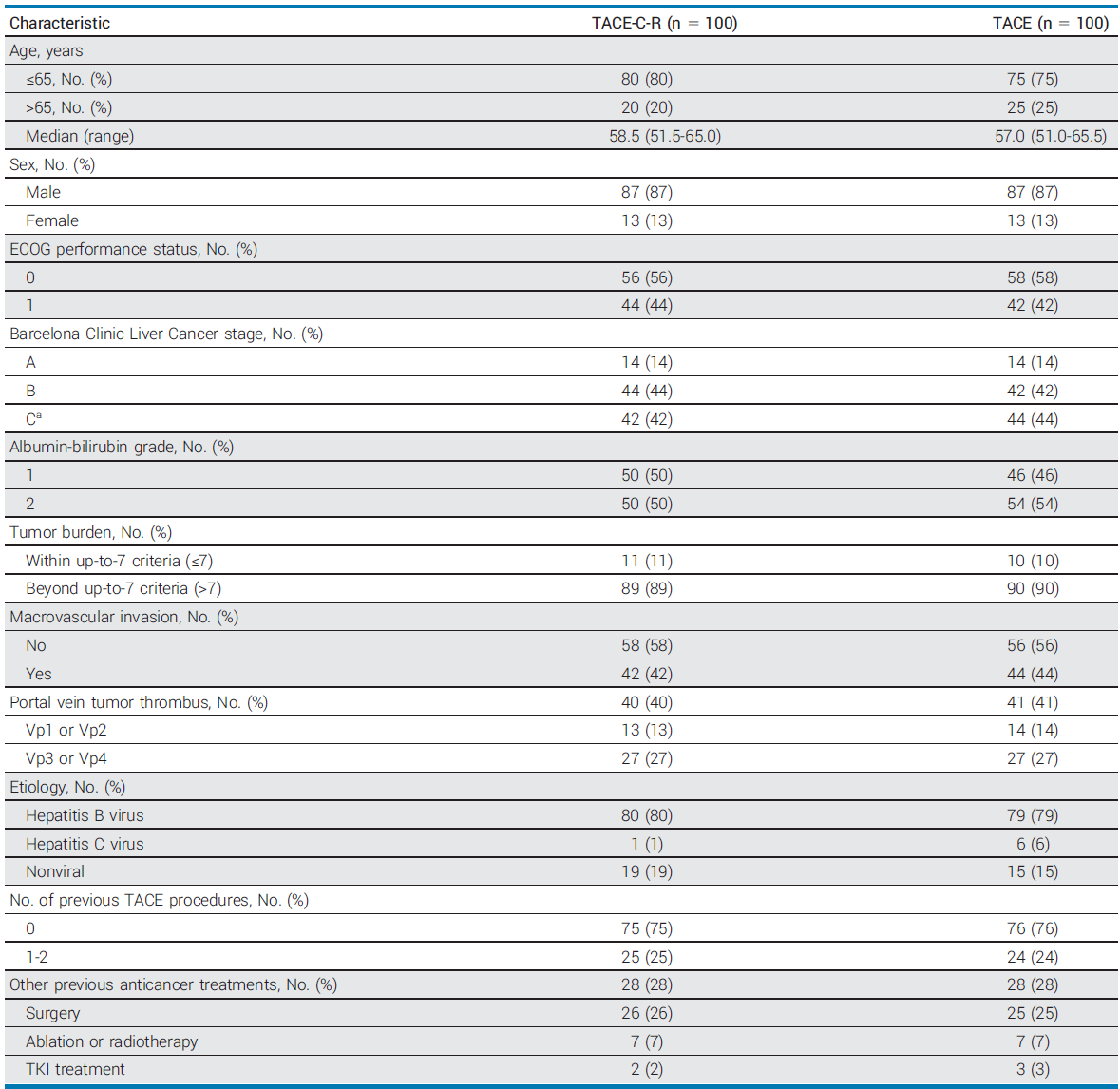
疗效结果
复合标准中位PFS:TACE-C-R组显著优于TACE组:10.8个月(95%CI 8.8-13.7) vs 3.2个月(95%CI 2.4-4.2),风险比(HR)0.34(95%CI 0.24-0.50,P<0.001)。
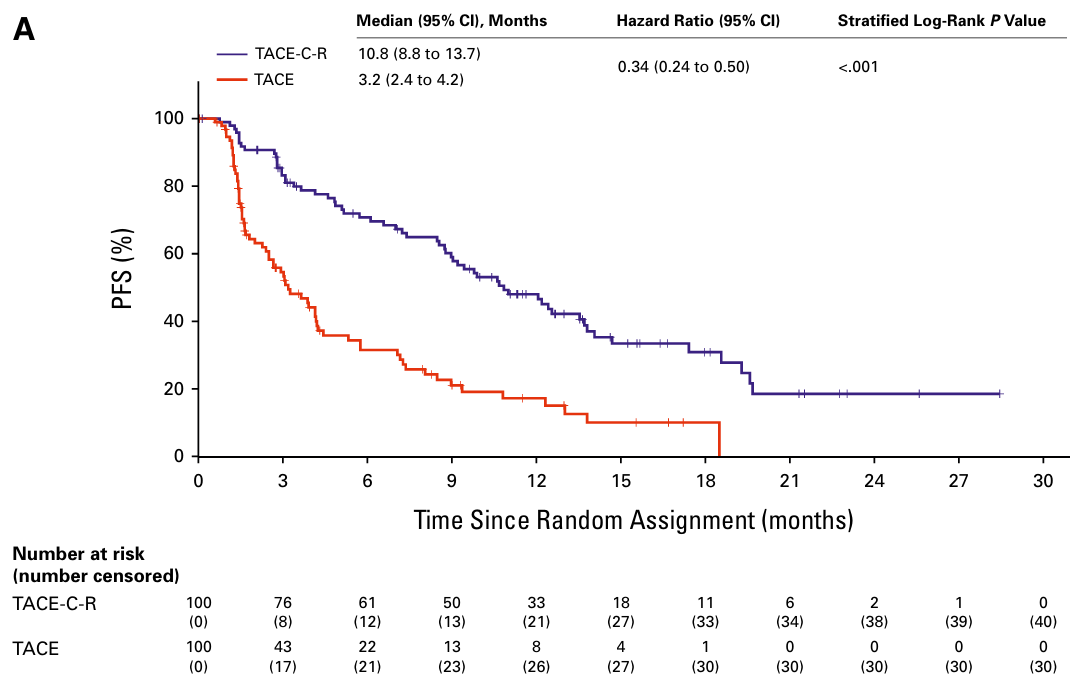
复合标准PFS
mRECIST标准中位PFS:TACE-C-R组同样优于TACE组8.8个月 vs 3.1个月(HR=0.43,95%CI 0.30-0.62,P<0.001)。
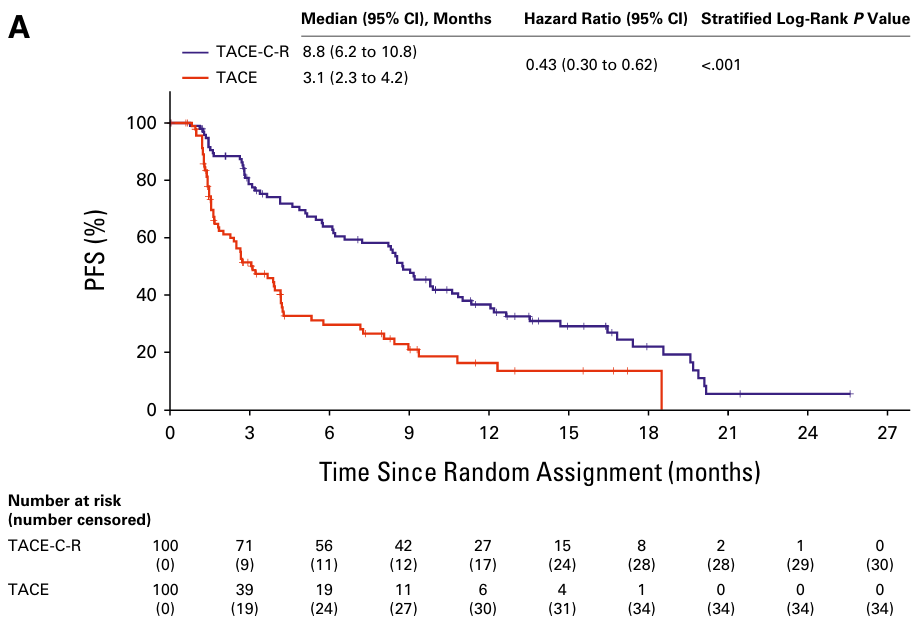
mRECIST标准PFS
各亚组PFS:事后亚组分析显示,无论BCLC分期、有无大血管侵犯、既往治疗史,各亚组均显示出TACE-C-R组的PFS获益趋势。特别值得注意的是,BCLC C期(无肝外转移)患者同样从三联疗法中显著获益。
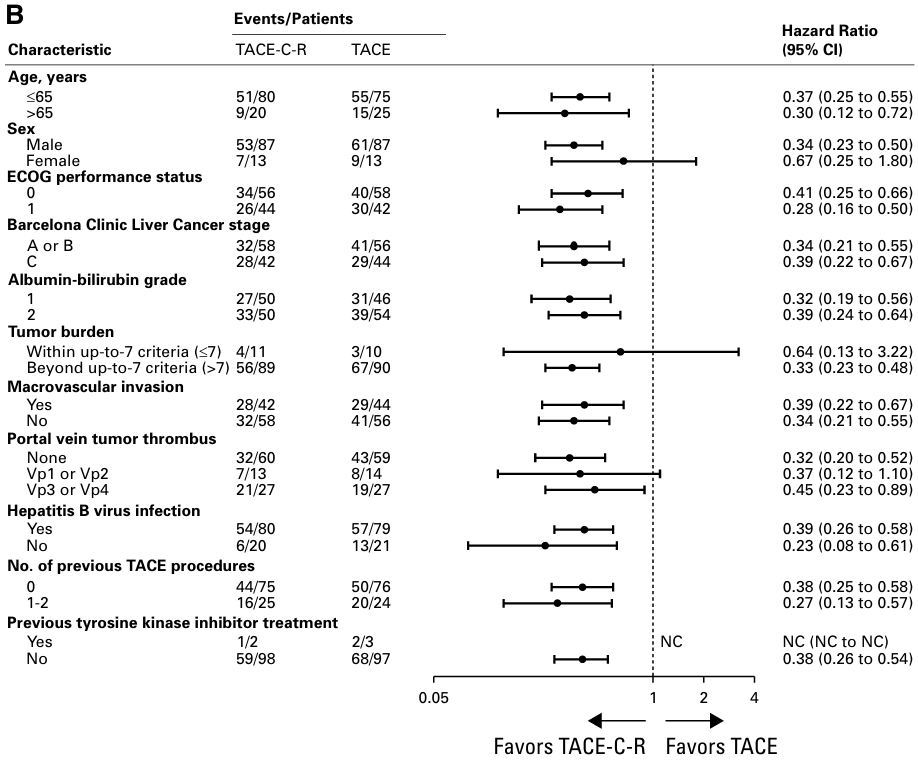
各亚组PFS分析
OS:数据尚不成熟,TACE-C-R组和TACE组的中位OS分别为24.0个月 vs 21.5个月(HR=0.87,95%CI 0.57-1.32,P=0.50),TACE组中有75%进展后交叉至TACE-C-R组,可能影响OS分析。
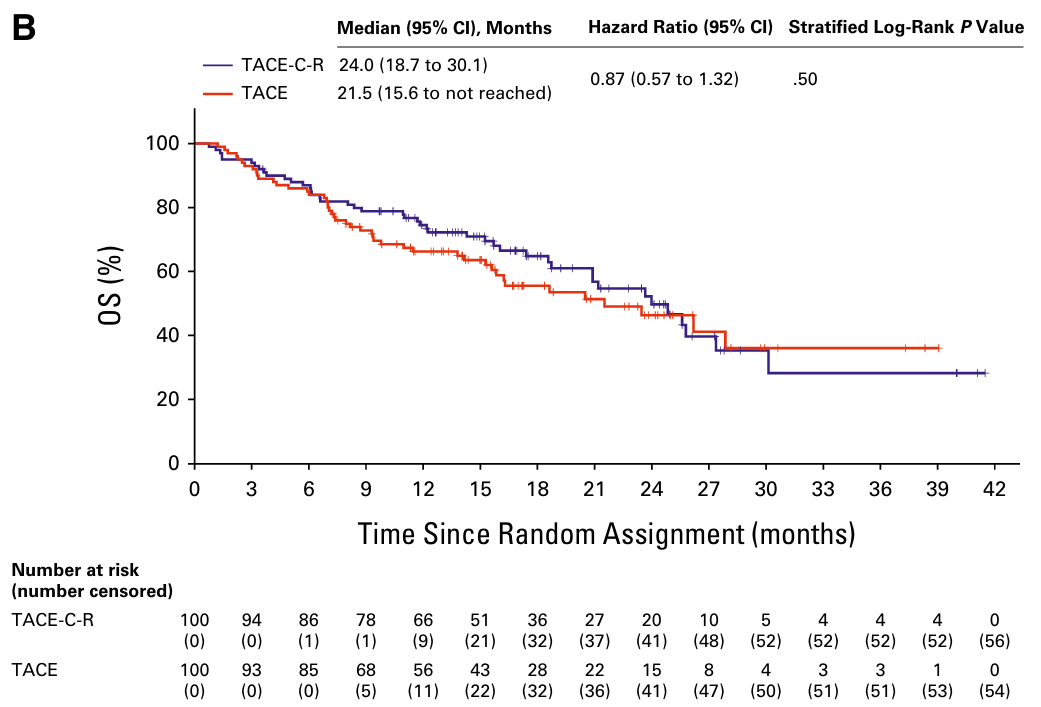
mRECIST标准OS
TTUP:TACE-C-R组的中位TTUP为13.7个月(95%CI 10.7-19.6),远高于TACE组的3.9 个月(95%CI 2.5-5.7),明显延迟患者进入 TACE不可治的时间。
肿瘤缓解方面,RECICL 5标准下,TACE-C-R组与的TACE组ORR分别为65% vs 29%、DCR分别为87% vs 63%、DOR分别为11.4个月 vs 6.9个月;mRECIST标准下,两组的ORR分别为61% vs 29%、DCR分别为85% vs 58%。
安全结果
安全性分析集纳入TACE-C-R组94例、TACE组103例患者。
治疗相关不良事件(TRAEs):
TACE-C-R组:任何级别99%,≥3级74%
TACE组:任何级别66%,≥3级22%
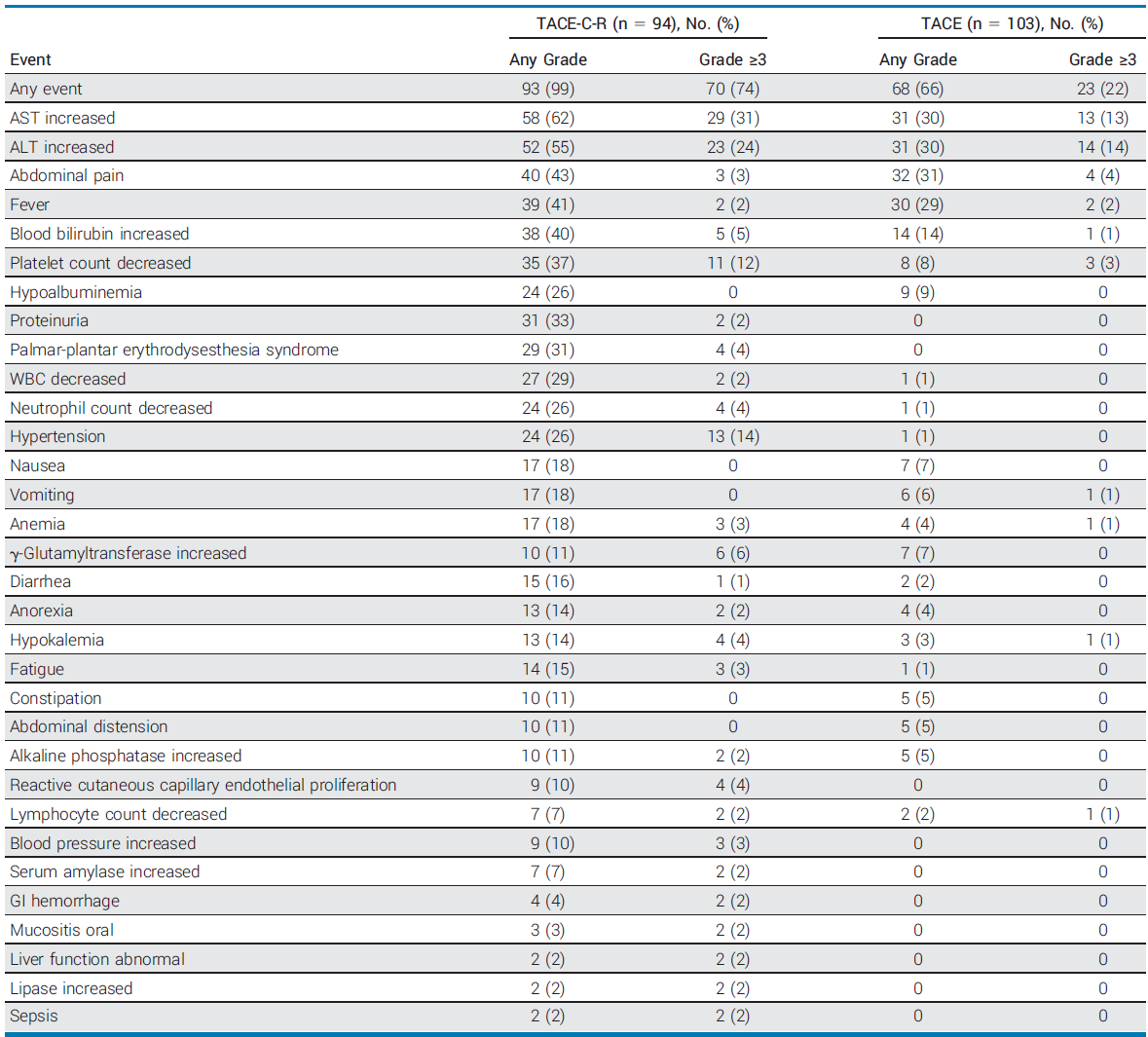
两组最常见的≥3级TRAEs均为天冬氨酸转氨酶(AST)升高和丙氨酸转氨酶(ALT)升高,TACE-C-R组发生率分别为31%和24%,TACE组为13%和14%。
特异性不良事件:TACE-C-R组免疫相关AE发生率为23%(≥3级12%,最常见为反应性皮肤毛细血管内皮增生[3%])。TACE-C-R组中VEGFR2抑制剂的典型不良反应,≥3级高血压、血小板计数降低发生率分别为14%和12%。
治疗相关不良事件
研究结论
CHANCE2005/CARES-005研究证实,在TACE基础上联合卡瑞利珠单抗和阿帕替尼可显著改善不可切除HCC患者的PFS,尤其在合并大血管侵犯和高肿瘤负荷的高危人群中表现出持续获益,且安全性可控。这项研究的重要意义在于TACE联合靶免治疗不仅使中期的HCC获益,也使晚期和高肿瘤负荷的肝癌获益,增补了联合治疗策略的重要证据。
随着EMERALD-1、LEAP-012、TALENTACE及本研究结果的相继公布,TACE联合ICIs及抗血管生成药物有望成为不可切除HCC的新型标准治疗模式。未来需进一步明确最佳的联合策略、患者筛选标志物,以及等待OS成熟数据以确认长期生存获益。
来源:肿瘤界