2026年2月19日,中山大学肿瘤防治中心徐瑞华院士、袁庶强教授、赵齐研究员团队在Cancer Cell发表题为"胃癌新辅助免疫化疗疗效异质性的多组学解析:遗传驱动与免疫微环境协同机制研究"的研究论文(点击文末阅读原文查看),通过对前期开展的NEOSUMMIT-01研究队列进行多组学检测和动态分析,揭示了胃癌新辅助免疫化疗的疗效预测标志物及耐药机制,建立精准分层模型指导临床治疗决策。

胃癌是全球第五大常见恶性肿瘤,也是癌症相关死亡的第四大原因。近年来,新辅助免疫化疗(nICT)在局部晚期胃癌治疗中取得突破性进展,显著提高了病理缓解率和手术切除率。然而,仍有接近一半的的患者无法从联合治疗中获益,耐药问题成为制约疗效的关键瓶颈。如何精准筛选获益人群、破解耐药机制,成为胃癌精准治疗领域亟待解决的科学问题。
肿瘤微环境(TME)的异质性是导致治疗反应差异的核心因素。既往研究多聚焦于单一组学数据、单臂设计或治疗前静态样本,缺乏对免疫化疗动态过程中基因组与免疫微环境协同演变的系统性解析。为此,研究团队依托NEOSUMMIT-01随机对照临床试验,创新性地设计了多组学转化研究,通过整合全外显子测序、转录组、蛋白质组及单细胞测序数据,绘制了胃癌免疫化疗响应的"动态全景图"。
核心发现1:找到预测疗效的多维生物标志物
研究团队创新建立交互选择模型,系统筛选出特异性预测nICT疗效的分子标志物体系。在基因组层面,突变特征SBS19富集与免疫抑制通路激活相关、提示不良预后,该发现在独立食管癌队列中得到验证;HLA分型方面,HLA-B*15:02阳性患者抗原呈递功能缺陷,表现为NK细胞活化、TCR信号及干扰素反应通路全面抑制,单细胞水平证实其肿瘤浸润CD8+T细胞细胞毒性显著减弱。在转录和蛋白组层面,FDXR高表达患者铁死亡调控活跃、免疫治疗生存获益明确,该标志物在其他三个独立胃癌免疫治疗队列中均显示预测价值;相反,FGFR通路激活则通过促进免疫抑制信号传导导致耐药,与患者不良预后相关。
上述标志物覆盖DNA修复、抗原呈递、细胞死亡及信号通路等多个生物学维度,既可独立指导发现治疗敏感人群,更可整合构建复合预测模型,为临床制定个体化治疗决策提供精准依据。
核心发现2:建立五种肿瘤微环境生态型,揭示疗效差异规律
研究团队基于单细胞测序数据,鉴定出五种肿瘤微环境生态型(EC1-EC5),系统阐明了不同免疫景观对nICT的治疗响应特征:
EC1(免疫激活生态型):以组织驻留记忆T细胞和细胞毒性T细胞浸润为特征,对nICT治疗响应最佳;
EC2(三级淋巴结构生态型):富含成熟B细胞及三级淋巴结构,nICT可诱导其显著扩增;
EC3(血管正常化生态型):以促血管生成髓系细胞为标志,nICT可抑制其免疫抑制功能;
EC4(细胞外基质生态型):基质成分富集,对nICT反应中等;
EC5(代谢抑制生态型):以TREM2+巨噬细胞富集和脂质代谢活跃为特征,对nICT耐药。
多色免疫组化验证显示,EC1型肿瘤富含CD8+效应T细胞和GZMB+细胞,而EC5型则以TREM2+巨噬细胞为主,形成"冷肿瘤"微环境。
核心发现3:APOA1+肿瘤细胞通过激活
TREM2+巨噬细胞驱动免疫抑制
研究深入解析了EC5型耐药的细胞互作机制,发现一群具有肠上皮样特征的APOA1+肿瘤细胞是介导免疫抑制的关键"推手"。机制研究表明,APOA1+肿瘤细胞通过分泌载脂蛋白APOA1/APOB,与TREM2+巨噬细胞表面的TREM2受体结合,激活PI3K-SYK信号通路,诱导巨噬细胞向免疫抑制表型分化。功能实验证实,APOA1刺激可显著上调巨噬细胞中STAT3、LGALS3、CD274(PD-L1)、TGFB1等免疫抑制分子的表达。小鼠试验进一步证实,Apoa1过表达的肿瘤细胞显著促进TREM2+巨噬细胞浸润,减少CD8+T细胞浸润,PD-1表达降低,导致免疫化疗耐药;而联合TREM2阻断可有效逆转这一耐药表型,恢复抗肿瘤免疫应答。进一步研究发现,转录因子NR5A2是调控APOA1表达的核心驱动因子,为干预策略提供了潜在靶点。
核心发现4:创建多组学分型模型(MOS)优化临床决策
基于基因组、转录组及微环境特征,研究团队构建了三种多组学亚型(MOS1-3),实现患者精准分层:
MOS1(免疫激活型,30%):PIK3CA突变富集、FDXR高表达、基线即存在细胞毒性免疫细胞浸润、高nICT响应率88%(vs 化疗29%)
MOS2(免疫可塑型,42%):TP53野生型、氧化磷酸化及药物代谢通路活跃、基线呈免疫荒漠表型,但nICT可诱导CD8+T细胞和NK细胞显著浸润
MOS3(免疫抑制型,28%):CN8拷贝数异常特征富集、APOA1高表达、FGFR通路激活、TREM2+巨噬细胞及成纤维细胞浸润、对nICT无显著获益
该模型在三个抗PD-1单药队列和两个单纯化疗队列中得到验证,显示出良好的预后预测价值和跨治疗场景的适用性。
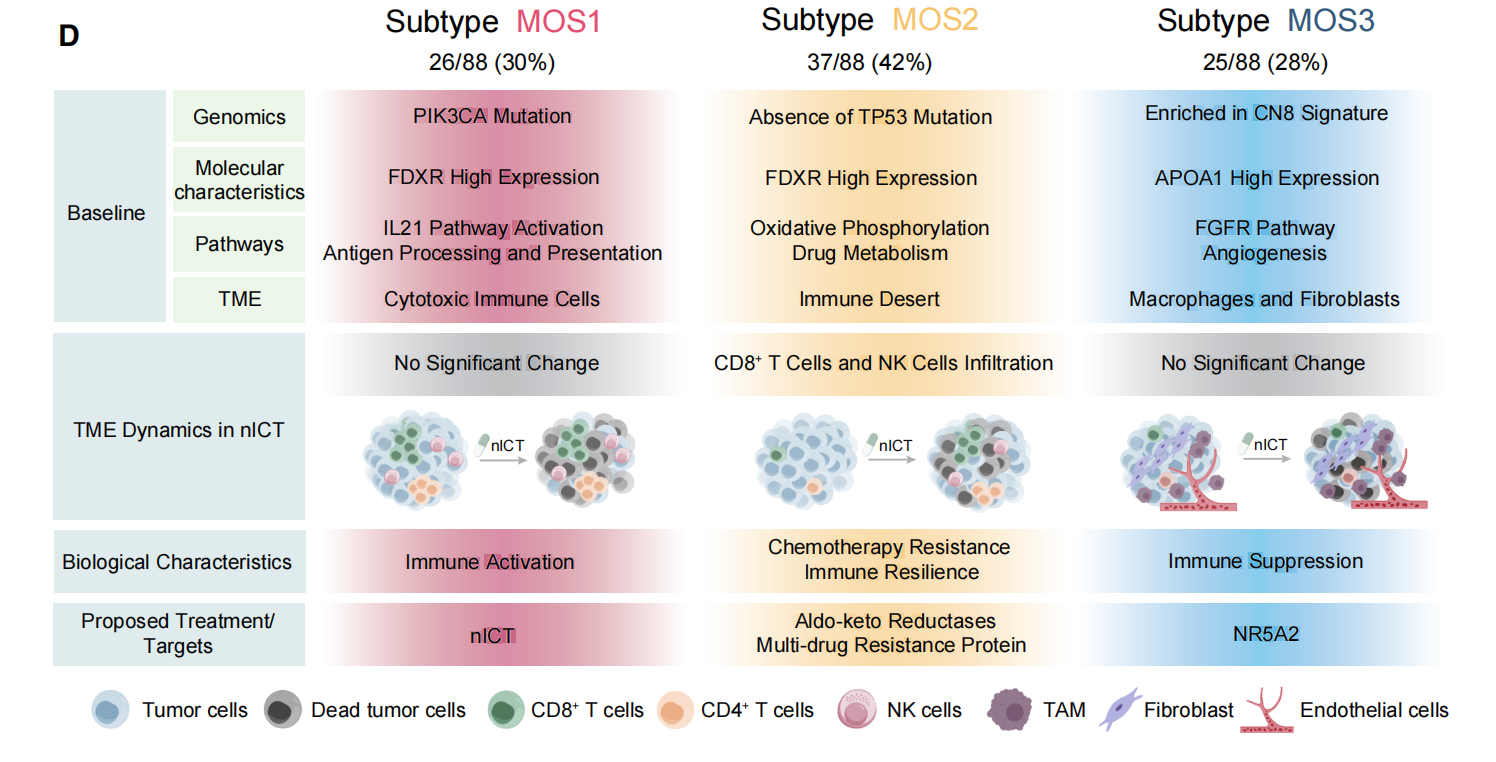
胃癌多组学治疗分型特征
综上,该研究依托前瞻性随机对照临床试验,系统鉴定了预测胃癌新辅助免疫化疗疗效的关键分子标志物,揭示APOA1⁺肿瘤细胞与TREM2⁺巨噬细胞互作介导耐药的免疫微环境重塑机制,并建立整合基因组特征与肿瘤免疫微环境的多组学分型(MOS)框架。研究全面描绘了影响胃癌免疫联合化疗反应的核心基因组变异与细胞图谱,为克服耐药及优化临床决策提供了新靶点和新策略。
中山大学肿瘤防治中心徐瑞华院士和袁庶强教授是本研究的共同通讯作者,赵齐研究员、黄润杰博士、王朝晔博士、胡佳佳博士、聂润聪副主任医师是本研究的共同第一作者。
研究者简介:

通讯作者 徐瑞华
中国工程院院士,中国医学科学院学术咨询委员会学部委员,中山大学肿瘤防治中心主任、医院院长、研究所所长,教授,博士生导师,华南恶性肿瘤防治全国重点实验室主任。中国临床肿瘤学会第四届理事长,中国抗癌协会副理事长,中国抗癌协会肿瘤内科学专业委员会主任委员,中国抗癌协会靶向治疗专委会首届主任委员,中国临床肿瘤学会第二届肠癌专委会主任委员,中国临床肿瘤学会胃癌专委会首届主任委员。以最后通讯作者在NEJM、JAMA(2)、BMJ、Cell、Nature Medicine(5)、Lancet Oncology(2)、Cancer Cell(5)、Annals of Oncology(2)等发表210余篇论文,其中IF>20分论文60余篇,成果被写入85部国内外指南共识,连续3年入选科睿唯安(Clarivate)全球高被引科学家,连续7年入选中国高被引学者榜单,H指数92。以第一完成人获得国家科技进步二等奖2项,中华医学科技奖、教育部科技奖及广东省科技奖等省部级一等奖共7项。获得第三届全国创新争先奖、何梁何利基金科学与技术奖、谈家桢临床医学奖、吴阶平医学创新奖以及CSCO年度成就奖。入选国家百千万人才工程、全国先进工作者、国务院特殊津贴专家、南粤百杰人才培养工程、国家卫生计生突出贡献中青年专家等人才项目。

通讯作者 袁庶强
中山大学肿瘤防治中心胃外科,医学博士、教授、主任医师、博士生导师、美国M.D. Anderson癌症中心访问学者。主攻胃肠肿瘤的外科及综合治疗,擅长机器人/腹腔镜微创及保胃功能手术,中国抗癌协会胃部肿瘤整合康复专委会常务委员,中国研究型医院学会腹膜后与盆底疾病专委会委员,广东省抗癌协会胃癌专委会副主任委员,广东省精准医学应用学会胃肠肿瘤分会副主任委员,第二届“广东实力中青年医生”,精术中国-手术视频演示大赛冠军,首届中国“达芬奇杯”机器人胃癌手术视频大赛季军,主持国自然基金、CSCO科研基金,作为第一或通讯作者在Nature Medicine、Cancer Cell、STTT、Molecular Cancer、Cancer Communications、Cell Rep Med等杂志发表论文50余篇,受邀美国ASCO年会口头报告。

第一作者 赵齐
中山大学肿瘤防治中心研究员,博士生导师,华南肿瘤学全国重点实验室肿瘤微生态研究平台负责人,广东省卫健委特支青年拔尖人才。围绕消化道肿瘤早筛、疗效和预后预测分子标志物发现难、验证难等问题,着重建立了一系列针对肿瘤组学数据特征鉴定、数据整合以及分子标志物筛选的生物信息学方法体系,先后建立中国人结直肠癌基因组大队列,绘制多个消化道肿瘤的基因组遗传图谱,发现POLE/POLD1、ecDNA扩增等多个具有临床转化价值的分子指标。 近些年以第一作者/通讯在包括Cancer Cell(3), JAMA oncology, Sci Trans Med, Cell Rep Med, Gut, Nature Communications(2)等杂志上发表SCI论文40余篇,总引用9000余次,入选2024、2025年全球前2%顶尖科学家榜单;主持包国家科技重大专项子课题、国自然面上、青年基金、广东省面上等多项基金项目。
来源:中山大学肿瘤防治中心订阅号