肿瘤免疫治疗通过激活机体免疫系统以实现对肿瘤的特异性清除,但其疗效在多种实体瘤中仍然受限,主要原因在于肿瘤免疫原性不足及免疫抑制性微环境的存在。诱导免疫原性癌细胞死亡(ICD)是增强抗肿瘤免疫的关键途径。越来越多的证据表明,内质网(ER)氧化应激能够驱动免疫原性反应。尽管钙网蛋白(CRT)暴露强调了内质网应激在ICD中的关键作用,但未折叠蛋白反应(UPR)的适应性反应抵消了内质网应激诱导的损伤,并减弱了免疫原性信号。因此,仅仅ER应激不足以产生持久有效的ICD反应,迫切需要将ER应激与互补的细胞死亡方式和免疫激活机制相结合。
近年来,铜死亡(cuproptosis)作为一种新型的线粒体依赖性细胞死亡方式受到关注,其通过破坏脂酰化蛋白稳态引发线粒体功能失衡,表现出显著的内在ICD效应。此外,线粒体相关内质网膜(MAMs)是连接内质网和线粒体的关键枢纽,协调钙流、氧化还原平衡和应激信号。内质网应激驱动的内源性Ca²⁺外流引起线粒体Ca²⁺超载,触发线粒体通透性转换孔开放,导致膜电位丧失,活性氧(ROS)生成增加,激活下游调节性死亡程序。同时,线粒体损伤导致的线粒体DNA释放可激活cGAS-STING通路,从而桥接细胞死亡与先天免疫反应。因此,利用内质网和线粒体之间复杂的相互作用来放大跨细胞器应激的传播,为增强ICD效应和激发持久的系统抗肿瘤免疫反应提供了一种有前途的策略。
基于上述背景,近日,西安交通大学第一附属医院锁爱莉教授、郑州大学附属肿瘤医院(河南省肿瘤医院)陈小兵教授团队在期刊Advanced Functional Materials上发表了题为 “Cage-Like Nanodrug Potentiates Tumor Immunotherapy by Orchestrating Endoplasmic Reticulum–Mitochondrial Crosstalk”的研究论文。

该研究构建了硼替佐米(BTZ)/伊利司莫(ES)负载的铜钙双金属(CuCa)纳米笼(CuCa-EB-H),用于协同级联放大内质网应激、线粒体损伤和cGAS-STING激活。在弱酸性的TME中,CuCa-EB-H纳米药物解离并释放大量的Ca²⁺、Cu- ES复合物和BTZ。在功能上,蛋白酶体抑制剂BTZ阻碍泛素化蛋白的降解,促进未折叠蛋白的积累,与外源Ca²⁺超载协同触发ER应激。内质网应激通过MAMs促进Ca²⁺外流并向线粒体传递,导致线粒体Ca²⁺超载和大量ROS产生。此外,Cu-ES复合物诱导的铜死亡加剧了线粒体功能障碍,从而导致过量的ROS积累和mtDNA释放。后者激活cGAS-STING通路产生I型干扰素,从而引发先天免疫反应。同时,cGAS-STING激活和ER应激参与循环级联放大,触发多种细胞死亡途径,表现出强大的ICD效应,从而增强DCs成熟并促进效应T细胞活化和分化。与传统的激活抗肿瘤免疫的单机制方法相比,这种级联放大过程将显著增强ICD效应。总之,本研究精心设计的CuCa-EB-H纳米药物利用细胞器间的串扰和循环级联放大来同步驱动强大的ICD并激活STING,从而唤醒先天和适应性免疫反应,为癌症提供了新的机制见解和治疗选择。
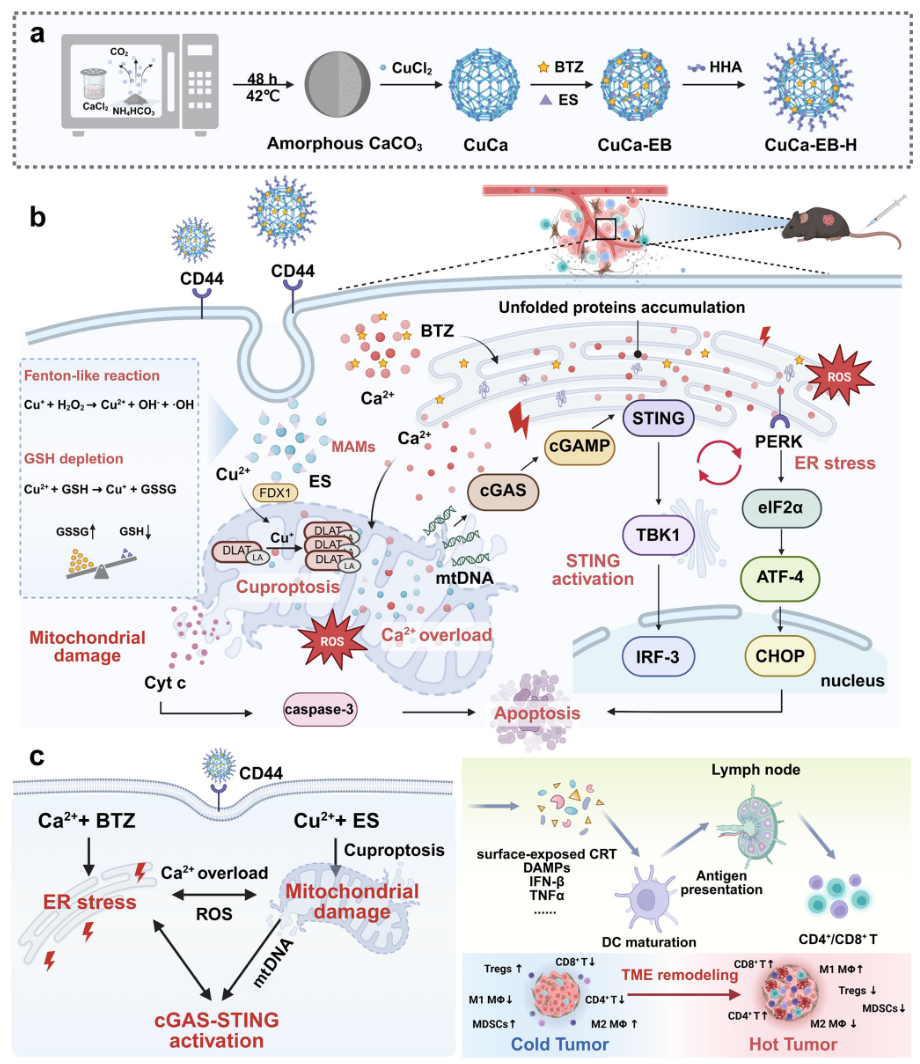
示意图:CuCa-EB-H纳米药物的制备和免疫治疗机制图
首先,通过Cu²⁺诱导无定形碳酸钙(ACC)纳米颗粒的原位转化合成了新颖的CuCa纳米笼。随后,ES和BTZ通过配位作用和静电作用被包裹到纳米笼中,形成CuCa-EB纳米颗粒。为了提高CuCa-EB纳米粒子的稳定性和肿瘤靶向性,用酰肼化的透明质酸(HHA)对其进行表面包覆,得到笼状CuCa-EB-H纳米药物。该纳米药物具有优异的生理稳定性和pH响应性,有利于纳米药物在肿瘤部位的靶向递送。此外,CuCa-EB-H纳米药物还具备类芬顿催化活性与GSH消耗能力,为其抗癌功效提供了坚实的基础。
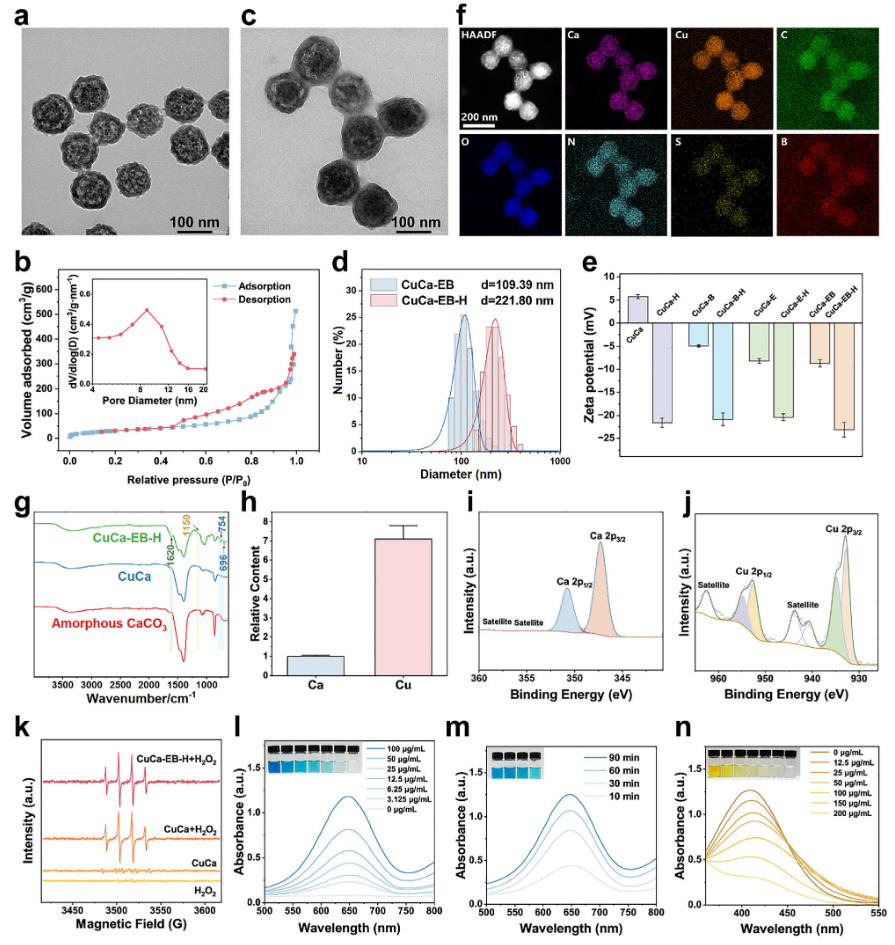
图1 CuCa-EB-H纳米药物的表征
体外研究表明,CuCa-EB-H纳米药物能够有效被Hepa1-6细胞摄取,并具有优异的肿瘤细胞杀伤效果。CuCa-EB-H纳米药物处理后,内质网应激相关信号通路显著激活,伴随PERK-eIF2α-ATF4-CHOP轴的增强。同时,内质网钙稳态被明显破坏,Ca²⁺由内质网向胞质释放。通过有效诱导ER应激和破坏Ca²⁺稳态来触发副凋亡(图2)。
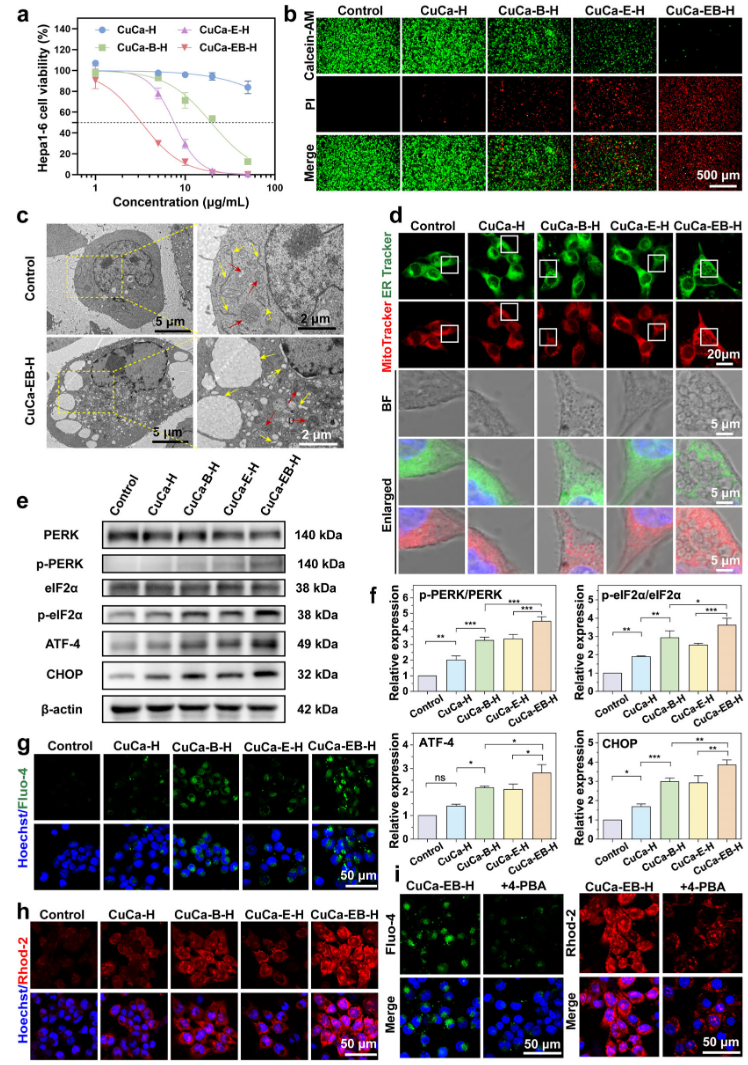
图2 CuCa-EB-H纳米药物的体外抗癌作用及内质网应激诱导能力
同时,ES选择性地将Cu²⁺运送到线粒体中,有效地提高细胞内的铜水平并激活铜死亡,包括DLAT脂酰化蛋白聚集、FDX1表达下降以及线粒体膜电位和ATP水平的显著降低。CuCa-EB-H纳米药物通过线粒体靶向的Cu-ES复合物触发的铜死亡与BTZ和外源Ca²⁺诱导的内质网应激、Ca²⁺稳态失调的协同作用显著破坏线粒体功能。此外,CuCa-EB-H纳米药物还能有效促进细胞凋亡,同时激活多种死亡途径协同杀伤肿瘤细胞(图3)。
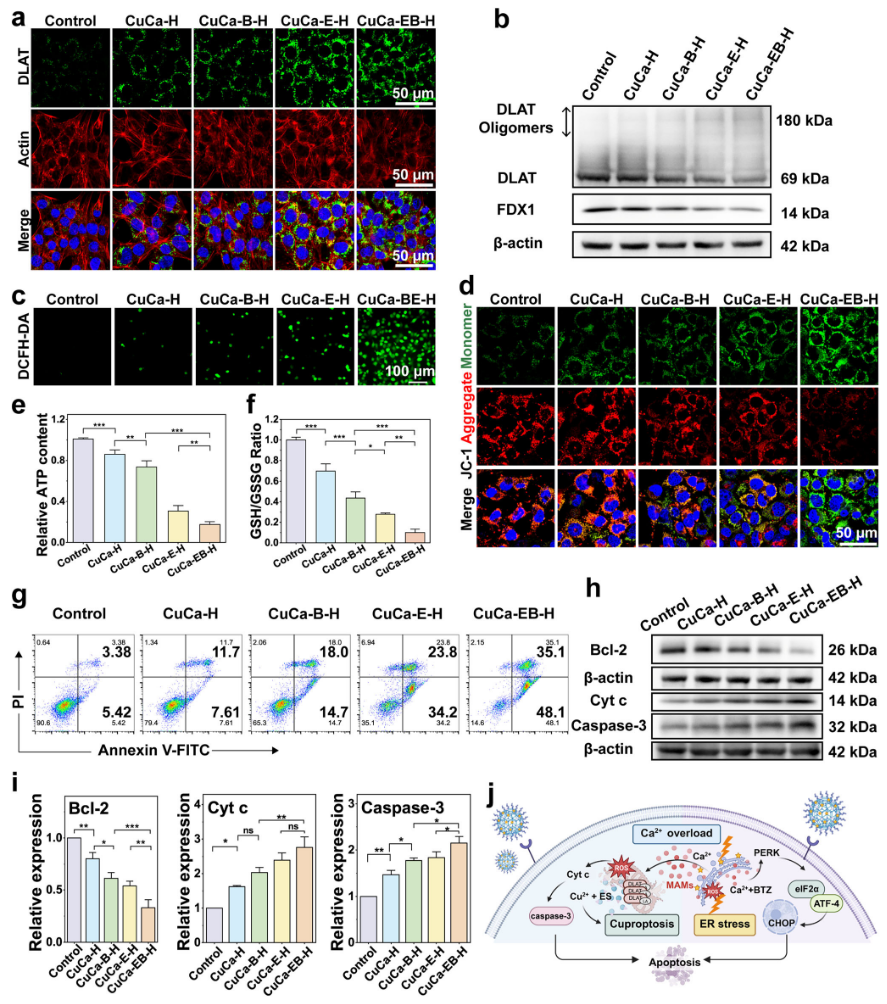
图3 CuCa-EB-H诱导的铜死亡与细胞凋亡
线粒体结构完整性受损后,大量mtDNA释放至胞质,显著激活cGAS-STING信号通路,下游TBK1与IRF3磷酸化水平升高,并伴随IFN-β、CXCL-10等炎症因子分泌增多。此外,验证了不同细胞器之间的功能串扰关系,结果显示,内质网应激促进线粒体损伤,而STING通路的激活反过来进一步加重内质网应激水平,形成稳定的正反馈调控回路,有助于维持免疫相关信号的持续激活(图4)。
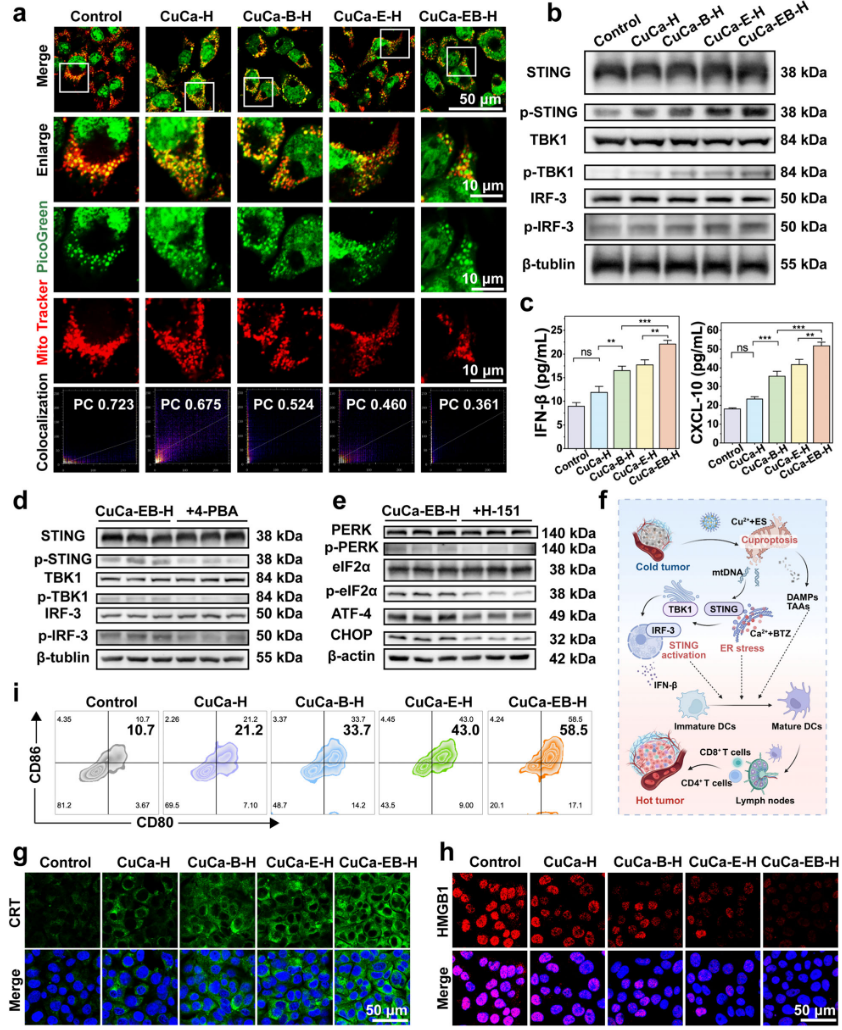
图4 cGAS-STING激活、ICD诱导和DCs成熟
RNA转录组测序分析表明CuCa-EB-H纳米药物不仅通过抑制致癌信号级联和诱导细胞凋亡发挥治疗作用,而且能够触发强烈的抗肿瘤免疫激活效果(图5)。
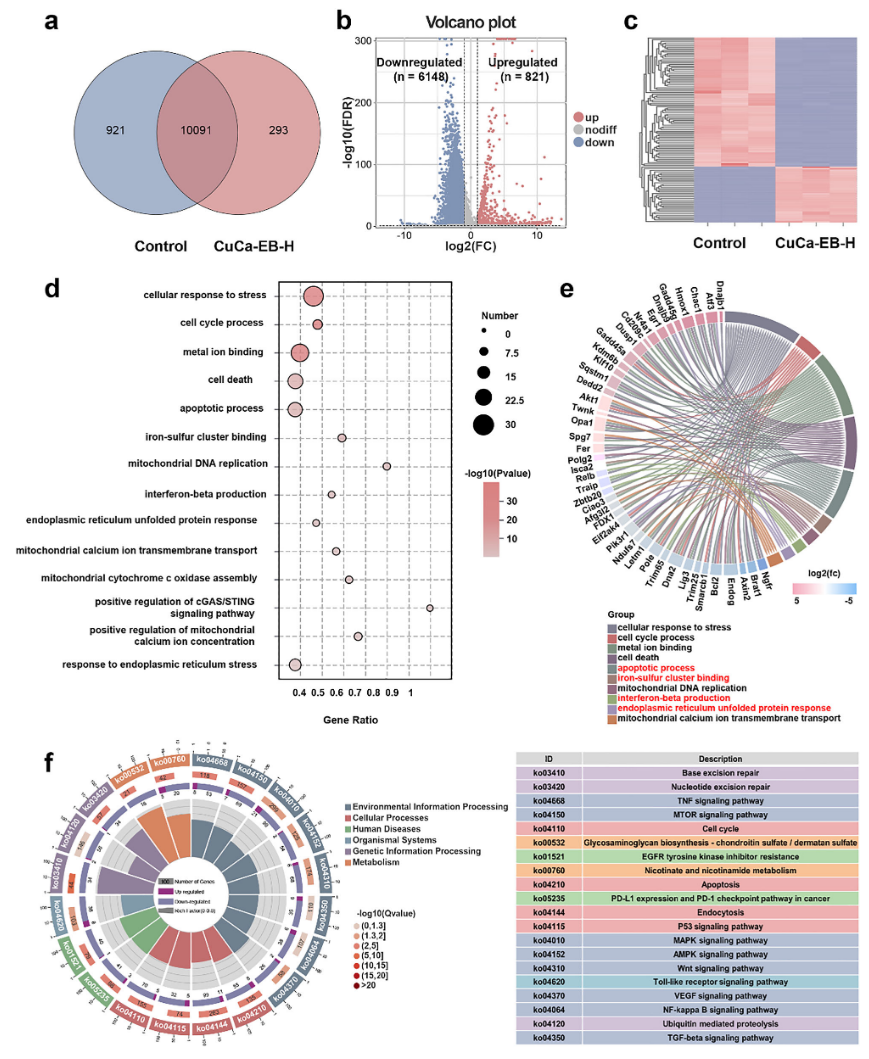
图5 CuCa-EB-H纳米药物处理Hepa1-6细胞的转录组分析
体内研究表明,在单发肿瘤模型中,CuCa-EB-H纳米药物治疗后肿瘤生长受到有效抑制,且未观察到明显系统毒性。免疫评估发现,CuCa-EB-H纳米药物治疗后肿瘤组织中树突状细胞成熟水平明显升高,CD8⁺ T细胞、M1型巨噬细胞浸润显著增加,而免疫抑制相关细胞群体比例下降。在双边肿瘤模型中,CuCa-EB-H纳米药物和α PD-1联合免疫治疗不仅抑制了原发和远处肿瘤的生长,延长了双侧荷瘤小鼠的生存期,而且增强了体内免疫激活效果。
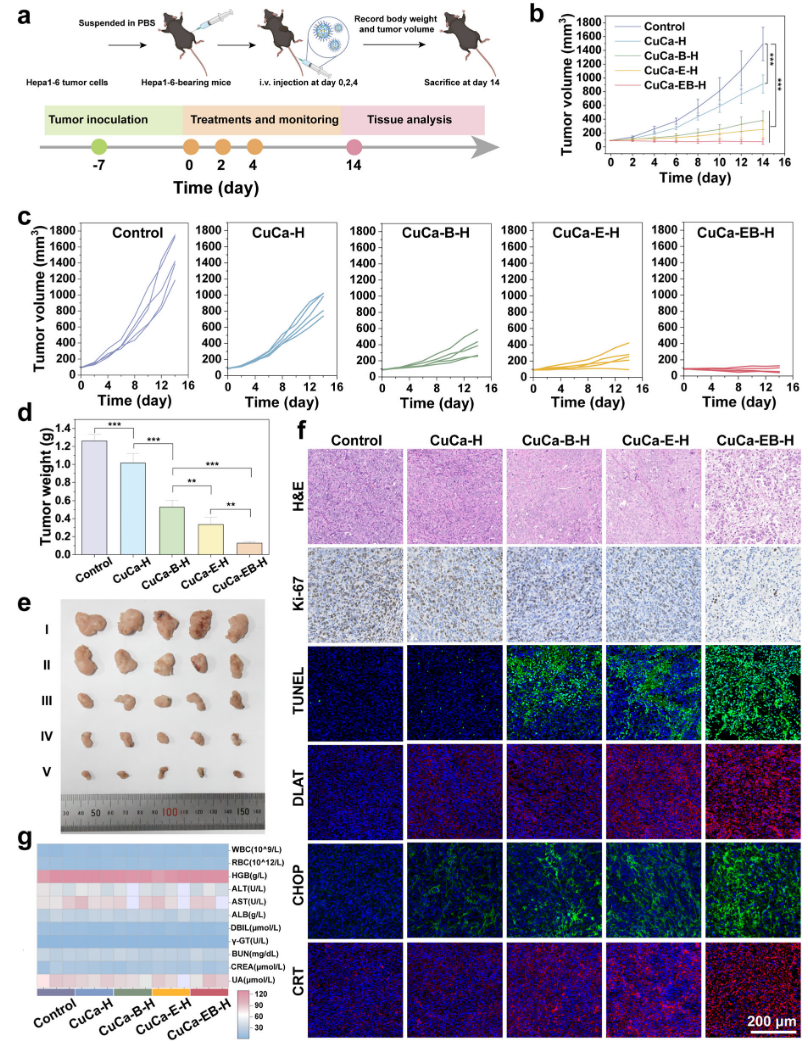
图6 CuCa-EB-H纳米药物体内抗肿瘤效率评估
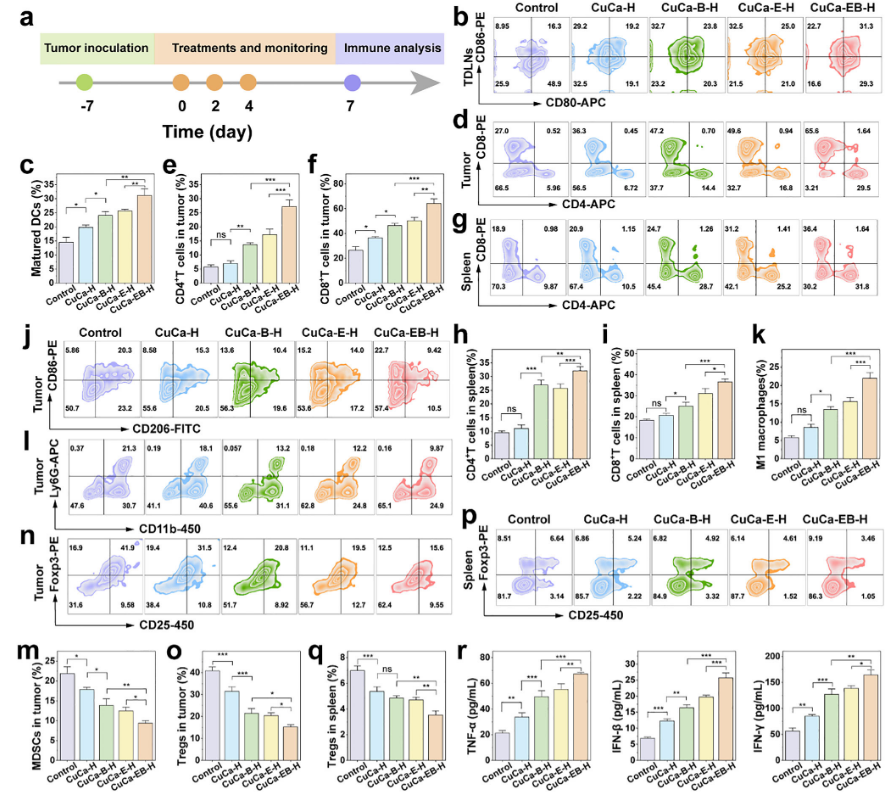
图7 CuCa - EB - H介导的免疫支持型TME的重塑
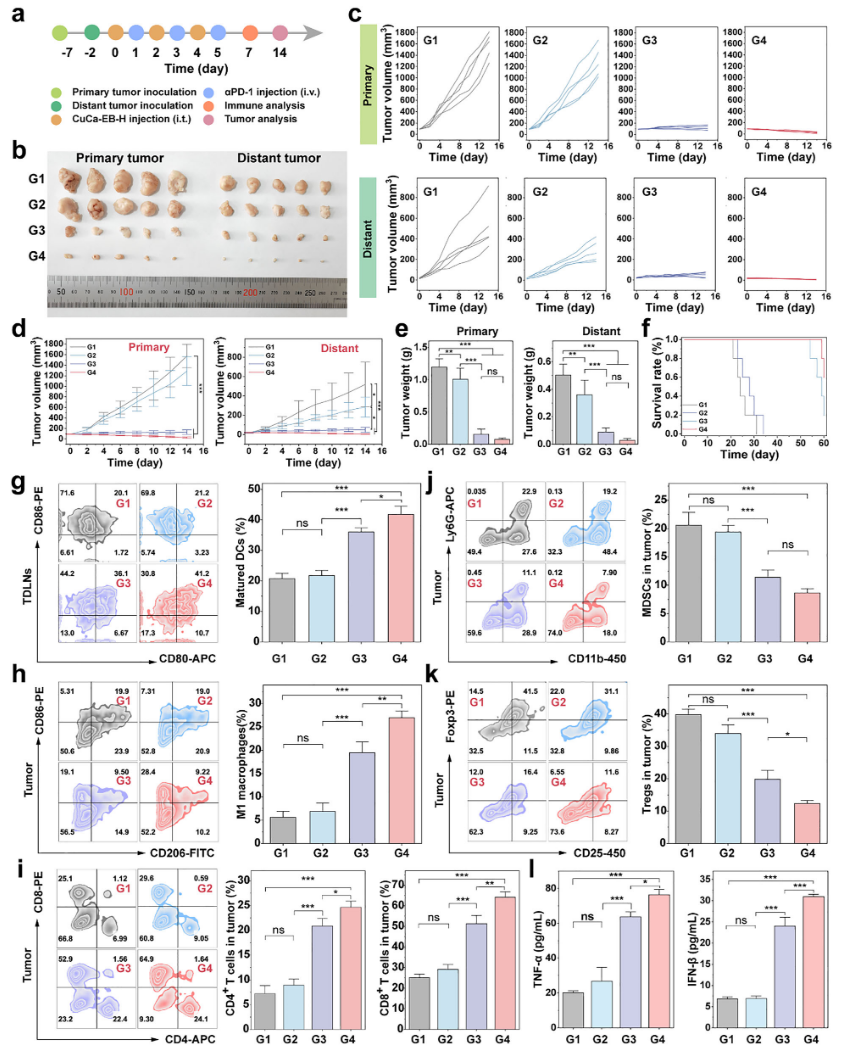
图 8 CuCa-EB-H纳米药物联合αPD-1在双侧肿瘤模型中的抗肿瘤免疫反应
总之,本研究成功开发了一种创新的装载BTZ/ES的纳米笼状铜/钙离子干扰剂(CuCa-EB-H),靶向干扰癌细胞中的细胞器网络和离子稳态,从而诱导多种细胞死亡途径,并激活先天和适应性抗肿瘤免疫,为离子干扰免疫治疗提供了机制见解,并为加强免疫检查点治疗提供了有希望的策略。
西安交通大学第一附属医院博士研究生肖莫凡为论文第一作者,西安交通大学第一附属医院锁爱莉教授、河南省肿瘤医院陈小兵教授、西安交通大学材料科学与工程学院钱军民教授为共同通讯作者。
本研究受到国家自然科学基金、陕西省重点研发计划和河南省科技研究与发展计划联合基金等项目资助。
原文链接:
http://doi.org/10.1002/adfm.202527957
专家介绍

锁爱莉 教授
主任医师,教授,博士生导师
西安交通大学第一附属医院 肿瘤内科副主任
美国Emory大学访问学者
中国抗癌协会食管肿瘤整合康复专委会常委
中国抗癌协会肿瘤胃病学专委会常委
中国抗癌协会整合肿瘤肾脏病专委会委员
北京癌症防治学会肝胆胰临床研究专业委员会副主任委员
陕西省抗癌协会老年肿瘤外科专委会副主任委员
陕西省抗癌协会安宁疗护专委会副主任委员
JCO胆道系统肿瘤中文版编委
主持国科金面上项目2项,一作/通讯作者SCI论
文20余篇,IF>10的10余篇,授权国家发明专利3项

陈小兵 教授
医学肿瘤学博士,郑州大学与河南科技大学博士研究生导师、博士后合作导师,郑州大学与河南中医药大学硕士研究生导师,河南省肿瘤医院(中国医学科学院肿瘤医院河南医院)肿瘤内科二级教授/主任医师
中国抗癌协会第九届理事会常务理事,河南省科学技术协会第十届常务委员会委员,河南省药学会常务理事,中国抗癌协会食管肿瘤整合康复专业委员会主任委员、整合食管癌委员会副主任委员,中国抗癌协会科普宣传部副部长、科普委员会副主任、康复委员会副主任。国务院政府特殊津贴专家,国家健康科普专家,全国科普工作先进工作者,中国科学技术协会“2017年十大科学传播人物”,教育部博硕士研究生学位论文与优秀论文评审专家,国家自然基金委网评专家。河南省优秀专家,河南省学术技术带头人,中原英才-中原科技创新领军人才,河南最美科技工作者,河南省“十大健康传播人物”,河南省医师协会医学科普医师分会会长。首批科技创新2030“癌症、心脑血管、呼吸和代谢性疾病防治研究”重大专项“上消化道癌风险分层新方法及序贯筛查新策略的建立和应用”课题组骨干成员之一。
从事肿瘤防治研究与临床工作27年,培养硕士研究生及博士研究生22名,指导博士后6名,主持国家自然科学基金面上项目3项,主持中原科技创新领军人才项目(2019)、河南省杰青(2014)、河南省自然重点(2022)、河南省医学科技重大项目(2023)等科研项目20余项,获河南省科技进步二等奖6项、河南省医学科技进步奖和教育科技进步奖一等奖9项;发表SCI论文130余篇,其中以第一/通讯作者在Signal Transduction and Targeted Therapy、Molecular Cancer、Oncogene、Journal of Clinical Investigation、Journal of Medicinal Chemistry、Advanced Science等国际高水平期刊上发表SCI论文85篇,总影响因子超过540,累计被引2600余次,ESI高被引论文2篇,H指数32。担任国家“十四五”重点图书《整合肿瘤学》临床卷《腹部盆腔肿瘤分册》主编,担任科普中国肿瘤防控科普丛书《全面说食管癌》主编、中国抗癌协会CACA指南《肾脏保护》主编、中国抗癌协会编著《2022-2023恶性肿瘤学科发展报告》主编、《肿瘤整体评估》《食管肿瘤整合康复患者指南2024版》主编、《中国肿瘤防治核心科普知识》执行主编、《癌前病变》《食管癌》(2025版)《中国抗癌协会癌症筛查科普指南》《中国肿瘤防治之要》副主编等。担任主编的《面对癌症:不恐慌不盲从》图书获科技部2020全国优秀科普作品奖、2023年中国抗癌协会科技奖科普奖。
来源:肿瘤界