2025年11月28日,中山大学肿瘤防治中心陈敏山、张耀军、王骏成团队联合中山大学附属第一医院沈顺利团队、湖南省人民医院王小辉团队在国际肝癌领域权威期刊《Liver Cancer》在线发表题为“Pathological complete response after systemic therapy and curative resection in initially unresectable hepatocellular carcinoma: feasibility of a Tumor-Free with Drug-Free strategy”的研究成果。该研究聚焦初始不可切除肝细胞癌(uHCC)患者经系统治疗转化并手术切除达到病理完全缓解(pCR)后是否需要术后辅助治疗的核心争议,首次以大样本真实世界数据证实“无瘤亦无药(Tumor-Free with Drug-Free)”策略的安全性与可行性,为肝癌精准治疗提供全新循证依据。

转化治疗推动部分不可切除肝癌迈向“可治”
随着以免疫检查点抑制剂(ICIs)为基础的系统治疗方案不断发展,越来越多原本不可切除的肝细胞癌患者有机会通过转化治疗实现根治性手术。本研究汇总2020-2023年三家三甲医院2212例uHCC转化手术患者数据,其中1,623例接受了系统治疗相关方案。最终共有257例(15.8%)在术后达到pCR,成为本研究重点分析的人群,充分体现了系统治疗在深度缓解方面的潜力。值得关注的是,这一人群在初诊时多为疾病负荷较高的中晚期患者:中位肿瘤直径9.0 cm,约四成存在多发病灶,超过一半合并大血管侵犯(55.6%),七成患者术前AFP升高(70.4%)。在如此高危的基线特征下,患者仍能达到病理完全缓解(pCR)并进入术后长期随访阶段,为探索更优化的后续治疗策略提供了宝贵窗口。
长期随访数据亮眼:pCR患者5年生存率达85.5%
经中位32.7个月随访,pCR患者展现出持久稳定的优异预后:1年、3年、5年无复发生存率(RFS)分别为81.7%、60.3%、58.3%;1年、3年、5年总体生存率(OS)更是高达98.0%、91.1%、85.5%。这一数据表明,“系统治疗深度缓解+根治性切除”可将部分晚期患者带入接近“功能治愈”的阶段,其预后显著优于传统同分期肝癌人群。
核心争议破解:辅助治疗无获益,反增毒性负担
针对“pCR患者术后是否需继续辅助治疗”这一临床痛点,研究给出明确答案:257例患者中,88例(34.2%)经多学科团队(MDT)评估后接受中位6.05个月辅助治疗,其余169例仅进行主动监测。结果显示,无论原始队列还是1:2倾向评分匹配(PSM)后队列,辅助治疗组与主动监测组的生存结局均无统计学差异。亚组分析进一步证实,无任何特定人群能从辅助治疗中明确获益。更关键的是,辅助治疗显著增加毒性风险:任何级别不良反应发生率85.2% vs 66.3%,3-4级不良反应8.0% vs 3.0%,常见毒性包括肝功能异常、皮肤反应、血液学异常及胃肠道症状。综合生存获益与毒性负担来看,在已经实现pCR的前提下,继续辅助治疗既未改善生存,又加重患者治疗负担与经济成本。
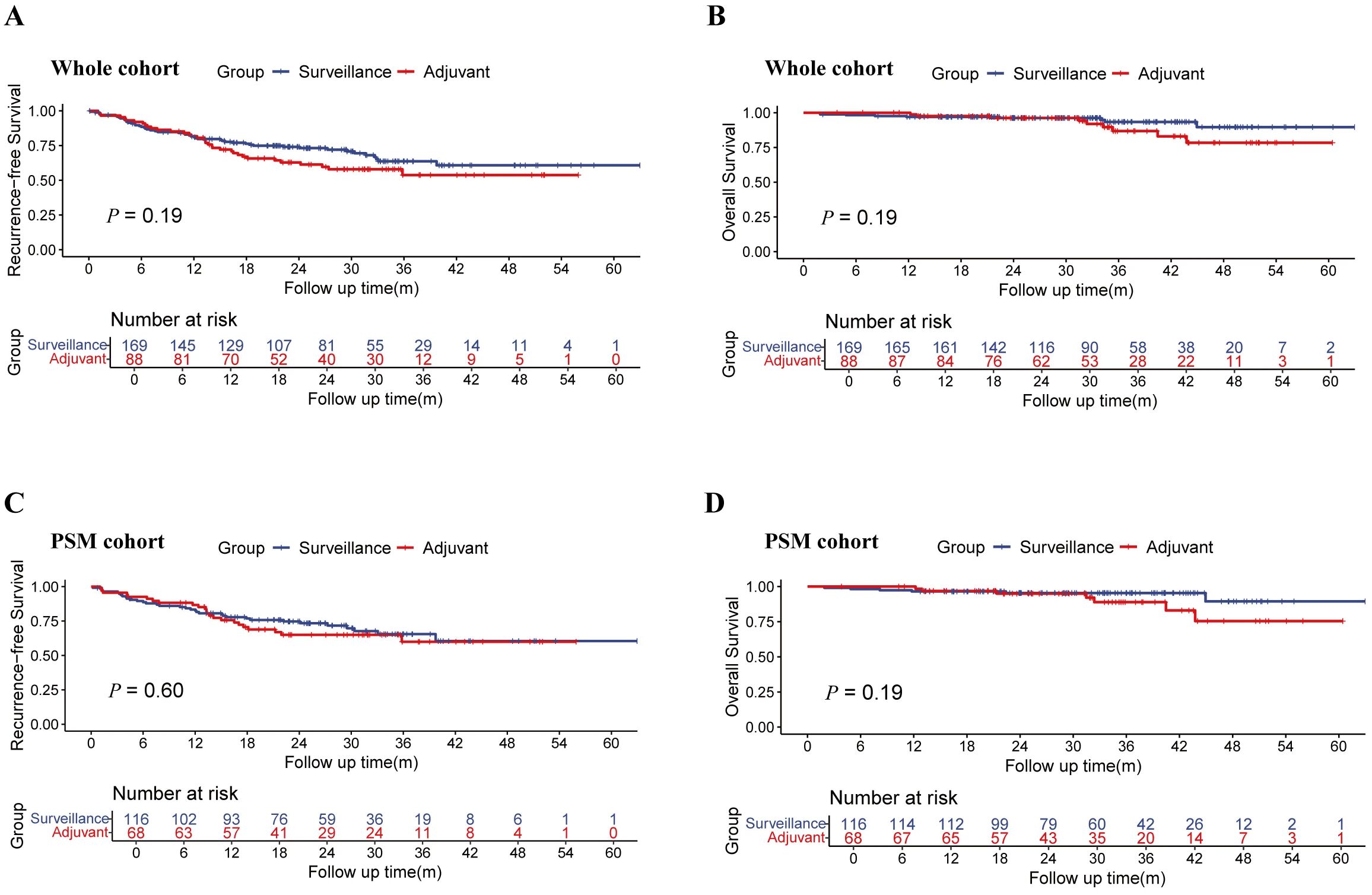
图1. 转化治疗后达到pCR患者,后续接受辅助治疗和主动监测的疗效比较
术后AFP:回答“是否真正无瘤”的关键线索
尽管pCR在病理学上定义为切除标本中无存活肿瘤细胞,但取材范围有限及肝内外潜在微小残留灶(MRD)仍是无法回避的问题:pCR是否等同于真正“无瘤”?本研究发现,术后AFP水平为判断隐匿残留风险提供了关键信息:多因素分析中,术后一月AFP阳性是唯一独立预测复发与死亡的危险因素;AFP阳性患者中位无复发生存仅为15.5个月,而AFP阴性患者随访期内中位RFS尚未达到;总生存方面,AFP阳性人群同样表现出明显不良趋势。
与之形成鲜明对比的是,无论是术前影像学完全缓解(rCR)还是临床完全缓解(cCR)均无法可靠预判术后长期预后(P>0.1)。这一发现提示,单纯影像学“无可见病灶”不足以反映体内MRD风险,而术后AFP正常化才是pCR患者“功能无瘤”的核心生物学标志。
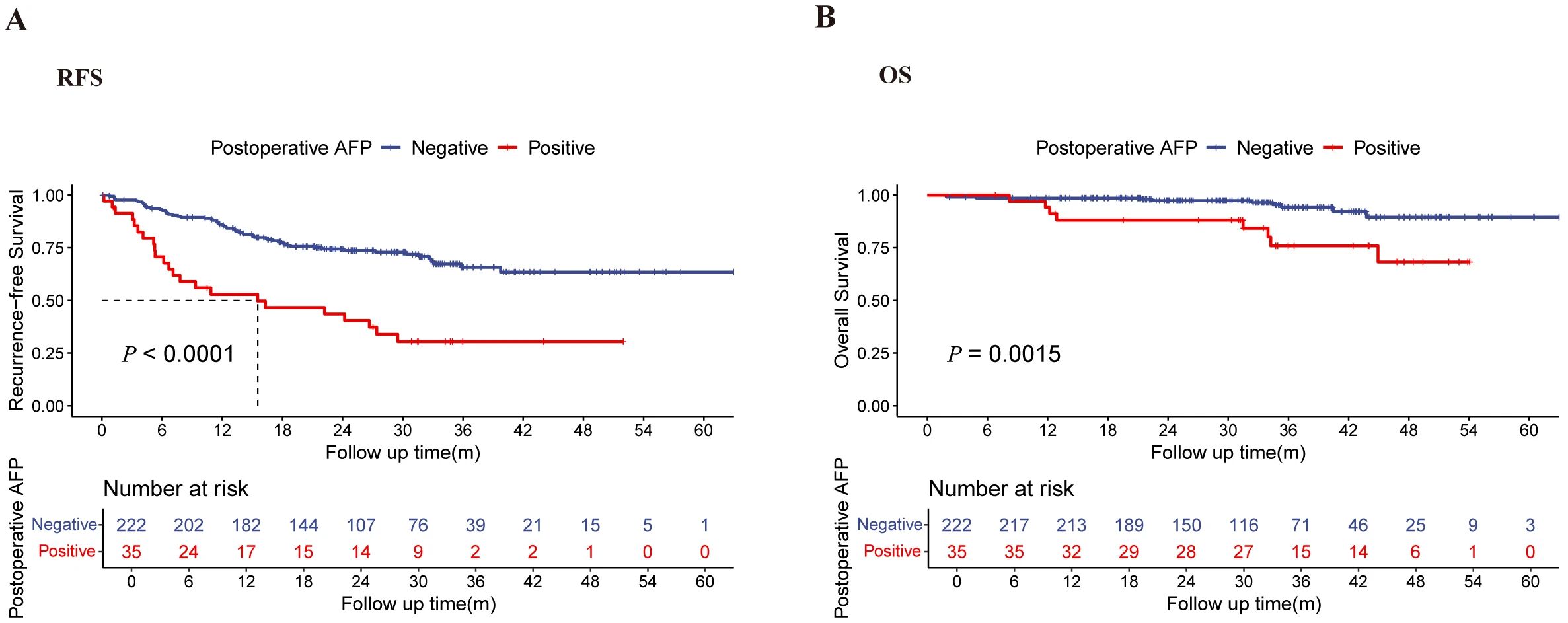
图2. 转化治疗后达到pCR患者,术后1月AFP阳性与阴性人群的疗效比较
“无瘤亦无药” 策略落地:精准分层的个体化管理
基于上述证据,研究团队明确提出术后管理方案:对于术后达到pCR且 AFP恢复正常的患者,在规范影像监测与肿瘤标志物随访基础上,可停止系统性辅助治疗,即“无瘤亦无药”策略,兼顾生存获益与生活质量;对于术后AFP阳性的高危人群,需警惕MRD存在,未来可探索更强化的个体化治疗方案(如延长或调整系统治疗)以及更密切的随访策略,并引入ctDNA等新型生物标志物以进一步优化风险分层。
结语:为转化治疗时代的“真正终点”给出实证
在系统治疗迅速发展的转化治疗时代,如何科学界定“治疗终点”是肝癌领域的重要命题。本研究基于大样本、多中心真实世界数据,首次系统回答了“转化手术后达到pCR的患者是否还需要继续用药”这一关键临床问题,证明在AFP正常化这一生物学标志前提下,“无瘤亦无药”并非理想化口号,而是可以在临床实践中落地的可行策略。
未来,随着AFP、ctDNA等多维指标的联合应用以及前瞻性研究的推进,有望进一步细化停药标准与随访路径,推动肝癌治疗从“延长生存”走向“减少毒性、兼顾生存与生活质量”的新阶段。
中山大学肿瘤防治中心陈敏山教授,中山大学附属第一医院沈顺利主任医师,中山大学肿瘤防治中心张耀军主任医师,以及中山大学肿瘤防治中心王骏成副主任医师为本研究的共同通讯作者。中山大学肿瘤防治中心林庆扬博士研究生、彭威博士研究生,中山大学附属第一医院于玺博士研究生,中山大学肿瘤防治中心谢帆博士研究生,以及湖南省人民医院王小辉主治医师为本研究的共同第一作者。
专家介绍

陈敏山 教授
中山大学肿瘤防治中心肝脏外科主任导师、二级教授
中山大学肝癌研究所所长
中山大学肿瘤防治中心肝癌单病种首席专家
中国抗癌协会肝癌专业委员会前任主任委员
中国老年保健协会副会长
中国老年保健协会肝癌综合治疗专业委员会名誉主任委员
中国医师协会肝癌专业委员会副主任委员
中国临床肿瘤学会(CSCO)肝癌工作委员会副主任委员
广东省医学会肝癌分会前任主任委员
广东省抗癌协会肝癌专业委员会名誉顾问
中华医学会外科学分会肝脏外科学组委员
中华医学会肝病学分会肝癌学组委员
中华医学会肿瘤学分会肝癌学组委员

张耀军 教授
中山大学肿瘤防治中心肝脏外科行政副主任
博士生导师、主任医师、医学博士
中国老年保健协会肝癌综合治疗专业委员会 主任委员
中国医促会免疫治疗专委会副主任委员
中国抗癌协会肝癌专业委员会委员
广东省医师协会肝胆外科分会副主任委员
广东省肝病学会微创治疗专业委员会副主任委员
广州市医师协会肝胆胰外科医师分会副主任委员
广东省抗癌协会肝癌专业委员会常委
广东省医学会肝癌专业委员会委员
广东省杰出青年医学人才(第二批)
英国帝国理工大学( Imperial College London )访问学者

王骏成 副主任医师
中山大学肿瘤防治中心 肝脏外科
副主任医师、医学博士、助理研究员、硕士生导师
中国老年保健协会肝癌综合治疗专业委员会 委员
广东省器官医学与技术学会肝癌多学科综合治疗专业委员会 秘书长
广东省肝脏病学会肝癌专业委员会 委员
广东省基层医药学会转移性肝癌专业委员会 委员
长期从事肝癌临床与科研工作,专注于肝癌的围手术期及转化治疗。
主持国自然青年基金、广东省自然青年基金及广州市科技计划项目等课题4项。
以第一作者和通讯作者(含共同)在Cancer Research、Molecular Therapy、European Journal of Cancer、International Journal of Surgery、Surgery等国际知名期刊发表高水平论文10余篇。
来源:中山大学肿瘤防治中心肝脏外科
文:林庆扬、王骏成
编辑:lagertha
审核:陈敏山教授